某兴趣小组的同学为从含有FeSO4、CuSO4的废液中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
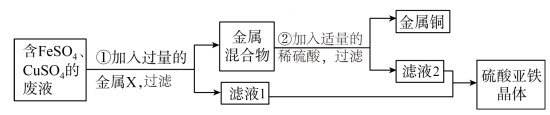
(1)过滤操作所需的玻璃仪器有___________ 、___________ 、___________ 。
(2)步骤①中,加入的金属X是___________ 。
(3)金属混合物的成分是___________ 。步骤②中,加入过量的稀硫酸的目的是___________ ,反应的化学方程式为___________ ,该反应属于___________ (填基本反应类型)。
(4)若实验过程中的物质损失可以忽略,最终得到的硫酸亚铁晶体的质量___________ (填“>”“=”或“<”)原废液中硫酸亚铁的质量。

(1)过滤操作所需的玻璃仪器有
(2)步骤①中,加入的金属X是
(3)金属混合物的成分是
(4)若实验过程中的物质损失可以忽略,最终得到的硫酸亚铁晶体的质量
更新时间:2022/02/27 22:09:34
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】钛及其合金大量用于航空工业。利用钛铁矿(FeTiO3)制备钛的主要转化过程如下:
(1)TiCl4中钛元素的化合价为___________ 。
(2)①中X为一种反应物,从元素守恒的角度推测,X可能是___________(填序号)。
(3)②中发生置换反应的化学方程式为___________ 。
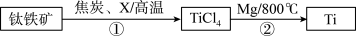
(1)TiCl4中钛元素的化合价为
(2)①中X为一种反应物,从元素守恒的角度推测,X可能是___________(填序号)。
| A.Cl2 | B.O2 | C.CO |
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
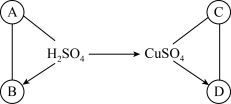
【推荐2】如图是初中化学常见物质间的反应及转化关系。(“→”表示物质间存在转化关系“一”表示相连物质相互间能反应,部分反应物和生成物已略去)。已知B是一种红色固体粉末,B、D是不同类别的物质,E、F含有相同的一种元素,由C反应生成E不属于化合反应。
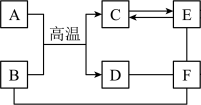
请完成下列问题:
(1)写出下列物质的化学式:D__________ 、E_________ 。
(2)写出C的用途_________ 。
(3)写出B与F反应的化学方程式_________ 。
(4)D和F发生反应的现象是__________ 。
(5)A和B的反应________ (填“是”、“不是”或“不一定是”)置换反应。

请完成下列问题:
(1)写出下列物质的化学式:D
(2)写出C的用途
(3)写出B与F反应的化学方程式
(4)D和F发生反应的现象是
(5)A和B的反应
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】铜是人类最早利用的金属之一。
⑴下列铜制品中,利用金属导热性的是________  填字母序号
填字母序号 。
。
A铜质奖牌 B铜导线 C铜锅
⑵利用废旧电池铜帽 含Cu、
含Cu、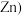 制取海绵铜
制取海绵铜 ,并得到硫酸锌溶液,主要流程如下
,并得到硫酸锌溶液,主要流程如下 反应条件已略去
反应条件已略去 :
:
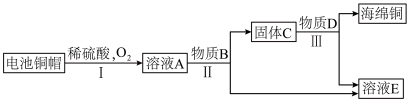
已知: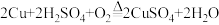
①过程Ⅲ中有气体产生,反应的化学方程式为___________ 。
② 中含铜、锌两种元素的物质有
中含铜、锌两种元素的物质有________  填字母序号
填字母序号 。
。
⑴下列铜制品中,利用金属导热性的是
 填字母序号
填字母序号 。
。A铜质奖牌 B铜导线 C铜锅
⑵利用废旧电池铜帽
 含Cu、
含Cu、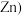 制取海绵铜
制取海绵铜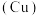 ,并得到硫酸锌溶液,主要流程如下
,并得到硫酸锌溶液,主要流程如下 反应条件已略去
反应条件已略去 :
:
已知:
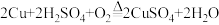
①过程Ⅲ中有气体产生,反应的化学方程式为
②
 中含铜、锌两种元素的物质有
中含铜、锌两种元素的物质有 填字母序号
填字母序号 。
。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】“沉睡三千年,一醒惊天下!”三星堆青铜器出土后立刻震惊了全世界。近日部分青铜器在呼和浩特市博物馆展出。
(1)青铜是由铜、锡熔合制成。相比于纯铜的质地柔软,青铜________ ,而应用于农具和兵器的生产中。
(2)《淮南万毕术》记载“曾青(硫酸铜溶液)得铁则化为铜”的湿法炼铜工艺,反应的化学方程式为________ 。
(3)小琦同学查阅资料发现: (氯化亚锡)溶于水可形成无色溶液。请你帮她设计实验方案证明锡的金属活动性强于铜
(氯化亚锡)溶于水可形成无色溶液。请你帮她设计实验方案证明锡的金属活动性强于铜________ (写出操作和现象)。
(4)出土的青铜器表面锈蚀物分为无害锈和有害锈。无害锈是一层致密薄膜,如铜绿;有害锈含氯,可加快青铜器锈蚀。锈层成分如图所示,下列叙述正确的是________。
(1)青铜是由铜、锡熔合制成。相比于纯铜的质地柔软,青铜
(2)《淮南万毕术》记载“曾青(硫酸铜溶液)得铁则化为铜”的湿法炼铜工艺,反应的化学方程式为
(3)小琦同学查阅资料发现:
 (氯化亚锡)溶于水可形成无色溶液。请你帮她设计实验方案证明锡的金属活动性强于铜
(氯化亚锡)溶于水可形成无色溶液。请你帮她设计实验方案证明锡的金属活动性强于铜(4)出土的青铜器表面锈蚀物分为无害锈和有害锈。无害锈是一层致密薄膜,如铜绿;有害锈含氯,可加快青铜器锈蚀。锈层成分如图所示,下列叙述正确的是________。
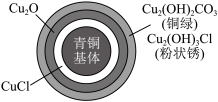
| A.图中的CuCl和粉状锈均是有害锈 |
B.形成铜绿的过程中有 、 、 参与,与 参与,与 无关 无关 |
| C.青铜器锈蚀的过程中铜元素的化合价未变化 |
| D.保护青铜器最重要的是防氯 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】铁锈的主要成分是Fe2O3,为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的盐酸中,他首先看到锈迹溶解,溶液呈____________ 色.这是因为(用化学方程式表示)____________ ;不一会儿,又看到溶液中有__________ 的现象,这是因为(用化学方程式表示)___________________ .
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】实验室废弃液中含一定量的AgNO3,兴趣小组同学回收金属银的流程如下:
(1)操作I、II所需要的玻璃仪器有:烧杯、玻璃棒、_______ .
(2)讨论a的选择:甲同学认为用锌,乙同学认为用铜,你认为_______ (选填“甲”或“乙”),你选择的理由是_______ ,加入a发生反应的化学方程式是_______ .
(3)固体B的成分是_______ (填化学式).
(4)向固体B加入适量稀硫酸后反应的化学方程式为_______________ .

(1)操作I、II所需要的玻璃仪器有:烧杯、玻璃棒、
(2)讨论a的选择:甲同学认为用锌,乙同学认为用铜,你认为
(3)固体B的成分是
(4)向固体B加入适量稀硫酸后反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“变化观念”是化学核心素养之一,以盐酸为例,多角度认识物质,回答下列问题。
(1)认识物质的构成:稀盐酸中含有大量的阳离子是_______ 。
(2)认识物质的性质:打开浓盐酸的瓶盖,观察到瓶口有______ 产生,说明浓盐酸具有挥发性。
(3)认识物质的变化,盐酸的5条化学性质如图所示:______ (填字母)。
a.无色酚酞溶液 b.紫色石蕊溶液
②为了探究盐酸的性质2,现将金属甲、乙放入足量的稀盐酸中,观察到的现象如下:甲表面有气泡产生且溶液变为浅绿色,乙无明显现象,由此推断甲、乙的金属活动性强弱顺序为________ 。写出金属甲与稀盐酸反应的化学方程式:_______ 。
③为了探究盐酸的性质4,某同学将碳酸钙与盐酸反应,观察到有汽泡产生,该气体成分是_______ 。
④若要验证盐酸的性质5,可选择下列哪种物质与盐酸反应达到目的:_______ 。
a.NaOH b.Na2CO3 c.Ca(OH)2 d.H2SO4
(4)认识物质的用途:稀盐酸可用于除铁锈,观察到的实验现象是_______ 。
(1)认识物质的构成:稀盐酸中含有大量的阳离子是
(2)认识物质的性质:打开浓盐酸的瓶盖,观察到瓶口有
(3)认识物质的变化,盐酸的5条化学性质如图所示:
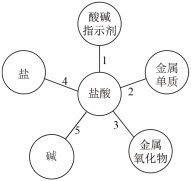
a.无色酚酞溶液 b.紫色石蕊溶液
②为了探究盐酸的性质2,现将金属甲、乙放入足量的稀盐酸中,观察到的现象如下:甲表面有气泡产生且溶液变为浅绿色,乙无明显现象,由此推断甲、乙的金属活动性强弱顺序为
③为了探究盐酸的性质4,某同学将碳酸钙与盐酸反应,观察到有汽泡产生,该气体成分是
④若要验证盐酸的性质5,可选择下列哪种物质与盐酸反应达到目的:
a.NaOH b.Na2CO3 c.Ca(OH)2 d.H2SO4
(4)认识物质的用途:稀盐酸可用于除铁锈,观察到的实验现象是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】碳酸锂(Li2CO3)是制备锂电池的重要原料。工业上以锂辉石精矿(主要成分为Li2O)为原料制取碳酸锂的主要工艺流程及碳酸锂的溶解度表如下:
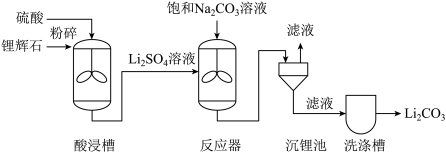
请回答下列问题:
(1)将锂辉石粉碎的目的是_______________ 。
(2)沉锂池中,分离固体和液体的操作是____ ,所需的玻璃仪器有____ 、烧杯、玻璃棒。
(3)酸浸槽中,发生反应的化学方程式为____ 。结合碳酸锂的溶解度表,洗涤槽中应用_____ (填“冷水”或“热水”)洗涤。

| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 碳酸锂的溶解度/g | 1.55 | 1.33 | 1.18 | 1.00 | 0.82 |
(1)将锂辉石粉碎的目的是
(2)沉锂池中,分离固体和液体的操作是
(3)酸浸槽中,发生反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】金属材料对于促进生产发展、改善人类生活发挥了重大作用。
(1)从废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:

①图中“操作”的名称是______ 。
②提炼得到的贵重金属有______ 。
③反应Ⅰ中发生的化学反应方程式为______ (写一个);
该反应的基本类型为______ 。
④反应Ⅱ中发生的化学反应方程式为______ 。
(2)下列保护金属资源的做法不正确的是______ (填字母序号)。
A.任意开采金属矿物 B.回收利用废旧金属
C.铁制品存放在潮湿的环境中 D.用塑料代替金属材料制造管道
(1)从废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:

①图中“操作”的名称是
②提炼得到的贵重金属有
③反应Ⅰ中发生的化学反应方程式为
该反应的基本类型为
④反应Ⅱ中发生的化学反应方程式为
(2)下列保护金属资源的做法不正确的是
A.任意开采金属矿物 B.回收利用废旧金属
C.铁制品存放在潮湿的环境中 D.用塑料代替金属材料制造管道
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组回收利用废旧干电池。
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如下图所示。

(1)操作1和操作2的名称都是_____ ,该操作中玻璃棒的作用是_____ 。
(2)灼烧滤渣l的目的是除去_____ 物质。
(3)已知滤液1中氯化铵和氯化锌的浓度相近。在某温度下蒸发滤液1时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度_____ 氯化锌的溶解度(填“<”、“=”或“>”)。
(4)氯化铵晶体可以作为_____ 肥,氯化铵与氯化锌都是白色的固体,析出的是氯化铵还是氯化锌,鉴别的方法是:取少量样品于_____ (填仪器名称)中和_____ (填药品名称)混合研磨,有_____ 现象的是氯化铵,该反应的化学方程式是_____ 。
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如下图所示。

(1)操作1和操作2的名称都是
(2)灼烧滤渣l的目的是除去
(3)已知滤液1中氯化铵和氯化锌的浓度相近。在某温度下蒸发滤液1时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度
(4)氯化铵晶体可以作为
您最近一年使用:0次

 。某研究性学习小组设计如图流程以回收铜和硫酸亚铁(加入试剂均过量),请回答下列问题:
。某研究性学习小组设计如图流程以回收铜和硫酸亚铁(加入试剂均过量),请回答下列问题:


