某澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl-、OH-和 离子中的一种或几种,为确定溶液中可能存在的离子,进行下面实验:
离子中的一种或几种,为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成,继续滴加NaOH溶液至不再产生沉淀为止,过滤;
③向实验②得到的滤液中滴加Na2CO3溶液,又观察到沉淀生成。
分析实验得出的以下结论中,正确的是
 离子中的一种或几种,为确定溶液中可能存在的离子,进行下面实验:
离子中的一种或几种,为确定溶液中可能存在的离子,进行下面实验:①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成,继续滴加NaOH溶液至不再产生沉淀为止,过滤;
③向实验②得到的滤液中滴加Na2CO3溶液,又观察到沉淀生成。
分析实验得出的以下结论中,正确的是
A.溶液中一定含有H+、Ba2+、Cl-,一定不含有Na+、Fe3+、OH-、 |
B.溶液中一定含有H+、Ba2+、Fe3+,一定不含有OH-和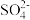 ,可能含有Na+、Cl- ,可能含有Na+、Cl- |
C.溶液中一定含有H+、Ba2+、Fe3+、Cl-,一定不含有OH-、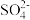 ,可能含有Na+ ,可能含有Na+ |
D.溶液中一定含有H+、Ba2+、Na+、Fe3+,一定不含有OH-、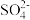 ,可能含有Cl- ,可能含有Cl- |
更新时间:2022-03-04 16:22:52
|
相似题推荐
选择题-单选题
|
较难
(0.4)
名校
【推荐1】现有氯化钠和碳酸钠的混合物17 g,向其中加入一定量的硝酸银溶液至恰好不再产生沉淀,将沉淀过滤洗涤干燥后称量其质量为42.5 g,并得到不饱和溶液274.5 g。则加入的硝酸银溶液的溶质质量分数为( )
| A.17% |
| B.34% |
| C.20% |
| D.51% |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】下列叙述正确的是
| A.除去 CO2 中少量的 CO,通过灼热的铜粉 |
| B.K2CO3、NaOH、稀 HCl、BaCl2 四种物质的水溶液,不用其他试剂就能鉴别出来 |
| C.NaCl、KOH、Na2CO3 在 pH=3 的溶液中能够共存,并形成无色透明液体 |
| D.AgNO3、BaCl2、H2SO4 的溶液中能够大量共存 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐3】甲、乙、丙、丁四种溶液中,分别含有 Ba2+、Mg2+、Na+、H+、OH﹣、Cl﹣、CO32﹣、SO42-中的一种阳离子和一种阴离子,为确定四溶液中分别含有哪种阳离子或阴离子,进行了下面实验:将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成;将乙、丁溶液混合,有气泡产生;向丙溶液中滴入硝酸银溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失.分析实验得到的以下结论,不正确的是( )
| A.甲溶液中一定含有钡离子 |
| B.乙溶液中可能含有硫酸根离子 |
| C.丙溶液中一定含有氯离子 |
| D.丁溶液中一定含有钠离子 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐1】有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种。取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如下图所示。由此推断白色固体中


| A.可能存在Na2SO4 | B.可能存在NaOH |
| C.可能存在BaCl2 | D.肯定只存在Na2CO3 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】有一瓶久置的氢氧化钠溶液,为了探究该溶液是否变质以及变质的程度,设计了如下方案,根据方案流程,说法错误的是


| A.由步骤①可知该氢氧化钠溶液已经变质 |
| B.若步骤②中“现象I”生产白色沉淀,结论是该氢氧化钠溶液部分变质 |
| C.若步骤②中“现象I”无明显现象,结论是该氢氧化钠溶液完全变质 |
| D.步骤①中的CaCl2溶液可以用Ca(NO3)2溶液代替,也可以用Ca(OH)2溶液代替 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐1】下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的是( )
| 选项 | 物质 | 目的 | 主要实验操作 |
| A | CH4、CO气体 | 区分 | 点燃,火焰上方罩一干冷烧杯,观察现象 |
| B | Cu(NO3)2(AgNO3)溶液 | 除杂 | 加入过量的铜、过滤 |
| C | Na2CO3 (NaOH) | 检验 | ①取样,加水溶解 ②滴加无色酚酞,观察溶液是否变红 |
| D | MnO2、KCl固体 | 分离 | 溶解、过滤、洗涤、烘干、蒸发 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
【推荐2】对于某些离子的检验及结论一定正确的是
| A.加入稀盐酸产生无色气体 ,一定有CO32- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐1】有一包白色固体粉末,可能含有CuSO4、Ba(NO3)2、BaSO4、Na2CO3、KCl中的一种或几种,某同学对其组成进行了探究,过程如下:根据以上实验操作与现象,该同学得出的结论不正确的是( )


| A.白色沉淀A中含有BaCO3和BaSO4 |
| B.无色溶液F中最少有4种离子 |
| C.原混合物中一定不含CuSO4,一定含有Ba(NO3)2、BaSO4、Na2CO3 |
| D.确定原固体混合物中是否有KCl,可取白色沉淀E加入足量稀硝酸,观察沉淀是否溶解 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
【推荐2】固体X可能由氢氧化钠、碳酸钠、氯化钠、硝酸镁、硝酸钡、硫酸钠、硫酸铜中的一种或几种物质组成(提示:以上物质中,只有氢氧化钠和碳酸钠的水溶液显碱性)。为确定其组成,进行如下实验:①将固体X 加入水中充分溶解,得到无色溶液 ②测X溶液的pH值,pH=13 ③向X的溶液中加入足量的硝酸钡溶液,产生白色沉淀,过滤 ④向步骤③所得沉淀中加入足量的稀盐酸,沉淀不溶解 ⑤向步骤③所得的滤液中加入过量的稀硝酸,再加入硝酸银溶液,产生白色沉淀。根据以上实验信息,下列关于固体X组成的判断正确的是
| A.硫酸钠、氢氧化钠、氯化钠一定存在 | B.不能确定是否有氯化钠 |
| C.一定不存在的只有硫酸铜、硝酸钡、碳酸钠 | D.不能确定是否有硝酸镁 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐3】一包白色粉末,可能含有CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的一种或几种。为探究其组成进行如下实验:
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
②取实验①滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体;
③取实验①得到的滤液,向其中通入CO2,产生白色沉淀;
根据以上实验现象,判断白色粉末。下列结论不正确 的是
①取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
②取实验①滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体;
③取实验①得到的滤液,向其中通入CO2,产生白色沉淀;
根据以上实验现象,判断白色粉末。下列结论
| A.白色粉末中一定不含CuSO4、Na2SO4 | B.白色粉末中一定含有CaCO3、BaCl2 |
| C.白色粉末中一定含有CaCO3、BaCl2、NaOH | D.白色粉末中可能含有NaOH |
您最近一年使用:0次



