为测定某石灰石样品中碳酸钙的质量分数,取2.0g石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经一系列的操作,得实验数据如下:
已知石灰石中的杂质既不与盐酸反应,也不溶解于水。请回答下列问题。
(1)检验上述反应所产生气体的方法为__________ 。
(2)样品中碳酸钙的质量分数为__________ 。
(3)所用稀盐酸的溶质质量分数______ (写出计算过程)。
(4)第四次实验后所得溶液中钙元素的质量为_______ g。
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 稀盐酸的用量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固体的质量/g | 1.5 | 1.0 | 0.5 | 0.3 |
(1)检验上述反应所产生气体的方法为
(2)样品中碳酸钙的质量分数为
(3)所用稀盐酸的溶质质量分数
(4)第四次实验后所得溶液中钙元素的质量为
2022·江西宜春·一模 查看更多[3]
更新时间:2022-03-28 22:25:51
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】取得Cu—Zn合金粉末20g放入烧杯中,加入50g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为69.8g。
求:①产生氢气的质量
②求稀硫酸溶液的溶质质量分数
③求反应后所得溶液的溶质质量分数
求:①产生氢气的质量
②求稀硫酸溶液的溶质质量分数
③求反应后所得溶液的溶质质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】一定质量的碳酸钙高温煅烧一段时间后生成二氧化碳 22g,测得剩余固体中碳元素的质量分数为6%。计算:
(1)根据化学方程式计算,参加反应的碳酸钙的质量;
(2)剩余固体的质量。
(1)根据化学方程式计算,参加反应的碳酸钙的质量;
(2)剩余固体的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】实验室制取氧气时,某学习小组同学将5g氯酸钾和二氧化锰的混合物加热至质量不再变化为止,实验过程中测得某些物质的质量与加热时间的关系图像如图所示。回答下列问题:
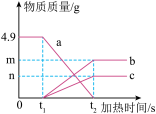
(1)在0~t1时间段内各物质质量没有发生明显变化的原因是___________ 。
(2)图中b代表的物质是___________ ,m+n的值为___________ 。
(3)计算生成氧气的质量。(写出计算过程)
(4)充分反应后,将剩余的固体混合物加入足量水充分溶解后过滤、洗涤、干燥,称量得到的黑色固体的质量为___________ g。

(1)在0~t1时间段内各物质质量没有发生明显变化的原因是
(2)图中b代表的物质是
(3)计算生成氧气的质量。(写出计算过程)
(4)充分反应后,将剩余的固体混合物加入足量水充分溶解后过滤、洗涤、干燥,称量得到的黑色固体的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】化学小组的同学对赤铁矿样品进行了探究。他们称取了20g赤铁矿样品,用图1所示的装置进行实验,实验过程中测得集气瓶内的物质总质量随时间的关系图像如图2所示(假设赤铁矿中的杂质不与CO反应,且不考虑空气与澄清石灰水反应)。请回答有关问题:
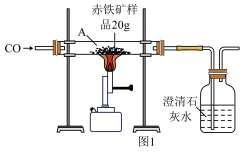

(1)图1中A处固体颜色的变化是______ ,该反应产生的CO2气体的质量为______ g。
(2)计算赤铁矿样品中氧化铁的质量分数。(写出计算过程)
(3)待充分反应后,图1中A处固体的质量为______ g。
(4)从环保的角度分析,图1装置需要进行改进,你的改进方法是______ 。


(1)图1中A处固体颜色的变化是
(2)计算赤铁矿样品中氧化铁的质量分数。(写出计算过程)
(3)待充分反应后,图1中A处固体的质量为
(4)从环保的角度分析,图1装置需要进行改进,你的改进方法是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】取一定量的木炭在氧气中燃烧,生成23.2 g气体(氧气已完全反应)。将气体通入过量的澄清石灰水中,生成40 g沉淀。
计算:
(1)生成气体的成分及质量___________。
(2)生成气体中碳元素的质量分数_________。
计算:
(1)生成气体的成分及质量___________。
(2)生成气体中碳元素的质量分数_________。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】氯化钙钾石的化学式为KCl·xCaC12(x是CaCl2的系数)。它是一种天然的钾肥,溶于水后得到KCl与CaCl2的混合溶液。某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解得到KCl与CaCl2的混合溶液,向该溶液中逐滴加入Na2CO3溶液,产生的沉淀与加入Na2CO3溶液的质量关系如下图所示。请回答下列问题:

(1)写出Na2CO3与CaCl2反应的化学方程式______ 。
(2)图中AB段表示的意义是_________ 。
(3)18.55g氯化钙钾石样品中:
①CaCl2的质量是______ g;
②KCl的质量是____ g;
③钾元素的质量分数是______ 。
(4)所用Na2CO3溶液中溶质的质量分数是多少?(最后一问要求写出计算过程)____________

(1)写出Na2CO3与CaCl2反应的化学方程式
(2)图中AB段表示的意义是
(3)18.55g氯化钙钾石样品中:
①CaCl2的质量是
②KCl的质量是
③钾元素的质量分数是
(4)所用Na2CO3溶液中溶质的质量分数是多少?(最后一问要求写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
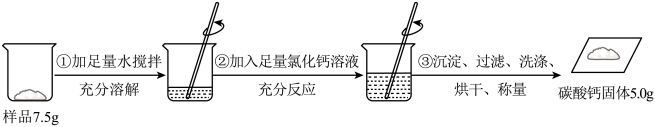
【推荐2】为了探究煅烧了一段时间的石灰石中各成分的质量(其中杂质高温不分解、不溶于水也不与酸反应),进行了如下图所示的实验,请回答下列问题:

(1)写出有气体生成 的化学反应方程式______ ;
(2)列出求解所探究的固体中碳酸钙质量(X)的比例式______ ;
(3)求解最终所得的不饱和溶液中溶质的质量分数,并填写在标签上。

(4)若用36.5%的浓盐酸加水稀释配制实验所需的稀盐酸,在实验过程中需要的仪器有量筒、玻璃棒,其中缺少的仪器有______ ;

(1)写出
(2)列出求解所探究的固体中碳酸钙质量(X)的比例式
(3)求解最终所得的不饱和溶液中溶质的质量分数,并填写在标签上。

(4)若用36.5%的浓盐酸加水稀释配制实验所需的稀盐酸,在实验过程中需要的仪器有量筒、玻璃棒,其中缺少的仪器有
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某碳酸钠样品中混有少量氯化钠,根据如图所示信息完成相关计算。
(反应的化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl)
(1)Na2CO3由 种元素组成;
(2)一个Na2CO3分子中Na、C、O的原子个数比为 ;
(3)Na2CO3中氧元素的质量分数是 %(结果精确到0.1%);
(4)计算该样品中碳酸钠的质量分数。(写出计算过程,结果精确到0.1%)
(反应的化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl)

(1)Na2CO3由 种元素组成;
(2)一个Na2CO3分子中Na、C、O的原子个数比为 ;
(3)Na2CO3中氧元素的质量分数是 %(结果精确到0.1%);
(4)计算该样品中碳酸钠的质量分数。(写出计算过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物主要是尿素.若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出体外,每人每天相当于排出尿素30g.尿素是一种优质的氮肥,其化学式为:CO(NH2)2,据此我能计算:
(1)尿素的相对分子质量为_____;其中C和H的质量比为_____.
(2)30g尿素中含氮元素_____g.
(3)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质为_____g.
(1)尿素的相对分子质量为_____;其中C和H的质量比为_____.
(2)30g尿素中含氮元素_____g.
(3)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质为_____g.
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】蔗糖是重要的食品和调味品,易溶于水形成蔗糖溶液,其化学式为C12H22O11
(1)蔗糖的相对分子质量是___________ 从物质的分类看,蔗糖溶液属于___________ (选填单质、化合物、氧化物、混合物)
(2)若使蔗糖中氧元素的质量与36克水中氧元素的质量相等,则蔗糖的质量是多少?(请写出计算过程,结果精确到小数点后一位)
(3)蔗糖溶液中氢元素的质量分数可能是___________
(4)蔗糖溶液中,若氧元素的质量分数为80%,则碳元素的质量分数___________ 。
(1)蔗糖的相对分子质量是
(2)若使蔗糖中氧元素的质量与36克水中氧元素的质量相等,则蔗糖的质量是多少?(请写出计算过程,结果精确到小数点后一位)
(3)蔗糖溶液中氢元素的质量分数可能是___________
| A.2% | B.5% | C.7% | D.14% |
您最近一年使用:0次



