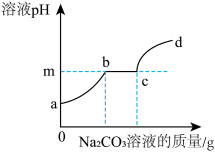
磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等(SiO2几乎不溶于水和常见的酸)。
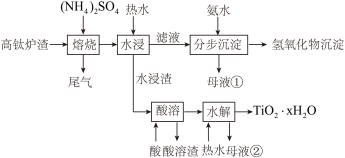
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
回答下列问题:
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是______ ,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为NH4Al(SO4)2的化学方程式为: 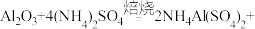
______ 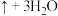 。
。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是________ (按先后顺序填写)。
(3)实验室进行过滤时玻璃棒的作用________ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是________ 。“酸溶渣”的成分是_______ 、CaSO4。
(5)氢氧化物沉淀中的________ 、_________ 能用来制备治疗胃酸过多的药物,写出一个用氢氧化物治疗胃酸过多的化学方程式________ 。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到_______ ,循环利用;农业上也可以用作___________ 。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
| 金属离子 | Fe3+ | A13+ | Mg2+ | Ca2+ |
| 开始沉淀的pH | 2.2 | 3.5 | 9.5 | 12.4 |
| 沉淀完全的pH | 3.2 | 4.7 | 11.1 | 13.8 |
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是
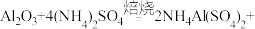
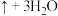 。
。(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是
(3)实验室进行过滤时玻璃棒的作用
(4)“水浸渣”在160℃“酸溶”最适合的酸是
(5)氢氧化物沉淀中的
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到
更新时间:2022-04-05 12:13:17
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】稀土金属因其独特的性能而被誉为“新材料之母”。稀土金属钇的氧化物(Y2O3)广泛应用于航空航天涂层材料,其颗粒大小决定了产品的质量。利用富钇稀土(含Y2O3约70%, 含Fe2O3、CuO、SiO2等约30%)生产大颗粒-氧化钇的一种工艺如下:

(1)操作I的名称是_____ 。
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是______ 。
(3)“分离提纯”是为了除去滤液1中的_____ (填化学式)。
(4)“调pH”时加入碱液使溶液的pH_____ (填“增大”或“减小”)。
(5)碳酸钇灼烧分解的化学方程式是_____ ,此反应属于基本反应类型中的_____ 反应。

(1)操作I的名称是
(2)“酸溶”过程中,氧化钇与盐酸反应的化学方程式是
(3)“分离提纯”是为了除去滤液1中的
(4)“调pH”时加入碱液使溶液的pH
(5)碳酸钇灼烧分解的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐2】燃煤产生的烟气中含有二氧化硫,直接排放会污染空气,它与水反应形成酸雨污染环境,某科研小组利用海水除去二氧化硫,其工艺流程见下图:
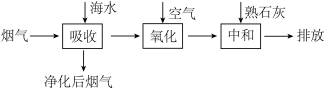
请回答下列问题:
(1)二氧化硫中硫的化合价是________ 。
(2)用熟石灰中和稀硫酸的化学方程式是_________ 。
(3)亚硫酸(H2SO3)被空气中氧气氧化为硫酸,写出反应的化学方程式_________ 。
(4)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比——与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
由表中实验数据可得出的结论是 ______ 。
(5)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+。
①反应中Cu+的作用是________ 。
②除去二氧化硫的总反应的化学方程式是________ 。

请回答下列问题:
(1)二氧化硫中硫的化合价是
(2)用熟石灰中和稀硫酸的化学方程式是
(3)亚硫酸(H2SO3)被空气中氧气氧化为硫酸,写出反应的化学方程式
(4)为了研究脱硫率(脱硫率是已除去的二氧化硫的量占总二氧化硫量的百分比——与温度、烟气中SO2浓度的关系,他们进行了探究实验。实验结果如下:
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g·L-1 | 脱硫率/% |
| I | 23 | 2.5% | 99.5 |
| II | 23 | 3.2% | 97.1 |
| III | 40 | 2.5% | 94.3 |
(5)目前,科学家正在研究在一定条件下将乙烯(C2H4)和烟气混合除去二氧化硫,其反应的过程可分为如下三步:
第一步:O2与Cu+反应生成Cu+(O2)
第二步:Cu+(O2)与SO2反应生成Cu+(SO3)2
第三步:Cu+(SO3)2与C2H4反应生成S、CO2、H2O和Cu+。
①反应中Cu+的作用是
②除去二氧化硫的总反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】生活离不开化学,用所学化学知识回答下列问题:
(1)日常生活中食用的鸡蛋、脱脂奶中富含的营养素是_______ 。为了防止佝偻病及发育不良,幼儿青少年可以补充一些含________ 元素的食品。
(2)下列主要用有机合成材料制成的是_________ 。(填标号)
A.羊毛衫 B.涤纶连衣裙 C.纯棉T恤
(3)正常人的胃液中含有约0.5%的盐酸。某种胃药中含有Al(OH)3,能治疗胃酸过多的疾病。服药后发生的化学反应方程式为____ ,该反应属于____ (填写基本反应类型)。
(4)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有___________ 的功能.
(5)A、B两种物质是初中阶段常见化合物,由相同元素组成 且A的相对分子质量比B大。
① 若A、B均为气体,且A、B可以互相转化,则A→B的化学方程式为___________
② 若A、B两种液体均能转化为气体C,则C的化学式为___________ 。
(1)日常生活中食用的鸡蛋、脱脂奶中富含的营养素是
(2)下列主要用有机合成材料制成的是
A.羊毛衫 B.涤纶连衣裙 C.纯棉T恤
(3)正常人的胃液中含有约0.5%的盐酸。某种胃药中含有Al(OH)3,能治疗胃酸过多的疾病。服药后发生的化学反应方程式为
(4)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有
(5)A、B两种物质是初中阶段常见化合物,
① 若A、B均为气体,且A、B可以互相转化,则A→B的化学方程式为
② 若A、B两种液体均能转化为气体C,则C的化学式为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的化学性质,因为不同的酸溶液中都含有______ (填化学符号)。若浓硫酸不慎溅到皮肤上,应立即用大量水冲洗,再涂上 3%-5%的______ 溶液。
(2)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液 pH 变化,实验结果如图:
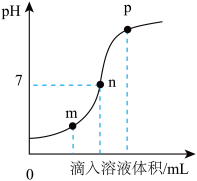
① 根据图示判断,该实验是将______ (填“氢氧化钠溶液”或“盐酸”)滴加到另一种溶液中。
② 该实验共用到 7.3%的稀盐酸 20g。在配置稀盐酸时,量取水仰视量筒读数,所配盐酸溶液的溶质质量分数______ 7.3%(填“大于”或“等于”或“小于”)。
③ 若取 m 点时的溶液,滴加硝酸银溶液,发现有白色沉淀生成,从而证明稀盐酸有剩余。小明认为该做法不对,理由是______ (请用化学方程式解释)。若滴加足量硝酸银溶液,共生成沉淀______ g。
(3)某溶液可能含有盐酸、硫酸、碳酸钠、氯化钠、氯化镁中的一种或几种,为了探究其组成,进行如下实验:
步骤 1:取少量该溶液,测其 pH=3 ;
步骤 2:向少量该溶液中逐滴加入氢氧化钡溶液,刚开始没有明显现象,过一会儿后有沉淀产生。该溶液中一定没有的是______ (填化学式)。
(1)酸具有相似的化学性质,因为不同的酸溶液中都含有
(2)利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液 pH 变化,实验结果如图:

① 根据图示判断,该实验是将
② 该实验共用到 7.3%的稀盐酸 20g。在配置稀盐酸时,量取水仰视量筒读数,所配盐酸溶液的溶质质量分数
③ 若取 m 点时的溶液,滴加硝酸银溶液,发现有白色沉淀生成,从而证明稀盐酸有剩余。小明认为该做法不对,理由是
(3)某溶液可能含有盐酸、硫酸、碳酸钠、氯化钠、氯化镁中的一种或几种,为了探究其组成,进行如下实验:
步骤 1:取少量该溶液,测其 pH=3 ;
步骤 2:向少量该溶液中逐滴加入氢氧化钡溶液,刚开始没有明显现象,过一会儿后有沉淀产生。该溶液中一定没有的是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】以绿矾(FeSO4・7H2O)为原料制备高铁酸钾(K2FeO4)的流程如下:
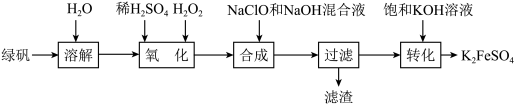
(1)“氧化”是将FeSO4,转化为Fe2(SO4)3,该反应的化学方程式为__ 。
(2)“合成”时发生的反应为Fe2(SO4)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+3X+5H2O,X的化学式为____ 。
(3)不同温度和pH下FeO42-在水溶液中的稳定性如图所示。
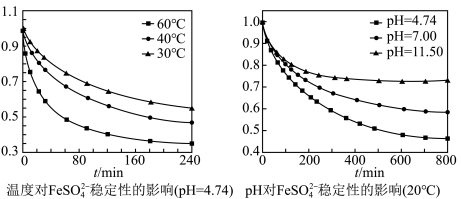
图中纵坐标表示单位体积内FeO42-离子数目的多少,数值越小,表明FeO42-离子数目越少,在该条件下越不稳定。为了提高“合成”时Na2FeO4的产率,下列措施可行的是____
A 充分搅拌反应液
B 控制反应在60℃左右进行
C 控制反应在碱性条件下进行
(4)“滤渣”呈红褐色,推测其主要成分为____ (填化学式)。
(5)常温下向“过滤”后的滤液中加入饱和KOH溶液,即可析出K2FeO4晶体,由以上信息可知K2FeO4的溶解度比Na2FeO4的溶解度_______ (填“大”或“小”)。

(1)“氧化”是将FeSO4,转化为Fe2(SO4)3,该反应的化学方程式为
(2)“合成”时发生的反应为Fe2(SO4)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+3X+5H2O,X的化学式为
(3)不同温度和pH下FeO42-在水溶液中的稳定性如图所示。

图中纵坐标表示单位体积内FeO42-离子数目的多少,数值越小,表明FeO42-离子数目越少,在该条件下越不稳定。为了提高“合成”时Na2FeO4的产率,下列措施可行的是
A 充分搅拌反应液
B 控制反应在60℃左右进行
C 控制反应在碱性条件下进行
(4)“滤渣”呈红褐色,推测其主要成分为
(5)常温下向“过滤”后的滤液中加入饱和KOH溶液,即可析出K2FeO4晶体,由以上信息可知K2FeO4的溶解度比Na2FeO4的溶解度
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】碱式碳酸镁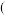 化学式为
化学式为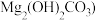 是一种新型阻燃剂,其工业制备流程如下:
是一种新型阻燃剂,其工业制备流程如下:
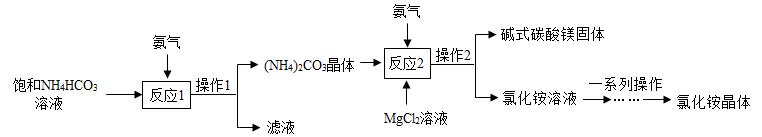
 操作1的名称是
操作1的名称是______ ,所用的玻璃仪器是______  填写一种即可
填写一种即可 。
。
 写出“反应2”的化学方程式:
写出“反应2”的化学方程式:______ 。
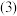 副产品氯化铵
副产品氯化铵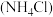 中铵根离子的化合价为
中铵根离子的化合价为______ 。
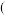 化学式为
化学式为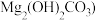 是一种新型阻燃剂,其工业制备流程如下:
是一种新型阻燃剂,其工业制备流程如下:
 操作1的名称是
操作1的名称是 填写一种即可
填写一种即可 。
。 写出“反应2”的化学方程式:
写出“反应2”的化学方程式: 副产品氯化铵
副产品氯化铵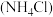 中铵根离子的化合价为
中铵根离子的化合价为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
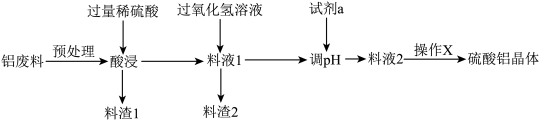
【推荐2】硫酸铝在造纸、水净化、土壤改良中有广泛的应用,某化工厂利用炼铝厂废料(主要成分含Al、Al2O3、SiO2、FeO、Fe2O3)制备硫酸铝晶体的工艺流程如图所示,回答以下问题。
查阅资料:部分金属离子生成氢氧化物开始沉淀和沉淀完全的pH范围:
资料:加入过氧化氢溶液使得溶液中的亚铁离子转化为铁离子。
(1)“预处理”时需要将铝废料粉碎,其目的是_______ 。
(2)料液1中含有的阳离子是______ ,料渣1的成分是______ 。
(3)试剂a用来调pH使得部分离子沉淀,为了不引入新的杂质,试剂A最好选用______ 。
A.氧化铝 B.氢氧化钾 C.氢氧化钠 D.稀硫酸
pH的范围应该控制在______ 。
(4)操作X是蒸发浓缩、______ 、过滤、洗涤、干燥。
查阅资料:部分金属离子生成氢氧化物开始沉淀和沉淀完全的pH范围:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀的pH | 3.6 | 6.3 | 2.3 |
| 沉淀完全的pH | 4.9 | 8.3 | 3.2 |
(1)“预处理”时需要将铝废料粉碎,其目的是
(2)料液1中含有的阳离子是
(3)试剂a用来调pH使得部分离子沉淀,为了不引入新的杂质,试剂A最好选用
A.氧化铝 B.氢氧化钾 C.氢氧化钠 D.稀硫酸
pH的范围应该控制在
(4)操作X是蒸发浓缩、
您最近一年使用:0次
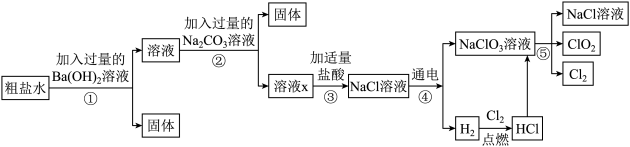
【推荐3】二氧化氯(C1O2)是一种高效、光谱、安全的杀菌消毒剂,可应用于自来水和公共场所的杀菌消毒处理。化工生产中通常以粗盐水(只含可溶性杂质MgSO4、CaCl2)为原料,通过五个步骤制取ClO2,工艺流程如下图:______ ,步骤①中不能用Ba(NO3)2代替Ba(OH)2,原因是:______ ;
(2)步骤②得到的固体除了CaCO3之外,还有______ (填名称),溶液X中的溶质有______ (填化学式);
(3)步骤④发生反应的化学方程式为______ 。
(2)步骤②得到的固体除了CaCO3之外,还有
(3)步骤④发生反应的化学方程式为
您最近一年使用:0次