碱式碳酸镁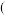 化学式为
化学式为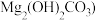 是一种新型阻燃剂,其工业制备流程如下:
是一种新型阻燃剂,其工业制备流程如下:
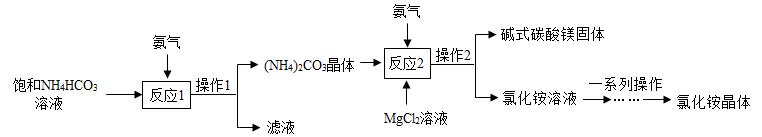
 操作1的名称是
操作1的名称是______ ,所用的玻璃仪器是______  填写一种即可
填写一种即可 。
。
 写出“反应2”的化学方程式:
写出“反应2”的化学方程式:______ 。
 副产品氯化铵
副产品氯化铵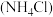 中铵根离子的化合价为
中铵根离子的化合价为______ 。
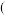 化学式为
化学式为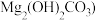 是一种新型阻燃剂,其工业制备流程如下:
是一种新型阻燃剂,其工业制备流程如下:
 操作1的名称是
操作1的名称是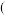 填写一种即可
填写一种即可 。
。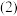 写出“反应2”的化学方程式:
写出“反应2”的化学方程式: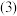 副产品氯化铵
副产品氯化铵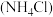 中铵根离子的化合价为
中铵根离子的化合价为
更新时间:2019-03-07 21:44:09
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
真题
【推荐1】有一包白色固体粉末,可能含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl、KCl中的一种或几种.现做如下实验:
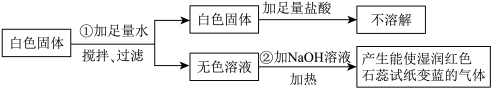
根据上述实验现象判断:
(1)白色固体中一定不含_______________ ,一定含有________ ,可能含有_____ .
(2)写出①中化学反应方程式___________________________ .
(3)写出②中化学反应方程式___________________________ .

根据上述实验现象判断:
(1)白色固体中一定不含
(2)写出①中化学反应方程式
(3)写出②中化学反应方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E是初中化学中常见的物质,均由碳、氢、氧中的一种或几种元素组成。其中C能供给呼吸;D是一种气体肥料;E由三种元素组成,可作燃料。这些物质之间的转化关系如图所示。
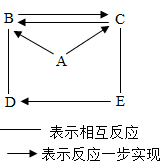
(1)B的化学式为_______________ 。B→C的基本反应类型是_____________ 。
(2)反应A→B的化学方程式是____________________ 。
(3)反应E→D的化学方程式是____________________ 。

(1)B的化学式为
(2)反应A→B的化学方程式是
(3)反应E→D的化学方程式是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
【推荐1】现有四只烧杯,分别盛有稀盐酸、饱和石灰水、碳酸钠溶液中的一种,并向其中滴加了酚酞或石蕊溶液(如下图所示)。
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性。
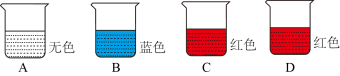
选用下列药品继续实验:铁、氧化钙、氧化铁、稀盐酸、饱和石灰水、碳酸钠溶液请依据实验回答问题:
(1)B 中溶液是________ 。
(2)取A 中溶液于试管中,加入甲,溶液由无色变为黄色,则甲是_______ ,反应的化学方程式为_______ 。
(3)取C中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为_______ 。
(4)取D中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡。
①用化学方程式表示溶液变浑浊的原因:_______ 。
②最终所得溶液中溶质的组成为______________________________ (写出所有可能)。
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性。

选用下列药品继续实验:铁、氧化钙、氧化铁、稀盐酸、饱和石灰水、碳酸钠溶液请依据实验回答问题:
(1)B 中溶液是
(2)取A 中溶液于试管中,加入甲,溶液由无色变为黄色,则甲是
(3)取C中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为
(4)取D中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡。
①用化学方程式表示溶液变浑浊的原因:
②最终所得溶液中溶质的组成为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】D、E、I都属于氧化物, A是人体胃液的主要成分之一,C为浅绿色溶液,E常用作温室肥料,G是空气中的主要成分之一,J是常见金属,M是一种常见的碱。它们的转化关系如下图,部分物质略去。
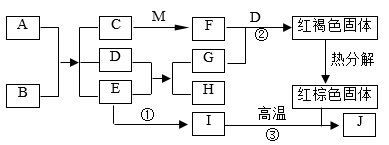
(1)写出C的化学式:_____ ; H属于_____ (填“无机物”或“有机物”)。
(2)写出③有关反应的化学方程式:_____ 。
(3)反应①的过程中_____ (选填“放热”或“吸热”)。
(4)图中转化_____ (选填“是”或“否”)涉及到化学反应基本反应类型中的所有类型。

(1)写出C的化学式:
(2)写出③有关反应的化学方程式:
(3)反应①的过程中
(4)图中转化
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
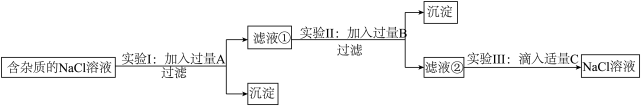
回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是_________ 。
(2)实验Ⅱ中加入的试剂B是_________ 溶液;加入过量B的目的是__________ 。
(3)滤液②中除Na+和Cl-外,还含有的离子是__________ (填离子符号)。
(4)实验Ⅲ中发生的中和反应的化学方程式__________ 。
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为_________ 。

回答下列问题:
(1)实验Ⅰ中加入试剂A除去的杂质是
(2)实验Ⅱ中加入的试剂B是
(3)滤液②中除Na+和Cl-外,还含有的离子是
(4)实验Ⅲ中发生的中和反应的化学方程式
(5)由所得NaCl溶液制成氯化钠晶体,所需操作为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图所示:
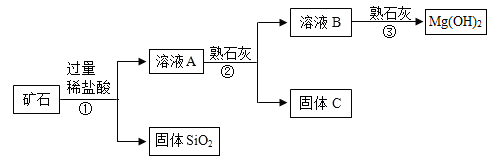
回答下列问题:
(1)步骤①和步骤②均用到的操作是_________________ ,该操作中用到的玻璃棒的作用是 _______ 。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和_________ (填离子符号)。步骤①中发生反应的化学方程式是(只要求写出一个)_______________ 。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
步骤②加入熟石灰,调节溶液的pH范围为_______________ ,固体C中所含成分的化学式为 ___________ 。
(4)步骤③中制得Mg(OH)2的化学方程式为_____ 。在医药上,氢氧化镁可用来____ 。

回答下列问题:
(1)步骤①和步骤②均用到的操作是
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
| 对应离子 | Fe3+ | Cu2+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 4.2 | 9.1 |
| 完全沉淀时的pH | 3.2 | 6.7 | 11.1 |
(4)步骤③中制得Mg(OH)2的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
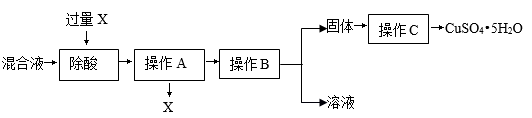
【推荐2】为了除去铜粉中混有的铁粉,并用提纯的铜粉制取胆矾(CuSO4•5H2O),某课外活动小组的同学按如下流程进行实验(反应中部分生成物已略去)。
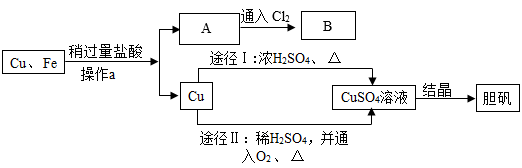
已知: 回答下列有关问题:
回答下列有关问题:
(1)操作a的名称是___________ 。
(2)A溶液的溶质为________ ;A到B的反应中,发生了化合反应,溶液最终变为黄色,则反应的方程式为_________ 。
(3)由Cu制CuSO4溶液的途径Ⅱ中,反应的方程式为_________ (产物为硫酸铜和一种液体);途径Ⅱ与途径Ⅰ相比较,其显著的优点是___________ 。

已知:
 回答下列有关问题:
回答下列有关问题:(1)操作a的名称是
(2)A溶液的溶质为
(3)由Cu制CuSO4溶液的途径Ⅱ中,反应的方程式为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】要从BaCl2和NaOH混合固体中获得纯净的BaCl2,设计方案如下:
(1)方案一:将混合物溶于足量的水,过滤蒸干。该方案不合理,原因是__________________________________________ 。
(2)方案二:将混合物溶于足量的水,再加入适量的CuCl2溶液,充分反应后,过滤蒸干。该方案不合理,原因是______________________________________________________ 。
(3)合理的方案是将混合物溶于足量的水,先用适量试剂①把BaCl2转化为含钡不溶物,过滤,再用足量试剂②将不溶物转化为BaCl2溶液,蒸干。所用试剂①和试剂②依次是__________________________ 。
(1)方案一:将混合物溶于足量的水,过滤蒸干。该方案不合理,原因是
(2)方案二:将混合物溶于足量的水,再加入适量的CuCl2溶液,充分反应后,过滤蒸干。该方案不合理,原因是
(3)合理的方案是将混合物溶于足量的水,先用适量试剂①把BaCl2转化为含钡不溶物,过滤,再用足量试剂②将不溶物转化为BaCl2溶液,蒸干。所用试剂①和试剂②依次是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸镁,为了除去杂质并制得纯净的精盐,小丽设计方案如下:回答下列问题:___________ 。
(2)步骤②中发生反应的化学方程式为___________ 。
(3)步骤③发生反应的化学方程式为___________ 。
(4)向步骤④过滤后所得固体中加入过量的酸,现象是___________ 。
(5)步骤⑤中加入适量的___________ ,该试剂的作用是___________ 。

(2)步骤②中发生反应的化学方程式为
(3)步骤③发生反应的化学方程式为
(4)向步骤④过滤后所得固体中加入过量的酸,现象是
(5)步骤⑤中加入适量的
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等(SiO2几乎不溶于水和常见的酸)。
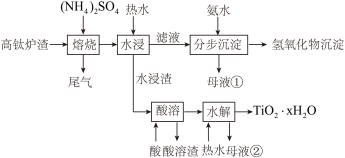
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
回答下列问题:
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是______ ,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为NH4Al(SO4)2的化学方程式为: 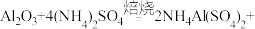
______ 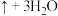 。
。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是________ (按先后顺序填写)。
(3)实验室进行过滤时玻璃棒的作用________ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是________ 。“酸溶渣”的成分是_______ 、CaSO4。
(5)氢氧化物沉淀中的________ 、_________ 能用来制备治疗胃酸过多的药物,写出一个用氢氧化物治疗胃酸过多的化学方程式________ 。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到_______ ,循环利用;农业上也可以用作___________ 。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
| 金属离子 | Fe3+ | A13+ | Mg2+ | Ca2+ |
| 开始沉淀的pH | 2.2 | 3.5 | 9.5 | 12.4 |
| 沉淀完全的pH | 3.2 | 4.7 | 11.1 | 13.8 |
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是
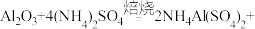
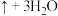 。
。(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是
(3)实验室进行过滤时玻璃棒的作用
(4)“水浸渣”在160℃“酸溶”最适合的酸是
(5)氢氧化物沉淀中的
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到
您最近一年使用:0次