要从BaCl2和NaOH混合固体中获得纯净的BaCl2,设计方案如下:
(1)方案一:将混合物溶于足量的水,过滤蒸干。该方案不合理,原因是__________________________________________ 。
(2)方案二:将混合物溶于足量的水,再加入适量的CuCl2溶液,充分反应后,过滤蒸干。该方案不合理,原因是______________________________________________________ 。
(3)合理的方案是将混合物溶于足量的水,先用适量试剂①把BaCl2转化为含钡不溶物,过滤,再用足量试剂②将不溶物转化为BaCl2溶液,蒸干。所用试剂①和试剂②依次是__________________________ 。
(1)方案一:将混合物溶于足量的水,过滤蒸干。该方案不合理,原因是
(2)方案二:将混合物溶于足量的水,再加入适量的CuCl2溶液,充分反应后,过滤蒸干。该方案不合理,原因是
(3)合理的方案是将混合物溶于足量的水,先用适量试剂①把BaCl2转化为含钡不溶物,过滤,再用足量试剂②将不溶物转化为BaCl2溶液,蒸干。所用试剂①和试剂②依次是
更新时间:2017-09-26 11:04:04
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
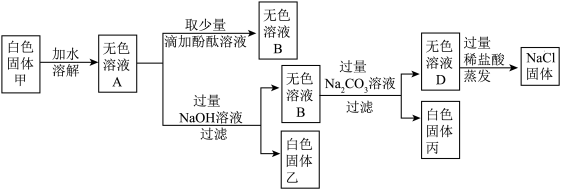
【推荐1】某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:_____ 。
(2)向无色溶液D中加入过量稀盐酸的步骤中发生反应的化学方程式为_____ ; _____ 。
(3)在蒸发的操作中,当蒸发皿内出现有_____ 时,应停止加热。
(4)分析上述实验可知,白色固体甲中 一定没有的物质是_____ 。
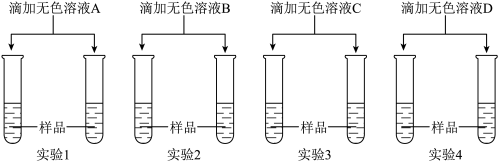
(5)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按下图所示操作进行实验,就能达到鉴别目的是实验_____ (填实验编号)。
(2)向无色溶液D中加入过量稀盐酸的步骤中发生反应的化学方程式为
(3)在蒸发的操作中,当蒸发皿内出现有
(4)分析上述实验可知,白色固体甲中 一定没有的物质是
(5)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按下图所示操作进行实验,就能达到鉴别目的是实验
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl﹣、 、
、 的相互分离。相应的实验过程可用下列流程图表示:
的相互分离。相应的实验过程可用下列流程图表示:
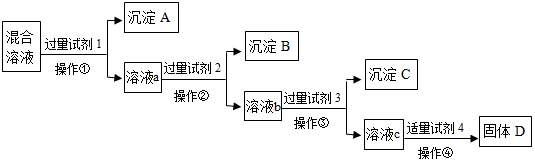
(1)写出上述实验过程中所用试剂、沉淀的化学式:试剂1:___________ 沉淀C:___________
(2)写出溶液a中所含有的阳离子___________ ;
(3)恰当地控制试剂4的加入量的方法是___________ 。
 、
、 的相互分离。相应的实验过程可用下列流程图表示:
的相互分离。相应的实验过程可用下列流程图表示:
(1)写出上述实验过程中所用试剂、沉淀的化学式:试剂1:
(2)写出溶液a中所含有的阳离子
(3)恰当地控制试剂4的加入量的方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】一包白色固体粉末,可能含有 CaO、Ca(OH)2 中的一种或二种。为确定其成分,取样品进行如下实验。

①悬浊液中除水外,含有的物质化学式是__ ,该悬浊液称呼为 __ 。
②若取出少量悬浊液置于试管中,滴加酚酞,再继续逐滴滴入盐酸至过量,边滴边振荡。实验过程试管中产生的现象依次为__ (请选择并依次填写下列序号)
a.红色,浑浊 b.无色,澄清 c.红色,澄清 d.白色,浑浊
③上述实验②后,为判断溶液中盐酸是否过量,可选用的试剂是__ (选填编号)。
a.镁粉 b.氯化钙溶液 c.氢氧化钠溶液 d.硝酸银溶液
④分别称取样品于固体的质量进行比较,若固体质量大于样品质量,则样品的成分可能是__ 。

①悬浊液中除水外,含有的物质化学式是
②若取出少量悬浊液置于试管中,滴加酚酞,再继续逐滴滴入盐酸至过量,边滴边振荡。实验过程试管中产生的现象依次为
a.红色,浑浊 b.无色,澄清 c.红色,澄清 d.白色,浑浊
③上述实验②后,为判断溶液中盐酸是否过量,可选用的试剂是
a.镁粉 b.氯化钙溶液 c.氢氧化钠溶液 d.硝酸银溶液
④分别称取样品于固体的质量进行比较,若固体质量大于样品质量,则样品的成分可能是
您最近一年使用:0次
【推荐1】为除去粗盐溶液中的CaCl2、Na2SO4两种可溶性杂质,并最终获得纯净的氯化钠晶体。化学实验小组成员设计的实验操作有:①加过量Na2CO3溶液;②加适量盐酸;③加过量Ba(OH)2溶液;④蒸发结晶;⑤过滤。
(1)请你将正确的步骤排序写出来(写序号,步骤不重复)。
(2)请你写出加过量Ba(OH)2溶液,发生反应的化学方程式。
(1)请你将正确的步骤排序写出来(写序号,步骤不重复)。
(2)请你写出加过量Ba(OH)2溶液,发生反应的化学方程式。
您最近一年使用:0次
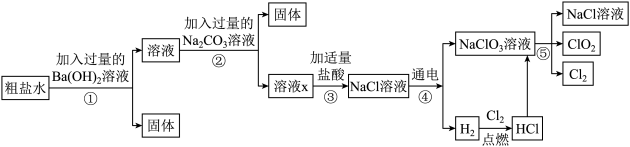
【推荐2】二氧化氯(C1O2)是一种高效、光谱、安全的杀菌消毒剂,可应用于自来水和公共场所的杀菌消毒处理。化工生产中通常以粗盐水(只含可溶性杂质MgSO4、CaCl2)为原料,通过五个步骤制取ClO2,工艺流程如下图:______ ,步骤①中不能用Ba(NO3)2代替Ba(OH)2,原因是:______ ;
(2)步骤②得到的固体除了CaCO3之外,还有______ (填名称),溶液X中的溶质有______ (填化学式);
(3)步骤④发生反应的化学方程式为______ 。
(2)步骤②得到的固体除了CaCO3之外,还有
(3)步骤④发生反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等(SiO2几乎不溶于水和常见的酸)。
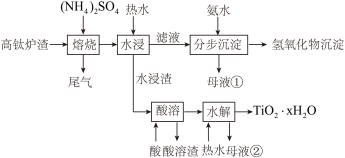
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
回答下列问题:
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是______ ,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为NH4Al(SO4)2的化学方程式为: 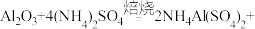
______ 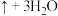 。
。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是________ (按先后顺序填写)。
(3)实验室进行过滤时玻璃棒的作用________ 。
(4)“水浸渣”在160℃“酸溶”最适合的酸是________ 。“酸溶渣”的成分是_______ 、CaSO4。
(5)氢氧化物沉淀中的________ 、_________ 能用来制备治疗胃酸过多的药物,写出一个用氢氧化物治疗胃酸过多的化学方程式________ 。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到_______ ,循环利用;农业上也可以用作___________ 。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
| 金属离子 | Fe3+ | A13+ | Mg2+ | Ca2+ |
| 开始沉淀的pH | 2.2 | 3.5 | 9.5 | 12.4 |
| 沉淀完全的pH | 3.2 | 4.7 | 11.1 | 13.8 |
(1)“焙烧时,将炼铁高钛炉渣粉碎的主要目的是
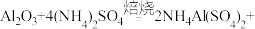
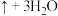 。
。(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,依次析出的金属离子是
(3)实验室进行过滤时玻璃棒的作用
(4)“水浸渣”在160℃“酸溶”最适合的酸是
(5)氢氧化物沉淀中的
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得到
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】KMnO4和MnO2都是实验室常见药品,某小组同学对这两种物质做了如下探究。
Ⅰ.从MnO2粗品(含有较多的MnO、MnCO3和Fe2O3)中获得MnO2,其工艺流程如下图。
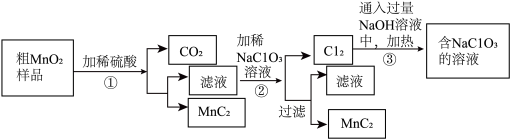
请回答下列问题:
(1)第①步操作中,加快酸溶速率的措施有__________ 。
(2)第①步中,样品中的MnO和MnCO3分别和硫酸反应生成可溶性的MnSO4,则MnCO3和硫酸反应的化学方程式为___________ 。
(3)第②步操作中,NaClO3将Mn2+转化为MnO2,利用电解法可实现这步转化。则生成MnO2的化学方程式为_________ 。
(4)第③步操作中,Cl2与热的NaOH溶液发生歧化反应(歧化反应是指反应中某个元素的化合价既有上升又有下降),则生成NaClO3的反应化学方程式为_______ 。
(5)为得到纯净的MnO2,需将过滤后的MnO2合并后进行洗涤。设计检验MnO2是否洗涤干净的实验方案是_________ 。
Ⅱ.探究酸性KMnO4和Na2C2O4的反应
(6)将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),反应的化学方程式为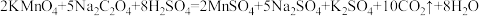 ,现象如下表。请分析KMnO4溶液褪色时间变化的最可能原因
,现象如下表。请分析KMnO4溶液褪色时间变化的最可能原因_______ 。
Ⅰ.从MnO2粗品(含有较多的MnO、MnCO3和Fe2O3)中获得MnO2,其工艺流程如下图。

请回答下列问题:
(1)第①步操作中,加快酸溶速率的措施有
(2)第①步中,样品中的MnO和MnCO3分别和硫酸反应生成可溶性的MnSO4,则MnCO3和硫酸反应的化学方程式为
(3)第②步操作中,NaClO3将Mn2+转化为MnO2,利用电解法可实现这步转化。则生成MnO2的化学方程式为
(4)第③步操作中,Cl2与热的NaOH溶液发生歧化反应(歧化反应是指反应中某个元素的化合价既有上升又有下降),则生成NaClO3的反应化学方程式为
(5)为得到纯净的MnO2,需将过滤后的MnO2合并后进行洗涤。设计检验MnO2是否洗涤干净的实验方案是
Ⅱ.探究酸性KMnO4和Na2C2O4的反应
(6)将酸性KMnO4溶液逐滴滴入一定体积的Na2C2O4溶液中(温度相同,并不断振荡),反应的化学方程式为
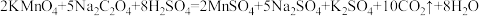 ,现象如下表。请分析KMnO4溶液褪色时间变化的最可能原因
,现象如下表。请分析KMnO4溶液褪色时间变化的最可能原因 | 滴加KMnO4溶液的量 | KMnO4溶液紫色褪去所需的时间 |
| 滴入第1滴 | 60s | |
| 滴入第2滴 | 15s | |
| 滴入第3滴 | 3s | |
| 滴入第4滴 | 1s |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuC12的流程图如下:
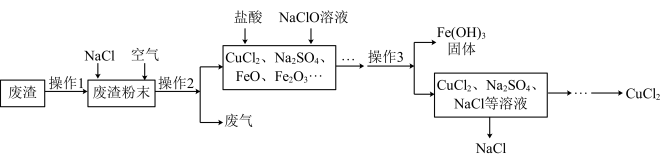
(1)操作1把废渣粉碎的目的是____________ 。
(2)在废渣粉末中加入NaCl和O2的目的是:CuS、NaCl和O2在高温条件下反应生成CuC12和Na2SO4,写出该反应的化学方程式____________ 。
(3)【查阅资料】:不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液PH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。
下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
为了使溶液中的Fe3+变成Fe(OH)3沉淀而除去,你认为调节溶液的pH到________ (填数值范围)比较合适。
(4)流程图中能循环利用的物质是____________ 和水。

(1)操作1把废渣粉碎的目的是
(2)在废渣粉末中加入NaCl和O2的目的是:CuS、NaCl和O2在高温条件下反应生成CuC12和Na2SO4,写出该反应的化学方程式
(3)【查阅资料】:不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液PH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。
下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
(4)流程图中能循环利用的物质是
您最近一年使用:0次



