铜镁合金经常作为导电材料被使用。某化学兴趣小组称取10g铜镁合金,把100g稀硫酸分4次加入样品中,充分反应后,测的剩余固体的质量记录如下:
(1)铜镁合金中铜的质量分数___________ 。
(2)求所加入的稀硫酸的溶质质量分数___________ 。
| 序号 | 加入稀硫酸的质量/g | 剩余固体的质量/g |
| 1 | 25 | 8.8 |
| 2 | 25 | 7.6 |
| 3 | 25 | 6.6 |
| 4 | 25 | 6.6 |
(2)求所加入的稀硫酸的溶质质量分数
更新时间:2022-04-10 17:42:25
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】过氧化钠(Na2O2)是一种重要的氧化剂,它与水反应产生氧气的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.现将一定量的Na2O2加入盛有87.6g水的烧杯中,完全反应后,称得溶液的质量比反应前过氧化钠和水的总质量减少了3.2g(假定水蒸气的挥发忽略不计).请回答:
(1)反应生成氧气的质量为_________ g.
(2)假定上述Na2O2中含氧的质量为m1,反应生成的NaOH中含氧的质量为m2,则m1______________ m2(填“=”“>”或“<”).
(3)计算反应后所得溶液中溶质的质量分数为___________ .(写出详细的计算过程)
(1)反应生成氧气的质量为
(2)假定上述Na2O2中含氧的质量为m1,反应生成的NaOH中含氧的质量为m2,则m1
(3)计算反应后所得溶液中溶质的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】某同学用一定溶质质量分数的稀硫酸做“氧化铜+硫酸→硫酸铜+水”的实验,其五次实验结果如下表所示:
根据实验结果填写下列空格:
(1)哪几次反应氧化铜有剩余?
(2)哪几次反应硫酸有剩余?
(3)表中x的值是_____ 。
(4)硫酸溶液中溶质的质量分数为_____ 。
| 实验次数 | 氧化铜/g | 硫酸溶液/g | 硫酸铜/g |
| 1 | 2.0 | 120 | 4.0 |
| 2 | 4.0 | 120 | 8.0 |
| 3 | 6.0 | 120 | 9.6 |
| 4 | 8.0 | 200 | 16 |
| 5 | 10.0 | 200 | x |
(1)哪几次反应氧化铜有剩余?
(2)哪几次反应硫酸有剩余?
(3)表中x的值是
(4)硫酸溶液中溶质的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】已知金属钠和水能发生下列反应:2Na+2H2O=2NaOH+H2↑。现取金属钠9.2g投入到100g水中,充分反应后,冷却到室温(20℃),得到一种不饱和溶液,向所得溶液中逐滴滴入MgSO4溶液,实验测得溶液的总质量与滴入MgSO4溶液的质量关系曲线如图所示。

根据题意回答下列问题
(1)金属钠和水充分反应后,生成氢气的质量为________g。
(2)图中A点的纵坐标表示的溶液的质量是________g。
(3)通过计算求出当滴入120gMgSO4溶液时,所得溶液中溶质的质量分数是多少_____?(计算结果精确至1%)

根据题意回答下列问题
(1)金属钠和水充分反应后,生成氢气的质量为________g。
(2)图中A点的纵坐标表示的溶液的质量是________g。
(3)通过计算求出当滴入120gMgSO4溶液时,所得溶液中溶质的质量分数是多少_____?(计算结果精确至1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】为测定某铜锌合金中锌的含量,取50g样品进行实验,将l00g稀盐酸分五次加入该样品中(杂质不溶于水也不参与反应,反应原理为:Zn+2HCl=ZnCl2+H2↑),充分反应后测得生成气体的总质量如表所示:
试求:
(1)m的数值为_____。
(2)该铜锌合金中锌的质量分数是多少?______________(写出计算过程)
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的总质量/g | 0.05 | 0.10 | m | 0.20 | 0.20 |
试求:
(1)m的数值为_____。
(2)该铜锌合金中锌的质量分数是多少?______________(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】小李要测定某Cu-Zn合金中铜的质量分数,做了如下实验。
(1)量筒量取_____ mL 98%浓硫酸(密度为1.84g/mL)配成100g 19.6%的稀硫酸。
(2)将上述配成的稀硫酸全部加入盛有10g合金样品的烧杯中,反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示。
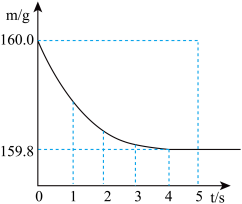
①产生氢气质量为_____ g。
②该合金样品中铜的质量分数为_____ 。
③反应后所得溶液中硫酸锌的质量分数。_____ (写出解答过程,精确到0.1%)
(1)量筒量取
(2)将上述配成的稀硫酸全部加入盛有10g合金样品的烧杯中,反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示。

①产生氢气质量为
②该合金样品中铜的质量分数为
③反应后所得溶液中硫酸锌的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为了测定黄铜(铜锌合金)样品中铜的溶质质量分数,实验过程和有关数据如下图。

进行计算:
(1)黄铜样品中铜的质量分数是多少?
(2)恰好完全反应时所得溶液中溶质质量分数是多少?

进行计算:
(1)黄铜样品中铜的质量分数是多少?
(2)恰好完全反应时所得溶液中溶质质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】往100g硝酸亚铁和硝酸银的混合液中,加入过量的锌粉,根据实验事实绘制了如图所示曲线,a点对应锌质量为0.65,b点对应锌质量为1.625,分析并计算:

(1)a→b段表示锌与混合物中的___________ 发生反应。(写化学式)
(2)求反应前混合液中硝酸亚铁的质量分数___________ (写出计算过程)。
(3)请画出固体中铁元素的质量随时间变化的曲线(不需要标出具体坐标点)。
(4)在上述100g混合液中改加铜粉,是否能测量硝酸亚铁的质量分数?___________ (填“能”或“不能”,理由是___________ 。

(1)a→b段表示锌与混合物中的
(2)求反应前混合液中硝酸亚铁的质量分数
(3)请画出固体中铁元素的质量随时间变化的曲线(不需要标出具体坐标点)。
(4)在上述100g混合液中改加铜粉,是否能测量硝酸亚铁的质量分数?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】为测定某盐酸的溶质质量分数,取100g样品于烧杯中,将50g碳酸钠溶液分为5等份,分5次加入盛有样品的烧杯中,测出每次反应后溶液的总质量,实验数据如下表:
(1)生成二氧化碳气体的总质量为______ g;
(2)第_______ 次实验所加Na2CO3溶液与100g盐酸恰好完全反应;
(3)所用盐酸的溶质质量分数为________ 。
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入Na2CO3溶液的质量(g) | 10 | 10 | 10 | 10 | 10 |
| 反应后溶液的质量(g) | 108.9 | 117.8 | 126.7 | 135.6 | 145.6 |
(1)生成二氧化碳气体的总质量为
(2)第
(3)所用盐酸的溶质质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】某化学学习小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
步骤1:取1片胃药研碎放入锥形瓶中,加水完全溶解得到100g溶液;
步骤2:配制100g0.365%的稀盐酸作为模拟胃酸;
步骤3:取步骤1中的溶液20g于锥形瓶中,向锥形瓶内逐滴滴加上述稀盐酸并用传感器测定溶液的pH,当pH等于7时恰好反应,消耗稀盐酸10g(胃药中其它成分不参加反应)。
请回答下列问题:
(1)NaHCO3中碳、氧元素的质量比为_____(写最简整数比)。
(2)用18.25%的浓盐酸配制100g0.365%的稀盐酸需加水_____mL
(3)请根据实验数据计算每片胃药中NaHCO3的质量,写出必要的计算过程。_____
步骤1:取1片胃药研碎放入锥形瓶中,加水完全溶解得到100g溶液;
步骤2:配制100g0.365%的稀盐酸作为模拟胃酸;
步骤3:取步骤1中的溶液20g于锥形瓶中,向锥形瓶内逐滴滴加上述稀盐酸并用传感器测定溶液的pH,当pH等于7时恰好反应,消耗稀盐酸10g(胃药中其它成分不参加反应)。
请回答下列问题:
(1)NaHCO3中碳、氧元素的质量比为_____(写最简整数比)。
(2)用18.25%的浓盐酸配制100g0.365%的稀盐酸需加水_____mL
(3)请根据实验数据计算每片胃药中NaHCO3的质量,写出必要的计算过程。_____
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】某学生在课外活动中用铁粉(含杂质且杂质不参加反应)和稀硫酸反应制取氢气。所做5次实验结果记录如下表(每次实验产生的氢气全部被收集,且体积在相同条件下测定。该条件下氢气的密度是0.089g/L)
根据上述实验结果进行分析、计算,并回答下列问题:
(1)上述实验中,铁粉一定过量的实验编号是_____ ;
(2)计算铁粉的纯度(要求写出计算过程,计算结果精确到0.1,下同);
(3)计算稀硫酸的质量分数。
实验编号 | 铁粉的质量/g | 稀硫酸的质量/g | 生成氢气的体积/L |
1 | 2.0 | 50.0 | 0.77 |
2 | 4.0 | 50.0 | 1.54 |
3 | 5.8 | 50.0 | 2.24 |
4 | 5.8 | 60.0 | 2.24 |
5 | 6.4 | 50.0 | 2.24 |
(1)上述实验中,铁粉一定过量的实验编号是
(2)计算铁粉的纯度(要求写出计算过程,计算结果精确到0.1,下同);
(3)计算稀硫酸的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】已知金属钠加入硫酸铜溶液中会发生如下反应:2Na+2H2O=2NaOH+H2↑,2NaOH+CuSO4= Cu(OH)2↓+ Na2SO4。现将2.3g 金属钠投入一定量的硫酸铜溶液中,充分反应后所得溶液中只含一种溶质,其质量分数为7.1%。求:
(1)CuSO4中铜元素和氧元素的质量比为______ 。(化成最简整数比)
(2)生成氢气的质量为______ g。
(3)原硫酸铜溶液中溶质的质量分数。(请写出计算过程结果保留到0.I%)
(1)CuSO4中铜元素和氧元素的质量比为
(2)生成氢气的质量为
(3)原硫酸铜溶液中溶质的质量分数。(请写出计算过程结果保留到0.I%)
您最近一年使用:0次



