小莉同学进行如图实验,充分反应后,将试管①②内的物质倒入同一烧杯中混合。等充分反应后再过滤,结果得到滤渣A和无色滤液B。
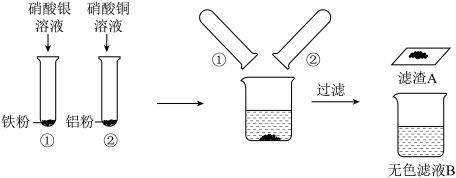
(1)试管①中反应的化学方程式为________ ;试管②中观察到的现象是:________ 。
(2)无色滤液B中含有的溶质是________ (填化学式)。
(3)设计实验探究滤渣A的成分
【提出问题】滤渣A的成分是什么?
【查阅资料】银、铜、铁、铝四种金属中,只有铝能跟氢氧化钠溶液反应,该反应的化学方程式为: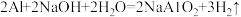 。
。
【作出猜想】滤渣A的成分为:
猜想Ⅰ:银、铜;猜想Ⅱ:银、铜、铁;猜想Ⅲ:_________ 。
【分析思考】猜想Ⅰ一定不正确,原因是___________ 。
【进行实验】结合猜想Ⅱ和Ⅲ,只要证明物质________ 是否存在即可。
【作出判断】如果__________ ,则猜想Ⅱ成立。如果_________ ,则猜想Ⅲ成立。

(1)试管①中反应的化学方程式为
(2)无色滤液B中含有的溶质是
(3)设计实验探究滤渣A的成分
【提出问题】滤渣A的成分是什么?
【查阅资料】银、铜、铁、铝四种金属中,只有铝能跟氢氧化钠溶液反应,该反应的化学方程式为:
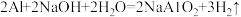 。
。【作出猜想】滤渣A的成分为:
猜想Ⅰ:银、铜;猜想Ⅱ:银、铜、铁;猜想Ⅲ:
【分析思考】猜想Ⅰ一定不正确,原因是
【进行实验】结合猜想Ⅱ和Ⅲ,只要证明物质
| 实验步骤 | 实验现象 |
| 取滤渣样品放入小烧杯中,加入足量 |
2022·广东·一模 查看更多[5]
(已下线)金榜卷01-2023年中考化学考前一模名师押题金榜卷(广东专用)(已下线)2023年中考风向标-广东-科学探究题2022年贵州省安顺市平坝区乐平中学中考模拟化学试题82022年广东省百校联考中考模拟(一模)化学试题 2022年广东省初中学业水平考试一模化学试题
更新时间:2022/04/24 20:50:53
|
相似题推荐
综合应用题
|
较难
(0.4)
【推荐1】人类文明与社会进步同金属材料关系密切。
(一)铁的广泛应用
(1)人体缺铁会造成贫血,这里的铁是指_____ 。 (选填序号)
A.单质 B.元素 C.原子
(2)双吸剂的主要成分是铁粉,其原理是铁锈蚀,在过程中吸收______ 和 _______ 。
(3)暖宝宝的主要成分是铁粉、氯化钠等,原理也是铁锈蚀,锈蚀过程中发生______ 。
A.剧烈氧化 B.缓慢氧化
(4)西汉时期有“曾青得铁则化为铜”之说,用化学方程式表示其原理________ 。
(二)铁的锈蚀
(1)下列情况下铁制品最易生锈的是_____ (填序号)。
a.潮湿空气中 b.部分浸入食盐水中 c.干燥空气中
(2)铁生锈的主要过程为:写出转化①的化学方程式_______ 。




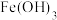


(3)铁锈中一定含Fe2O3•nH2O,可能含FeCO3 (FeCO3和稀盐酸的反应与CaCO3相似),在某铁锈样品中加稀盐酸,_______ (填现象),证明不含FeCO3。
(三)铁的冶炼
取24.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
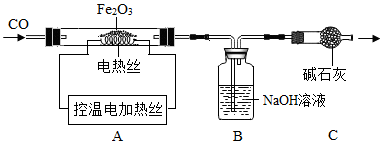
资料:NaOH溶液能很好地吸收CO2,碱石灰可吸收H2O和CO2。
(1)连接装置,先______ ,再装入药品。
(2)实验时先通入CO,目的是_________ ,反应后还要继续通CO目的是______ 。
(3)控制A中温度在700℃至固体全部 变黑,继续通CO至冷却。
①通过测定装置B的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是_______ 。
②现直接测得装置A中剩余固体质量为19.2g。则装置B应增重_______ g。
(4)请指出上述实验装置的一个明显缺陷_______ 。
(一)铁的广泛应用
(1)人体缺铁会造成贫血,这里的铁是指
A.单质 B.元素 C.原子
(2)双吸剂的主要成分是铁粉,其原理是铁锈蚀,在过程中吸收
(3)暖宝宝的主要成分是铁粉、氯化钠等,原理也是铁锈蚀,锈蚀过程中发生
A.剧烈氧化 B.缓慢氧化
(4)西汉时期有“曾青得铁则化为铜”之说,用化学方程式表示其原理
(二)铁的锈蚀
(1)下列情况下铁制品最易生锈的是
a.潮湿空气中 b.部分浸入食盐水中 c.干燥空气中
(2)铁生锈的主要过程为:写出转化①的化学方程式




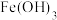


(3)铁锈中一定含Fe2O3•nH2O,可能含FeCO3 (FeCO3和稀盐酸的反应与CaCO3相似),在某铁锈样品中加稀盐酸,
(三)铁的冶炼
取24.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。

资料:NaOH溶液能很好地吸收CO2,碱石灰可吸收H2O和CO2。
(1)连接装置,先
(2)实验时先通入CO,目的是
(3)控制A中温度在700℃至固体
①通过测定装置B的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是
②现直接测得装置A中剩余固体质量为19.2g。则装置B应增重
(4)请指出上述实验装置的一个明显缺陷
您最近半年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】人类的生活、生产离不开金属材料。大自然向人类提供了丰富的金属矿物资源,人类每年提取较大的金属依次是铁、铝、铜。
(1)在金属活动性顺序中铁没有铝活泼,但铝具有很好抗腐蚀性原因是_______ 。
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的_______ 共同作用的结果。
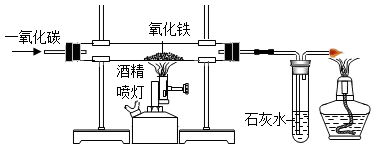
(3)下图是实验室模拟工业炼铁的装置图。该装置中一共发生的化学反应有_______ 个,酒精灯的作用是_______ ,炼铁的原理_______ (写化学方程式)。
(4)将锌粉放入含有Mg(NO3)2、Cu(NO3)2、AgNO3三种溶质的混合溶液中,充分反应后过滤。以下是对固体或滤液成分的探究。
①若向反应后所得固体上滴加盐酸有气泡产生,则该固体含有的金属有哪些?____
②猜想:滤液中的溶质为Mg(NO3)2、Zn(NO3)2、AgNO3,请分析猜想不合理原因是什么?____
(5)黄铜是铜锌合金,为测定某黄铜(铜锌合金)样品中铜的含量,取10g样品放在烧杯中,然后向其中逐渐加入稀硫酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀硫酸的质量为14g,反应后烧杯中物质总质量为23.8g。请计算样品中铜的质量分数。
(1)在金属活动性顺序中铁没有铝活泼,但铝具有很好抗腐蚀性原因是
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的
(3)下图是实验室模拟工业炼铁的装置图。该装置中一共发生的化学反应有

(4)将锌粉放入含有Mg(NO3)2、Cu(NO3)2、AgNO3三种溶质的混合溶液中,充分反应后过滤。以下是对固体或滤液成分的探究。
①若向反应后所得固体上滴加盐酸有气泡产生,则该固体含有的金属有哪些?
②猜想:滤液中的溶质为Mg(NO3)2、Zn(NO3)2、AgNO3,请分析猜想不合理原因是什么?
(5)黄铜是铜锌合金,为测定某黄铜(铜锌合金)样品中铜的含量,取10g样品放在烧杯中,然后向其中逐渐加入稀硫酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀硫酸的质量为14g,反应后烧杯中物质总质量为23.8g。请计算样品中铜的质量分数。
您最近半年使用:0次
综合应用题
|
较难
(0.4)
名校
【推荐3】金属是一种重要的资源。
(1)为减少污染并变废为宝,某化学小组实验探究工业度水的综合利用,设计了以下流程图并完成了回收金属锌和硫酸锌的实验,

①固体X的成分是________ ;操作Ⅰ需用的玻璃仪器有烧杯、玻璃棒和_______ 。
②上述流程中,在加入适量B时反应的化学方程式为_________ 。
③操作Ⅱ中玻璃棒的作用是________ 。
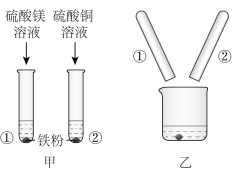
(2)某同学为探究Mg、Fe、Cu三种金属的有关性质,进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤,滤液中含有的金属离子的可能组合有 (填字母)。
(1)为减少污染并变废为宝,某化学小组实验探究工业度水的综合利用,设计了以下流程图并完成了回收金属锌和硫酸锌的实验,

①固体X的成分是
②上述流程中,在加入适量B时反应的化学方程式为
③操作Ⅱ中玻璃棒的作用是
(2)某同学为探究Mg、Fe、Cu三种金属的有关性质,进行了如图甲所示的实验,实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤,滤液中含有的金属离子的可能组合有 (填字母)。

| A.Mg2+ |
| B.Mg2+和Fe2+ |
| C.Mg2+和Fe3+ |
| D.Mg2+和Cu2+ |
| E.Mg2+、Fe2+和Cu2+ |
您最近半年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐1】化学兴趣小组在实验室进行如图1所示的探究实验:

(1)上述三个实验中有气泡产生的反应的化学方程式为________ 。
(2)另取少量实验3反应后的溶液,滴加无色酚酞溶液后溶液仍为无色,说明反应后的溶液一定不呈_________ 性。
(3)小组同学对反应后三支试管中物质进行以下操作,请填写下表中的空格:
(4)同学们继续对滤液B中的成分进行探究。
【提出问题】滤液B中含有哪些离子?
【猜想与假设】猜想一:Na+、C1-、K+
猜想二:Na+、C1-、K+、
猜想三:Na+、C1-、K+、
猜想四:Na+、C1-、K+、Ba2+
猜想五:_________ (写出一种合理的猜想)
【实验与探究】
①小刚为验证猪想一进行以下实验:取少量滤液B于试管中并加入足量的氯化钡溶液,无明显现象,由此得出猜想一正确的结论。但小亮不同意这一结论,理由是_________ 。
②小明通过以下方法进一步证明滤液B中离子成分:取少量滤液B于试管中,向其中加入硫酸钠溶液,通过仪器测定并绘制如图2所示的溶液中离子数目的变化趋势图。
【实验结论】滤液B的成分是________ (填离子符号)。
【归纳与总结】通过以上实验我们能够总结出,在研究反应后溶液中离子成分时,不需要对所有的离子进行探究,只要对_________ 的离子进行探究,就能得出正确的结论。

(1)上述三个实验中有气泡产生的反应的化学方程式为
(2)另取少量实验3反应后的溶液,滴加无色酚酞溶液后溶液仍为无色,说明反应后的溶液一定不呈
(3)小组同学对反应后三支试管中物质进行以下操作,请填写下表中的空格:
| 步骤 | 现象 | 分析与结论 |
| ①将有沉淀产生的试管中的混合物过滤,再将滤液与另两支试管中的溶液混合,使其充分反应 | 产生气泡,并生成白色沉淀 | / |
| ②将步骤①中最终得到的混合物过滤,得到滤渣A和滤液B。向滤渣A中加入足量稀硝酸 | 产生气泡,固体部分消失 | 滤渣A的成分为 |
(4)同学们继续对滤液B中的成分进行探究。
【提出问题】滤液B中含有哪些离子?
【猜想与假设】猜想一:Na+、C1-、K+
猜想二:Na+、C1-、K+、

猜想三:Na+、C1-、K+、

猜想四:Na+、C1-、K+、Ba2+
猜想五:
【实验与探究】
①小刚为验证猪想一进行以下实验:取少量滤液B于试管中并加入足量的氯化钡溶液,无明显现象,由此得出猜想一正确的结论。但小亮不同意这一结论,理由是
②小明通过以下方法进一步证明滤液B中离子成分:取少量滤液B于试管中,向其中加入硫酸钠溶液,通过仪器测定并绘制如图2所示的溶液中离子数目的变化趋势图。
【实验结论】滤液B的成分是
【归纳与总结】通过以上实验我们能够总结出,在研究反应后溶液中离子成分时,不需要对所有的离子进行探究,只要对
您最近半年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】2014年3月,习近平总书记来到开封市兰考县焦裕禄精神发祥地考察调研。兰考的部分土地属于盐碱地,在春秋天地面会泛出白色物质,某化学兴趣小组从当地地里采集了样品,对其成分进行探究

查阅资料:
①盐碱地泛出白色物质可能有氯化钠、氯化钙、氯化镁、碳酸钠和硫酸钠等物质.
②氯化银,硫酸钡既不溶于水,也不溶于酸.
(1)氯化钠、氯化钙和氯化镁中都含有氯元素,如图1是氯元素的元素周期表中的相关信息,下列说法不正确的是________ (填标号).
A .该元素属于非金属元素
B .该原子核内质子数为17
C .该元素的原子形成离子后,离子结构示意图为图2
D .该元素的相对原子质量为35.45g
(2)同学们将样品放入适量水中,搅拌后样品完全溶解,得到无色、澄清的溶液.
①甲同学取少量溶液于试管中,先向试管中滴加适量的稀盐酸,发现有气泡产生;再向试管中滴加适量氢氧化钠溶液,观察无明显现象,请推测:该样品中一定含有什么物质___ ?一定不含有什么物质_____ ?
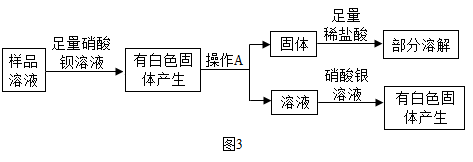
②乙同学为了进一步探究该样品的成分,做了如图3实验:操作A的名称是_____ ;由以上实验分析,该样品中还含有什么物质________ ?
(3)棉花适宜生长的pH为6-8的土壤中.设计实验检验当地是否适合种植棉花,请简述实验操作步骤________ .
(4)丙同学取10g盐碱地泛出的白色物质放入烧杯中,加入20.0g足量稀盐酸,充分反应后,称量得知烧杯内溶液总质量为27.8g,请计算:
①生成二氧化碳的质量________ .
②该白色物质中碳酸钠的质量分数________ .


查阅资料:
①盐碱地泛出白色物质可能有氯化钠、氯化钙、氯化镁、碳酸钠和硫酸钠等物质.
②氯化银,硫酸钡既不溶于水,也不溶于酸.
(1)氯化钠、氯化钙和氯化镁中都含有氯元素,如图1是氯元素的元素周期表中的相关信息,下列说法不正确的是
A .该元素属于非金属元素
B .该原子核内质子数为17
C .该元素的原子形成离子后,离子结构示意图为图2
D .该元素的相对原子质量为35.45g
(2)同学们将样品放入适量水中,搅拌后样品完全溶解,得到无色、澄清的溶液.
①甲同学取少量溶液于试管中,先向试管中滴加适量的稀盐酸,发现有气泡产生;再向试管中滴加适量氢氧化钠溶液,观察无明显现象,请推测:该样品中一定含有什么物质
②乙同学为了进一步探究该样品的成分,做了如图3实验:操作A的名称是
(3)棉花适宜生长的pH为6-8的土壤中.设计实验检验当地是否适合种植棉花,请简述实验操作步骤
(4)丙同学取10g盐碱地泛出的白色物质放入烧杯中,加入20.0g足量稀盐酸,充分反应后,称量得知烧杯内溶液总质量为27.8g,请计算:
①生成二氧化碳的质量
②该白色物质中碳酸钠的质量分数
您最近半年使用:0次
综合应用题
|
较难
(0.4)
名校
【推荐3】草酸亚铁晶体(FeC2O4•2H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成,探究过程如下:
【查阅资料】1、草酸亚铁晶体热分解的气体产物是H2O,CO,CO2
2、白色的无水CuSO4遇水蒸气会变成蓝色
【实验设计】
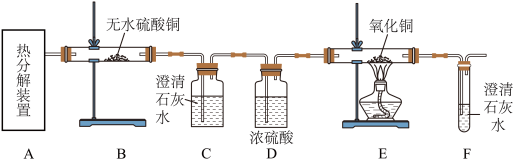
(1)从环保角度考虑,该套实验装置的明显缺陷是______
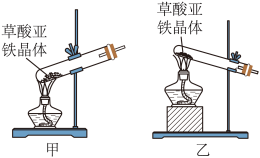
(2)可选择以下实验装置中的______ (选填“甲”或“乙”)作为虚线中的“热分解装置”。
【问题讨论】
(3)D中浓硫酸的作用是______ ,实验过程中观察到B中白色无水CuSO4变成蓝色,C中______ ,E中______ (填实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O,CO,CO2。
(4)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是______
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加盛有______ (填物质的名称或化学式)溶液的洗气瓶。
【数据分析】
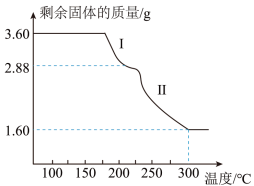
(6)称取3.60g草酸亚铁晶体(FeC2O4•2H2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:
①过程Ⅰ发生反应的化学方程式为______ 。
②300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式或名称______ 。(请写出计算过程)
【查阅资料】1、草酸亚铁晶体热分解的气体产物是H2O,CO,CO2
2、白色的无水CuSO4遇水蒸气会变成蓝色
【实验设计】

(1)从环保角度考虑,该套实验装置的明显缺陷是
(2)可选择以下实验装置中的

【问题讨论】
(3)D中浓硫酸的作用是
(4)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加盛有
【数据分析】
(6)称取3.60g草酸亚铁晶体(FeC2O4•2H2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:

①过程Ⅰ发生反应的化学方程式为
②300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式或名称
您最近半年使用:0次



