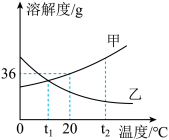
如图是甲、乙固体的溶解度曲线20℃时,将20g甲加入50g水中,充分搅拌后。形成溶液的质量为______ g;t2℃时,分别将甲、乙的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲______ (填“>”“<”或“=”)乙、20℃时,将68g甲的饱和溶液稀释为10%,需加水______ g。

更新时间:2022-05-03 18:31:00
|
相似题推荐
填空与简答-简答题
|
适中
(0.65)
【推荐1】水在生活、生产中和化学实验中起着十分重要的作用。
Ⅰ.自来水厂净化水的过程为:取水→沉降→过滤→吸附→消毒,高铁酸钾(K2FeO4)能用作絮凝剂。
(1)制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,则X的化学式为________ ,K2FeO4中铁元素的化合价为________ 。
(2)自来水厂的净水过程________ (选填“能”或“不能”)将硬水软化成软水。
Ⅱ.欲证明一瓶无色透明液体是纯水,可靠的实验方法是( )
A 1.01×105 Pa时沸点为100 ℃
B 测得其pH=7
C 电解时得到H2与O2的体积比为2∶1
Ⅲ.请根据如图实验现象并结合溶解度曲线回答(其中甲、乙、丙均不含结晶水)。
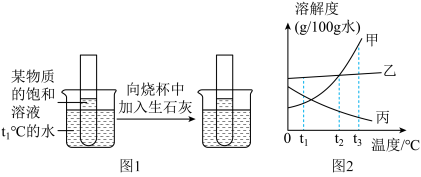
(1)生石灰与水反应的化学方程式为________ ,试管内所盛饱和溶液的溶质为对应溶解度曲线中的________ (选填“甲”“乙”或“丙”)。
(2)如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在________ ℃。
(3)t3℃时,将甲、乙、丙的饱和溶液都降温到t1℃,溶液中溶质质量分数由小到大的顺序为________ 。
Ⅰ.自来水厂净化水的过程为:取水→沉降→过滤→吸附→消毒,高铁酸钾(K2FeO4)能用作絮凝剂。
(1)制备K2FeO4的化学方程式为2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,则X的化学式为
(2)自来水厂的净水过程
Ⅱ.欲证明一瓶无色透明液体是纯水,可靠的实验方法是
A 1.01×105 Pa时沸点为100 ℃
B 测得其pH=7
C 电解时得到H2与O2的体积比为2∶1
Ⅲ.请根据如图实验现象并结合溶解度曲线回答(其中甲、乙、丙均不含结晶水)。

(1)生石灰与水反应的化学方程式为
(2)如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在
(3)t3℃时,将甲、乙、丙的饱和溶液都降温到t1℃,溶液中溶质质量分数由小到大的顺序为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】请根据物质的溶解度曲线,回答问题:

(1)40℃时,硝酸钾的溶解度是______ g,将160g硝酸钾的饱和溶液蒸发掉10g水,可析出固体______ g;
(2)溶解度受温度影响较大的是______ 。
(3)若实验室不小心将硝酸钾中混入了少量氯化钾,则提纯硝酸钾可以采用的方法的是______ 。
(4)60℃,将30g氯化钾加入50g水中充分搅拌,可形成溶液的质量为______ g。

(1)40℃时,硝酸钾的溶解度是
(2)溶解度受温度影响较大的是
(3)若实验室不小心将硝酸钾中混入了少量氯化钾,则提纯硝酸钾可以采用的方法的是
(4)60℃,将30g氯化钾加入50g水中充分搅拌,可形成溶液的质量为
您最近一年使用:0次
【推荐3】溶液出现在我们的生产和生活中。
(1)海水、河水或湖水中,都溶解了一定量的 ,但当气温升高时,养鱼池中常常要设法增加水中
,但当气温升高时,养鱼池中常常要设法增加水中 的含量,说明影响气体溶解度大小的主要因素之一是
的含量,说明影响气体溶解度大小的主要因素之一是___________ 。
(2)我国有些地区有一种说法:“冬天捞碱,夏天晒盐”。这里的碱是指 ,盐是指
,盐是指 。那么图中
。那么图中___________ (填“b”或“c”)的溶解度曲线与 的溶解度曲线相似。
的溶解度曲线相似。 ℃时,将
℃时,将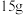 的a固体加入到
的a固体加入到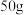 水中充分溶解并恢复到原温度后,得到溶液的质量为
水中充分溶解并恢复到原温度后,得到溶液的质量为___________ g。 的溶解度很小。
的溶解度很小。
a.“侯氏制碱法”的反应温度一般控制为30~35℃,因为在此温度时, 的溶解度较
的溶解度较___________ (填“大”或“小”)。
b.向饱和食盐水中先通入氨气后通入二氧化碳气体的目的是___________ 。
(1)海水、河水或湖水中,都溶解了一定量的
 ,但当气温升高时,养鱼池中常常要设法增加水中
,但当气温升高时,养鱼池中常常要设法增加水中 的含量,说明影响气体溶解度大小的主要因素之一是
的含量,说明影响气体溶解度大小的主要因素之一是(2)我国有些地区有一种说法:“冬天捞碱,夏天晒盐”。这里的碱是指
 ,盐是指
,盐是指 。那么图中
。那么图中 的溶解度曲线相似。
的溶解度曲线相似。 ℃时,将
℃时,将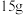 的a固体加入到
的a固体加入到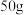 水中充分溶解并恢复到原温度后,得到溶液的质量为
水中充分溶解并恢复到原温度后,得到溶液的质量为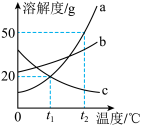

 的溶解度很小。
的溶解度很小。a.“侯氏制碱法”的反应温度一般控制为30~35℃,因为在此温度时,
 的溶解度较
的溶解度较b.向饱和食盐水中先通入氨气后通入二氧化碳气体的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】根据图1、2所示信息,回答相关问题。
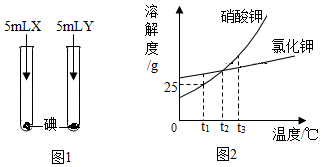
(1)图1所示实验,X、Y分别是水和汽油中的一种,实验中观察到:加入X后固体消失并得到棕色溶液,加入Y后固体未消失,则X是_______________ ,由实验可知,物质的溶解性与________________ 有关。
(2)图2为硝酸钾和氯化钾的溶解度曲线,则:
①t1°C时,硝酸钾的溶解度为_________________________ 。
②t1°C时,将20g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为__________________ 。
③t2°C时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是_________________________ 。
④将t3°C时硝酸钾、氧化钾的饱和溶液各100g 分别蒸发10g水,然后降温至t2°C,过滤,得到硝酸钾溶液a和氯化钾溶液b。对于溶液a和溶液b,下列说法正确的是__________________________ 。
A 都是饱和溶液
B 溶质质量a=b
C 溶质的质量分数a=b
D 溶液质量a<b
E 溶剂质量a<b

(1)图1所示实验,X、Y分别是水和汽油中的一种,实验中观察到:加入X后固体消失并得到棕色溶液,加入Y后固体未消失,则X是
(2)图2为硝酸钾和氯化钾的溶解度曲线,则:
①t1°C时,硝酸钾的溶解度为
②t1°C时,将20g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
③t2°C时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
④将t3°C时硝酸钾、氧化钾的饱和溶液各100g 分别蒸发10g水,然后降温至t2°C,过滤,得到硝酸钾溶液a和氯化钾溶液b。对于溶液a和溶液b,下列说法正确的是
A 都是饱和溶液
B 溶质质量a=b
C 溶质的质量分数a=b
D 溶液质量a<b
E 溶剂质量a<b
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为A、B、C三种固体物质的溶解度曲线,请回答下列问题:
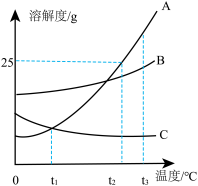
(1)t1 ℃时,三种物质的溶解度大小关系为________ 。
(2)t2 ℃时,A的饱和溶液的溶质质量分数为________ 。
(3)当B中混有少量的A时,提纯物质B一般采用_______ 方法。
(4)将等质量A、B、C的饱和溶液从t3 ℃降温至t1 ℃,下列说法正确的是____。

(1)t1 ℃时,三种物质的溶解度大小关系为
(2)t2 ℃时,A的饱和溶液的溶质质量分数为
(3)当B中混有少量的A时,提纯物质B一般采用
(4)将等质量A、B、C的饱和溶液从t3 ℃降温至t1 ℃,下列说法正确的是____。
| A.析出晶体质量:A > B > C |
| B.溶剂质量:A > C > B |
| C.溶质质量分数:B > A > C |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】A、B、C三种物质的溶解度曲线如图1所示。已知氧化钙溶于水后放热。

(1)P点含义是______ ,t3℃时,A物质的饱和溶液中溶质和溶液的质量比是______ 。
(2)t1℃时,A、B、C溶解度大小关系为______ 。
(3)若饱和A溶液中含有少量的B,提纯A的方法为______ 结晶,过滤。
(4)向图2试管中滴入2mL水后,若X中有固体析出,则X为______ (选填“A、B、C”)。
(5)将t2℃时A、B、C三种物质饱和溶液的温度升高到t3℃时,三种溶液的溶质质量分数大小关系是______ 。

(1)P点含义是
(2)t1℃时,A、B、C溶解度大小关系为
(3)若饱和A溶液中含有少量的B,提纯A的方法为
(4)向图2试管中滴入2mL水后,若X中有固体析出,则X为
(5)将t2℃时A、B、C三种物质饱和溶液的温度升高到t3℃时,三种溶液的溶质质量分数大小关系是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】(1)二氧化氮进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对 含有二氧化氮的废气进行处理。
①可以用 NaOH 溶液吸收:反应的化学方程式如下:2NO2+2NaOH==NaNO2+NaNO3+X,则 X 的化学式 为_______________ 。
②配制 200Kg 溶质质量分数为 5%的 NaOH 溶液,需要溶质质量分数为 20%的 NaOH 溶液___________ Kg,需要加水________________ Kg。
(2)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得 烧杯中溶液 pH 的变化如图所示。
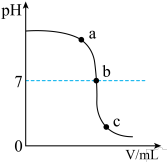
①经测定 a 点溶液中的溶质为__________ 、__________ (填化学式)。
②写出b点硫酸和氢氧化钠溶液反应的化学方程式__________ 。
③取 c 点溶液蒸发得到二种盐,它们是硫酸钠和硫酸氢钠。现若将 15g10%的硫酸氢钠溶液和 10g10% 的氢氧化钡溶液混合,请你写出该反应的化学方程式______________ 。
①可以用 NaOH 溶液吸收:反应的化学方程式如下:2NO2+2NaOH==NaNO2+NaNO3+X,则 X 的化学式 为
②配制 200Kg 溶质质量分数为 5%的 NaOH 溶液,需要溶质质量分数为 20%的 NaOH 溶液
(2)某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得 烧杯中溶液 pH 的变化如图所示。

①经测定 a 点溶液中的溶质为
②写出b点硫酸和氢氧化钠溶液反应的化学方程式
③取 c 点溶液蒸发得到二种盐,它们是硫酸钠和硫酸氢钠。现若将 15g10%的硫酸氢钠溶液和 10g10% 的氢氧化钡溶液混合,请你写出该反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属材料与人类的生产和生活密切相关。请回答:
(1)100g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量是_____ 。
(2)____ 是人体中含量最高的金属元素。
(3)家庭常见的锅有陶瓷锅、铁锅、铜锅等。
①铜锅比陶瓷锅加热更快。利用的金属性质是_______ 。
②铁锅清洗后如未擦干,容易产生红色铁锈,这是因为铁与________ 等发生化学反应,为防止铁制品生锈的方法有________ (填一条即可)。
(4)生活中常用的不锈钢、生铁、黄铜是_______ 材料。
(5)某同学为探究Fe、Cu、Mn三种金属的活动性,进行了如图所示的实验。
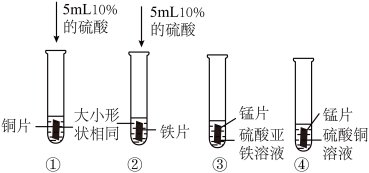
①C中观察到了明显的现象,则反应的化学方程式为_______ 。(已知锰可以与稀盐酸发生置换反应,生成物中锰元素显+2价)。
②通过以上实验,判断三种金属的活动性由强到弱的顺序是______ 。
③实验A-D中,不需要做的实验是______ (填序号)。
(1)100g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量是
(2)
(3)家庭常见的锅有陶瓷锅、铁锅、铜锅等。
①铜锅比陶瓷锅加热更快。利用的金属性质是
②铁锅清洗后如未擦干,容易产生红色铁锈,这是因为铁与
(4)生活中常用的不锈钢、生铁、黄铜是
(5)某同学为探究Fe、Cu、Mn三种金属的活动性,进行了如图所示的实验。

①C中观察到了明显的现象,则反应的化学方程式为
②通过以上实验,判断三种金属的活动性由强到弱的顺序是
③实验A-D中,不需要做的实验是
您最近一年使用:0次
【推荐3】溶液与人类的生活息息相关。
(1)下列少量物质分别放入水中,充分搅拌,能得到溶液的是_________(填序号)。
(2)下表是氯化钠和氯化钾在不同温度时的溶解度。
①20℃时,氯化钠的溶解度为______ g。
②20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液的质量为______ g。
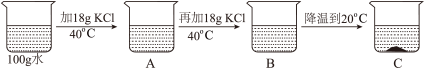
③某同学进行实验如图所示,得到相应的A、B、C三种溶液,其中属于饱和溶液的是______ 。
(3)如图是利用海水提取粗盐的过程:

根据海水晒盐的原理,下列说法正确的是______(填序号)。
(4)某同学配制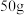 溶质质量分数为10%的氯化钠溶液。
溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为______ g。
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是______ (填序号)。
A.bcad B.bacd
③将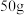 溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水
溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水______ g。
(1)下列少量物质分别放入水中,充分搅拌,能得到溶液的是_________(填序号)。
| A.面粉 | B.硝酸钾 | C.泥沙 | D.花生油 |
(2)下表是氯化钠和氯化钾在不同温度时的溶解度。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | |
②20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液的质量为
③某同学进行实验如图所示,得到相应的A、B、C三种溶液,其中属于饱和溶液的是

(3)如图是利用海水提取粗盐的过程:

根据海水晒盐的原理,下列说法正确的是______(填序号)。
| A.进入贮水池中的海水,氯化钠的质量逐渐减少 |
| B.在蒸发池中,海水中氯化钠的质量逐渐增加 |
| C.析出晶体后,母液中的氯化钠溶液达到饱和 |
(4)某同学配制
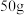 溶质质量分数为10%的氯化钠溶液。
溶质质量分数为10%的氯化钠溶液。①需要固体氯化钠的质量为
②配制过程有以下步骤:a.称量及量取b.计算c.溶解d.装瓶贴标签,正确顺序是
A.bcad B.bacd
③将
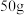 溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水
溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水
您最近一年使用:0次



