近日,中科院研究所在喜马拉雅地区发现超大型锂矿。工业上以锂辉石精矿(主要成分为Li2O)为原料制取碳酸锂的工艺流程如下图所示。
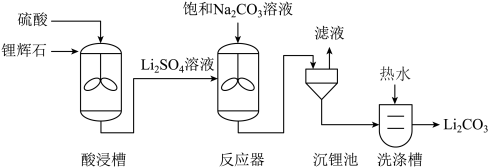
已知:碳酸锂的溶解度与温度的关系见下表。
请回答下列问题。
(1)标出碳酸锂中锂元素的化合价:______ 。
(2)“酸浸槽”中发生的反应的化学方程式是_____ ;工业上为提高酸浸速率,可采用的措施是_____ (写一条)。
(3)“沉锂池”中分离出的滤液中一定含有的溶质是______ 。
(4)“洗涤槽”中洗涤碳酸锂时要用热水,原因是_______ 。

已知:碳酸锂的溶解度与温度的关系见下表。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)标出碳酸锂中锂元素的化合价:
(2)“酸浸槽”中发生的反应的化学方程式是
(3)“沉锂池”中分离出的滤液中一定含有的溶质是
(4)“洗涤槽”中洗涤碳酸锂时要用热水,原因是
2022·江西·模拟预测 查看更多[1]
更新时间:2022-06-10 17:05:11
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】酸、碱、盐是我们身边重要的化合物,在生活和生产中具有广泛的应用。
(1)两种抗胃酸药剂的主要成分及建议每次剂量见表:
①根据表格写出用盐治疗胃酸过多的化学方程式___ 。
②服用Mg(OH)2的药效比服用NaHCO3“强”的原因是___ 。
(2)下列各组物质能在同一个反应中生成的是 (填字母)。
(3)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3),某些汽车安全气囊中装有叠氮化钠。请回答下列问题
①叠氮酸的水溶液中的阴离子是___ (填化学符号)。
②叠氮酸与NaOH溶液的反应的化学方程式是___ 。
(1)两种抗胃酸药剂的主要成分及建议每次剂量见表:
| 主要成分 | 氢氧化镁 | 碳酸氢钠 |
| 建议每次剂量/g | 0.5 | 0.3 |
②服用Mg(OH)2的药效比服用NaHCO3“强”的原因是
(2)下列各组物质能在同一个反应中生成的是 (填字母)。
| A.HCl、AgNO3 | B.Fe(OH)2、NaCl | C.ZnSO4、KNO3 | D.Fe2(SO4)3、H2 |
①叠氮酸的水溶液中的阴离子是
②叠氮酸与NaOH溶液的反应的化学方程式是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】请用化学方程式表示下列反应的原理。
(1)酒精用作燃料。___________ 。
(2)向饱和食盐水中依次通入氨气和二氧化碳,得到小苏打(在该溶液中难溶)和一种氮肥。___________ 。
(1)酒精用作燃料。
(2)向饱和食盐水中依次通入氨气和二氧化碳,得到小苏打(在该溶液中难溶)和一种氮肥。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(B1)等。
(1)次磷酸钠(NaH2PO2)常用作化学镀镍中的还原剂,次磷酸钠中磷元素的化合价是______ ;
(2)次磷酸是一种可溶于水的精细化工产品,请写出其化学式______ 。次磷酸可由 Ba(H2PO2)2溶液与硫酸反应制得,相关化学方程式为:______ 。
Ⅱ、价类二维图反映元素化合价与物质类别之间的关系。下图为铋元素(Bi)的价类二维图,物质A、B、C均含有元素铋。
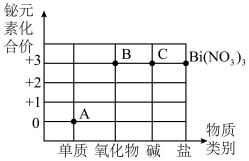
制备B的途径:
途径一:向硝酸铋溶液中滴加某溶流,充分混合,一定条件下可生成白色沉淀C;将C加热,脱水可得物质B。
途径二:物质A在氧气流中,加热可制得物质B。
请结合铋元素的价类二维图及制备B的两种途径回答相关问题:
(3)途径一,为得到沉淀C,应向硝酸铋溶液加入______ (填物质类别)溶液;由C生成B化学方程式为______ 。
(4)途径二,写出由A生成B的化学方程式为______ 。
(1)次磷酸钠(NaH2PO2)常用作化学镀镍中的还原剂,次磷酸钠中磷元素的化合价是
(2)次磷酸是一种可溶于水的精细化工产品,请写出其化学式
Ⅱ、价类二维图反映元素化合价与物质类别之间的关系。下图为铋元素(Bi)的价类二维图,物质A、B、C均含有元素铋。

制备B的途径:
途径一:向硝酸铋溶液中滴加某溶流,充分混合,一定条件下可生成白色沉淀C;将C加热,脱水可得物质B。
途径二:物质A在氧气流中,加热可制得物质B。
请结合铋元素的价类二维图及制备B的两种途径回答相关问题:
(3)途径一,为得到沉淀C,应向硝酸铋溶液加入
(4)途径二,写出由A生成B的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】用化学符号填空。
(1)氯化亚铁:_________ ;
(2)二氧化硫中硫元素的化合价为+4价:______ ;
(3)治疗胃酸过多的盐_________ 。
(1)氯化亚铁:
(2)二氧化硫中硫元素的化合价为+4价:
(3)治疗胃酸过多的盐
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】自来水厂净化过程的主要流程如图:

(1)下列有关说法错误的是_______________ (填字母)。
(2)“沉降池”中可用明矾作絮凝剂,其化学式为KA1(SO4)n·12H2O,n的值为__________ 。
(3)小刚取少量液体于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体d是_______________ 水。生活中为降低水的硬度并杀死病菌微生物,可采用的方法是________________ 。
(4)化学实验室中水的用途很多。如红磷燃烧测定空气中氧气的含量的实验中,集气瓶内加少量水可以吸收燃烧放出的热量以及生成的白烟,请写出红磷在氧气中燃烧的符号表达式________________ 。

(1)下列有关说法错误的是
| A.步骤ab可除去难溶性杂质 | B.X试剂常用的是活性炭 |
| C.步骤d为蒸馏 | D.净化后的水为纯净物 |
(2)“沉降池”中可用明矾作絮凝剂,其化学式为KA1(SO4)n·12H2O,n的值为
(3)小刚取少量液体于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体d是
(4)化学实验室中水的用途很多。如红磷燃烧测定空气中氧气的含量的实验中,集气瓶内加少量水可以吸收燃烧放出的热量以及生成的白烟,请写出红磷在氧气中燃烧的符号表达式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】研究物质的溶解对于生产、生活有着重要意义。
(1)如表是硝酸钾的部分溶解度数据。
由表中数据可知,硝酸钾的溶解度随温度的升高而_______ (填:增大或减小)。能将该不饱和溶液转化为饱和溶液的一种方法是_______ 。
(2)探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如图所示:_______ 。(选填编号)。
(1)如表是硝酸钾的部分溶解度数据。
| 温度(℃) | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 31.6 | 63.9 | 110 | 169 |
(2)探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如图所示:

a. b.
b. c.
c. d.
d.
您最近一年使用:0次
【推荐2】硫酸钾是重要的化工原料,在生产过程中常混有氯化钠杂质。
(1)硫酸钾在农业上可作为_________ (填“钾肥”或“磷肥”或“氮肥”)。
(2)取少量K2SO4溶液,滴入Ba(NO3)2溶液,反应的化学方程式是_____ ,该反应的基本反应类型是_________ 。
(3)硫酸钾和氯化钠的部分溶解度数据如下表。
60℃时,NaCl的溶解度为________ g;100℃时,10g水中最多溶解K2SO4________ g。
(4)某K2SO4样品中混有NaCl杂质,可利用溶解度差异进行提纯,称取27.5g样品进行实验,过程如下:

①滤液B中,K2SO4________ (选填“达到”或“未达到”)饱和状态;
②27.5g样品中NaC1的质量是_________ 。
③分析上述实验,说明设计步骤Ⅱ对后续操作的作用是__________ (填字母)。
A.获得较多的硫酸钾
B.可知样品中硫酸钾和氯化钠的质量
(1)硫酸钾在农业上可作为
(2)取少量K2SO4溶液,滴入Ba(NO3)2溶液,反应的化学方程式是
(3)硫酸钾和氯化钠的部分溶解度数据如下表。
| 温度(℃) | 0 | 20 | 60 | 100 |
| NaCl | 35.7 | 36.0 | 37.1 | 39.2 |
| K2SO4 | 7.4 | 11.1 | 18.2 | 24.1 |
(4)某K2SO4样品中混有NaCl杂质,可利用溶解度差异进行提纯,称取27.5g样品进行实验,过程如下:

①滤液B中,K2SO4
②27.5g样品中NaC1的质量是
③分析上述实验,说明设计步骤Ⅱ对后续操作的作用是
A.获得较多的硫酸钾
B.可知样品中硫酸钾和氯化钠的质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】NaCl和KNO3在不同温度时的溶解度如下表:
(1)两者的溶解度受温度影响较小的是______ 。
(2)20℃时,某同学进行了如下实验,得到相应溶液①~④。
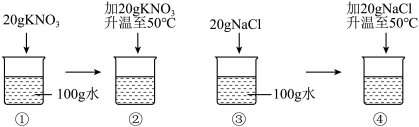
其中,①~④中是饱和溶液的是______  填序号,下同
填序号,下同 ,溶质质量分数相等的是①和
,溶质质量分数相等的是①和______ 。若再将②和④中溶液降温至 ,所得溶液质量较大的是
,所得溶液质量较大的是______  填化学式
填化学式 溶液。
溶液。
| 温度℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.6 | 63.9 | 85.5 | 110 | |
(1)两者的溶解度受温度影响较小的是
(2)20℃时,某同学进行了如下实验,得到相应溶液①~④。

其中,①~④中是饱和溶液的是
 填序号,下同
填序号,下同 ,溶质质量分数相等的是①和
,溶质质量分数相等的是①和 ,所得溶液质量较大的是
,所得溶液质量较大的是 填化学式
填化学式 溶液。
溶液。
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A一F均为初中化学常见的物质,它们之间的关系如图所示(“→”表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
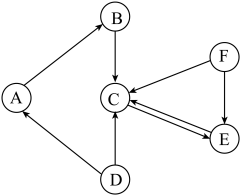
(1)C的化学式是__________ 。
(2)A→B反应的化学方程式为__________ 。
(3)F→E反应的化学方程式为__________ 。

(1)C的化学式是
(2)A→B反应的化学方程式为
(3)F→E反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】石灰石是自然界中一种重要的矿物。医用氯化钙晶体可以生产补钙、抗过敏和消炎等药物,以某地产的石灰石(含有一定量的MgCO3及SiO2)生产医用氯化钙晶体的主要流程如下:

(1)根据上述流程分析,SiO2具有的性质是_______ 。
(2)步骤②中生成固体X的化学方程式为_______ 。
(3)上述流程中所发生反应的基本反应类型为_______ 反应。
(4)下列结论正确的是_______(填字母序号,双选)。

(1)根据上述流程分析,SiO2具有的性质是
(2)步骤②中生成固体X的化学方程式为
(3)上述流程中所发生反应的基本反应类型为
(4)下列结论正确的是_______(填字母序号,双选)。
| A.溶液A中一定含有氯化钙、氯化镁、盐酸 |
| B.步骤③加入稀盐酸的目的是中和溶液中的氢氧化钙 |
| C.溶液B中的氯化钙质量小于溶液A中氯化钙质量 |
| D.溶液C中氯化钙的质量分数一定小于溶液D |
您最近一年使用:0次




