某化学兴趣小组的同学为测定假黄金(铜锌合金)中锌的质量分数,取20g假黄金加入到100g稀盐酸中,恰好完全反应,剩余固体质量为13.5g。试求:
(1)假黄金中锌的质量分数是_____________ 。
(2)所用稀盐酸中溶质的质量分数是多少。(写出计算过程)
(1)假黄金中锌的质量分数是
(2)所用稀盐酸中溶质的质量分数是多少。(写出计算过程)
更新时间:2022/06/06 00:11:33
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】镁是一种重要金属,广泛应用于制造火箭、导弹和飞机的部件等。工业上通过电解熔融氯化镁制备单质镁:MgCl2(熔融) Mg+Cl2↑。请计算:
Mg+Cl2↑。请计算:
(1)该反应前后氯元素的化合价___________ (填“升高”或“降低”或“不变”)。
(2)应用此法制备48t镁,至少需要消耗MgCl2的质量是多少?
 Mg+Cl2↑。请计算:
Mg+Cl2↑。请计算:(1)该反应前后氯元素的化合价
(2)应用此法制备48t镁,至少需要消耗MgCl2的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】小明喜欢养金鱼,他上网查阅资料得知:鱼缸中每升水的溶氧量低于 0.003g 时, 鱼就会死亡。过氧化钙(CaO2)是一种化学增氧剂,其反应原理是 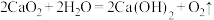 请回答:小明将 2.88g 过氧化钙放入盛有 200L 水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧量是否符合最低要求? (假设产生的氧气完全溶入水,其他因素忽略不计)
请回答:小明将 2.88g 过氧化钙放入盛有 200L 水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧量是否符合最低要求? (假设产生的氧气完全溶入水,其他因素忽略不计)
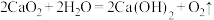 请回答:小明将 2.88g 过氧化钙放入盛有 200L 水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧量是否符合最低要求? (假设产生的氧气完全溶入水,其他因素忽略不计)
请回答:小明将 2.88g 过氧化钙放入盛有 200L 水的鱼缸中,请你通过计算分析,当氧气完全释放后,鱼缸中水的溶氧量是否符合最低要求? (假设产生的氧气完全溶入水,其他因素忽略不计)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某同学欲利用实验测定某锌粒中锌的纯度,实验数据如下表(已知:实验中稀硫酸过量,杂质不与稀硫酸反应)
(1)计算该锌粒的纯度(写出计算过程,结果精确到0.1%)。
(2)实际实验测得锌粒的纯度偏大,你认为可能的原因是___________ (写出1点即可)。
| 实验前烧杯和稀硫酸的质量/g | 实验前锌粒的质量/g | 实验后烧杯及剩余物的质量/g |
| 300.5 | 7.0 | 307.3 |
(2)实际实验测得锌粒的纯度偏大,你认为可能的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将2.4克镁粉投入100克稀硫酸溶液中,镁粉与硫酸(H2SO4)恰好完全反应,反应化学方程式为: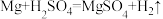 。请回答下列问题:
。请回答下列问题:
(1)MgSO4中Mg2+与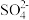 的质量比为
的质量比为_________ 。
(2)计算硫酸溶液的质量分数是多少?
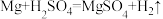 。请回答下列问题:
。请回答下列问题:(1)MgSO4中Mg2+与
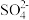 的质量比为
的质量比为(2)计算硫酸溶液的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】市场上常用黄铜(铜锌合金)冒充黄金骗取钱财。某同学取22.6g的某黄铜样品放入烧杯中,向其中分四次加入等质量的同一稀硫酸,每次均充分反应。实验数据记录如下:
分析表中数据,完成下列问题:
(1)该样品中铜的质量分数_______ ;(计算结果保留0.1%)
(2)第2次实验结束后,溶液中的溶质为_______ (化学式)。
(3)实验过程中,产生氢气的质量为______ ?(请写出计算过程,结果保留两位小数)。
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀硫酸的质量/g | 40 | 40 | 40 | 40 |
| 剩余固体质量/g | 20 | 17.4 | 14.8 | 14.2 |
分析表中数据,完成下列问题:
(1)该样品中铜的质量分数
(2)第2次实验结束后,溶液中的溶质为
(3)实验过程中,产生氢气的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】小王同学想测定某Cu-Zn合金中铜的质量分数,取合金粉末13g,向其中逐渐加入一定溶质质量分数的稀硫酸,所得稀硫酸与生成氢气的质量关系如图所示。
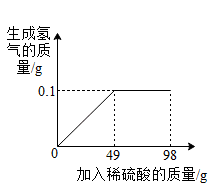
请完成下列分析及计算:
(1)铜锌合金属于________ (填“合成材料”或“金属材料”)。
(2)计算所用稀硫酸中溶质的质量分数。

请完成下列分析及计算:
(1)铜锌合金属于
(2)计算所用稀硫酸中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】我校化学实验室新进了一批石灰石,化学兴趣小组的同学很感兴趣,立即对其进行了如下探究活动。小红取6.0g石灰石于烧杯中,再向其中加入稀盐酸50.0g,恰好完全反应(杂质不反应),反应后烧杯中物质的总质量为53.8g。
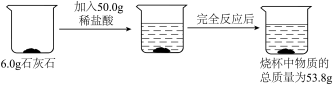
(1)生成CO₂的质量为______ 。
(2)稀盐酸中溶质的质量分数是多少?

(1)生成CO₂的质量为
(2)稀盐酸中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】日常使用的金属材料,大多数属于合金,黄铜是以锌作主要添加元素的铜合金。
(1)赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O中铜元素与氧元素的质量比是___ 。
(2)弹壳的黄铜只含有锌和铜。将11g弹壳放在盛有100g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是110.9g。计算:
①产生氢气的质量___________ 。
②弹壳中锌的质量___________ 。
③反应后所得溶液中ZnSO4的质量分数___________ (计算结果保留一位小数)。
(1)赤铜(Cu2O)是我国古代制取黄铜的一种原料。Cu2O中铜元素与氧元素的质量比是
(2)弹壳的黄铜只含有锌和铜。将11g弹壳放在盛有100g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是110.9g。计算:
①产生氢气的质量
②弹壳中锌的质量
③反应后所得溶液中ZnSO4的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】硫酸厂排放的废水中通常含有少量残余硫酸,为测定废水中硫酸的溶质质量分数,某校化学学习小组的同学们在老师的指导下做如下实验:取100g该废水,向其中逐滴加入溶质质量分数为8%的氢氧化钠溶液。所滴加的NaOH溶液的质量与溶液pH变化如图1所示:
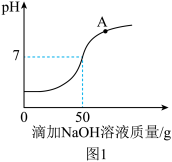
(1)恰好反应时,消耗的NaOH溶液中溶质NaOH的质量为______ g,A点处所得溶液中溶质为______ (填化学式)。
(2)求废水中硫酸的溶质质量分数(写由计算过程)。
(3)请在如图2画出废水中硫酸钠的质量随NaOH溶液质量变化的图像。


(1)恰好反应时,消耗的NaOH溶液中溶质NaOH的质量为
(2)求废水中硫酸的溶质质量分数(写由计算过程)。
(3)请在如图2画出废水中硫酸钠的质量随NaOH溶液质量变化的图像。

您最近一年使用:0次



