某同学欲利用实验测定某锌粒中锌的纯度,实验数据如下表(已知:实验中稀硫酸过量,杂质不与稀硫酸反应)
(1)计算该锌粒的纯度(写出计算过程,结果精确到0.1%)。
(2)实际实验测得锌粒的纯度偏大,你认为可能的原因是___________ (写出1点即可)。
| 实验前烧杯和稀硫酸的质量/g | 实验前锌粒的质量/g | 实验后烧杯及剩余物的质量/g |
| 300.5 | 7.0 | 307.3 |
(2)实际实验测得锌粒的纯度偏大,你认为可能的原因是
更新时间:2024-05-27 17:42:25
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】向6.5克锌中加入过量的10%的稀硫酸,完全反应后,测得反应后溶液的质量为106.3克,其反应过程如下图所示,求反应后溶液中H2SO4的质量。


您最近一年使用:0次
计算题
|
适中
(0.65)
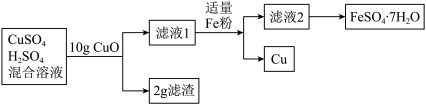
【推荐2】某工厂废水经初步处理后可得CuSO4和H2SO4的混合溶液,化学兴趣小组设计实验模拟后续处理过程,并得到了 Cu 和另一种重要化工原料绿矾(FeSO4·7H2O)。其过程如图:_____ g。
(2)若原混合溶液质量为200g,求混合溶液中H2SO4的质量分数(写出计算过程)。
(3)若反应消耗11.2gFe,求理论上得到的绿矾中硫酸亚铁的质量(写出计算过程)。
(2)若原混合溶液质量为200g,求混合溶液中H2SO4的质量分数(写出计算过程)。
(3)若反应消耗11.2gFe,求理论上得到的绿矾中硫酸亚铁的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用4.0g石灰石样品,把40g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
(1)从以上数据可知,这四次实验中,第___________ 次石灰石样品中碳酸钙完全反应。
(2)稀盐酸中溶质质量分数是多少?(写出计算过程,结果保留1位小数)。
(3)如果用溶质质量分数为35%、密度为1.10g/mL的浓盐酸配制40g的该稀盐酸,则需要___________ mL浓盐酸。
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入10g | 3.0g |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.0g |
| 第四次加入10g | 0.6g |
(2)稀盐酸中溶质质量分数是多少?(写出计算过程,结果保留1位小数)。
(3)如果用溶质质量分数为35%、密度为1.10g/mL的浓盐酸配制40g的该稀盐酸,则需要
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】小伟同学利用碳酸钠溶液测定除锈剂(主要成分是硫酸)中硫酸的质量分数,实验过程如下:
①向烧杯中加入50 g除锈剂;(除锈剂中其他成分不与碳酸钠反应,反应中产生的气体全部逸出)
②向除锈剂中滴加碳酸钠溶液,边滴加边搅拌,至不再有气泡放出,共消耗碳酸钠溶液40 g;
③反应后,烧杯中剩余物质的总质量为87.8 g。
根据上述实验数据计算除锈剂中硫酸的质量分数__________ 。
①向烧杯中加入50 g除锈剂;(除锈剂中其他成分不与碳酸钠反应,反应中产生的气体全部逸出)
②向除锈剂中滴加碳酸钠溶液,边滴加边搅拌,至不再有气泡放出,共消耗碳酸钠溶液40 g;
③反应后,烧杯中剩余物质的总质量为87.8 g。
根据上述实验数据计算除锈剂中硫酸的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
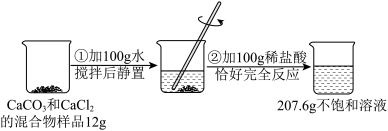
(1)实验产生的气体的质量 。
(2)所用稀盐酸的溶质的质量分数为多少?

(1)实验产生的气体的质量 。
(2)所用稀盐酸的溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为测定硫酸钠和硫酸镁固体混合物中硫酸镁的质量分数。某同学取固体混合物26.2g,向其中加入216.6g水,使其完全溶解配制成混合溶液。将250g一定溶质质量分数的氢氧化钠溶液平均分成5等份,依次加入到上述混合溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下表:
试分析该实验并计算。
(1)在溶解配制成硫酸钠和硫酸镁混合溶液时用到的玻璃仪器有___________ 。(写一种)
(2)m的值为___________ 。
(3)固体混合物中硫酸镁的质量___________ g 。
(4)恰好完全反应时,所得不饱和溶液中溶质的质量分数。(结果保留0.1%)
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 氢氧化钠溶液质量/g | 50 | 50 | 50 | 50 | 50 |
| 产生沉淀质量/g | 1.45 | 2.9 | m | 5.8 | 5.8 |
试分析该实验并计算。
(1)在溶解配制成硫酸钠和硫酸镁混合溶液时用到的玻璃仪器有
(2)m的值为
(3)固体混合物中硫酸镁的质量
(4)恰好完全反应时,所得不饱和溶液中溶质的质量分数。(结果保留0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】2023年7月,深海重器“奋斗者号”载人潜水器累计实现25次万米级下潜。潜水器的许多电子元件使用了黄铜。为测定某黄铜(假设合金中仅含铜、锌)中铜的含量,某同学称取10g黄铜粉末于烧杯中,将40g稀硫酸分四次加入,充分反应,测得实验数据如下表所示。
(1)10g黄铜粉末中含锌的质量是________________ g。
(2)所用稀硫酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 |
| 烧杯中剩余固体的质量(g) | 8.7 | 7.4 | 6.1 | 6.1 |
(2)所用稀硫酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有一份铁粉与铜粉混合物样品,为了解其组成,同学们取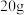 样品,向其中加入足量的稀硫酸,待反应完全后过滤,称得不溶物的质量为
样品,向其中加入足量的稀硫酸,待反应完全后过滤,称得不溶物的质量为 。
。
(1)金属混合物中铜的质量分数为___________ 。
(2)计算生成氢气的质量(写出计算过程)。
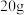 样品,向其中加入足量的稀硫酸,待反应完全后过滤,称得不溶物的质量为
样品,向其中加入足量的稀硫酸,待反应完全后过滤,称得不溶物的质量为 。
。(1)金属混合物中铜的质量分数为
(2)计算生成氢气的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】现有铁粉与铜粉混合物10g,小红想探究此混合物中铁的含量,于是请化学老师和她一起探究:在实验室用足量的稀硫酸分多次与该混合物充分反应,实验结果如表:
根据上表中的数据分析,完成下列问题:
(1)10g混合物中铜的质量为_______ 克。
(2)m的值为_______ 。
(3)计算稀硫酸的溶质质量分数为多少_______ ?
| 稀硫酸/g | 10 | 10 | 10 | 10 | 10 |
| 剩余固体质量/g | 8.6 | m | 5.8 | 4.4 | 4.4 |
(1)10g混合物中铜的质量为
(2)m的值为
(3)计算稀硫酸的溶质质量分数为多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】碳酸氢铵是我国主要的农用氮肥之一,同学们利用如图实验装置,测定某样品中碳酸氢铵的含量(已知:  ,碱石灰可吸收二氧化碳)。现取10.0g样品进行测定,实验测得D装置反应前后的质量关系如下表所示:
,碱石灰可吸收二氧化碳)。现取10.0g样品进行测定,实验测得D装置反应前后的质量关系如下表所示:
(1)试计算样品中碳酸氢铵的质量分数(写出计算过程)。
(2)实验测定样品中碳酸氢铵的质量分数比真实值偏小,其原因可能是:_____ (答一点即可)。
 ,碱石灰可吸收二氧化碳)。现取10.0g样品进行测定,实验测得D装置反应前后的质量关系如下表所示:
,碱石灰可吸收二氧化碳)。现取10.0g样品进行测定,实验测得D装置反应前后的质量关系如下表所示:
| D装置及其中的贼石灰总重量/g | 反应前 | 反应后 |
| 320 | 324.4 |
(1)试计算样品中碳酸氢铵的质量分数(写出计算过程)。
(2)实验测定样品中碳酸氢铵的质量分数比真实值偏小,其原因可能是:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】课外拓展活动时,化学实验员取出一瓶盐酸,让同学们测定其浓度。实验如下:取一个200mL的烧杯,测其质量,倒入一定量盐酸,再次测量,然后滴加10%的硝酸银溶液并用玻璃棒不断搅拌,待不再有沉淀产生后停止滴加。静置后将烧杯内物质过滤,将滤渣烘干、称量。实验数据记录如下:
解答下列问题:
(1)用玻璃棒不断搅拌的目的是:_______ 。
(2)根据实验数据计算盐酸的溶质质量分数_______ 。(写出计算过程,计算结果保留一位小数)
(3)实验结束后,实验员展示盐酸瓶上标签标注的质量分数为16%,则测定所得质量分数和标注质量分数有出入的原因可能是_______ 。
①盐酸瓶盖密封不严,HCl挥发了;②烧杯内有水;③过滤时滤纸破损;④搅拌后玻璃棒上沾有不溶物;⑤滴加硝酸银溶液的量不够;⑥滤渣未烘干,含有水分。
| 项目 | 质量(g) |
| 烧杯 | 58.6 |
| 烧杯+盐酸 | 108.6 |
| 滤渣 | 28.7 |
(1)用玻璃棒不断搅拌的目的是:
(2)根据实验数据计算盐酸的溶质质量分数
(3)实验结束后,实验员展示盐酸瓶上标签标注的质量分数为16%,则测定所得质量分数和标注质量分数有出入的原因可能是
①盐酸瓶盖密封不严,HCl挥发了;②烧杯内有水;③过滤时滤纸破损;④搅拌后玻璃棒上沾有不溶物;⑤滴加硝酸银溶液的量不够;⑥滤渣未烘干,含有水分。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】鸡蛋壳的主要成分是碳酸钙,某兴趣小组为了测定鸡蛋壳中CaCO3的含量。现取清洗、晾干、捣碎的鸡蛋壳碎片15g,放在烧杯中,然后向其中加入80g的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示。
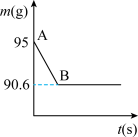
(1)实验前将鸡蛋壳捣碎,其目的是___________ ;
(2)依据图中数据分析,生成CO2的质量为___________ ;
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。

(1)实验前将鸡蛋壳捣碎,其目的是
(2)依据图中数据分析,生成CO2的质量为
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。
| A.向鸡蛋壳中滴加过量稀盐酸 | B.鸡蛋壳碎片未完全反应 |
| C.烧杯中部分氯化氢和水蒸气随二氧化碳逸出 | D.鸡蛋壳未晾干,有残留的水 |
您最近一年使用:0次



