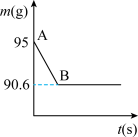
鸡蛋壳的主要成分是碳酸钙,某兴趣小组为了测定鸡蛋壳中CaCO3的含量。现取清洗、晾干、捣碎的鸡蛋壳碎片15g,放在烧杯中,然后向其中加入80g的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示。
(1)实验前将鸡蛋壳捣碎,其目的是___________ ;
(2)依据图中数据分析,生成CO2的质量为___________ ;
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。

(1)实验前将鸡蛋壳捣碎,其目的是
(2)依据图中数据分析,生成CO2的质量为
(3)计算该鸡蛋壳中CaCO3的质量分数(结果精确到0.1%);
(4)下列情况会导致鸡蛋壳中碳酸钙质量分数测量值偏小的是___________(双选)。
| A.向鸡蛋壳中滴加过量稀盐酸 | B.鸡蛋壳碎片未完全反应 |
| C.烧杯中部分氯化氢和水蒸气随二氧化碳逸出 | D.鸡蛋壳未晾干,有残留的水 |
更新时间:2024-02-07 14:34:21
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】氢化钙(CaH2)是一种常用的储氢材料,其与水反应方程式为:CaH2+2H2O=Ca(OH)2+2H2↑。某化学兴趣小组为了测定氢化钙样品中含CaH2的质量,设计了如下实验:将50g氢化钙样品加入50g水中充分反应(已知氢化钙样品中杂质不参与反应),最终得到剩余物质总质量为96g。计算:
(1)上述实验中生成氢气质量为______ g。
(2)氢化钙样品中含CaH2的质量为多少?
(1)上述实验中生成氢气质量为
(2)氢化钙样品中含CaH2的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现将15 g石灰石样品与105.4 g稀盐酸放入烧杯中充分反应(杂质不溶于稀盐酸且不与稀盐酸反应),反应时间与反应前后烧杯内物质的质量变化如下图所示:
(1)反应产生二氧化碳的质量_______ ;
(2)试计算这种石灰石中碳酸钙的质量分数。(计算结果保留一位小数)
| 反应时间 | 5 | 15 | 20 | 25 | 30 | 35 |
| 质量(克) | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
(2)试计算这种石灰石中碳酸钙的质量分数。(计算结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验中学兴趣小组的同学在实验室加热氯酸钾和二氧化锰的混合物制取氧气,反应过程中测量的有关数据记录如下,请计算:
(1)生成氧气质量是______ g。
(2)原混合物中氯酸钾的质量分数。(写出计算过程,精确到0.1%)
| 反应时间(min) | 0 | 1 | 2 | 3 | 4 |
| 试管中固体质量(g) | 27 | 23.8 | 20.6 | 17.4 | 17.4 |
(2)原混合物中氯酸钾的质量分数。(写出计算过程,精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室常用氯酸钾和二氧化锰的混合物制取氧气。现有氯酸钾和二氧化锰的混合物50g,完全反应后称量剩余物质的质量为40.4g。请计算:
(1)制得氧气的质量为__________ 。
(2)混合物中氯酸钾的质量分数。
(1)制得氧气的质量为
(2)混合物中氯酸钾的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某黄铜样品是由铜、锌和 5%其他物质组成(其他物质不含铜、锌元素,也不溶于水,不与其它物质反应),为了测定黄铜样品中铜的质量分数,某化学小组进行了如下实验:

(1)发生反应的化学方程式为_______ ;
(2)根据已知条件列出求解 100g 该黄铜样品中锌的质量(x)的比例式为_______ ;
(3)黄铜样品中锌的质量为_______ 。
(4)该黄铜样品中铜的质量分数是_______ ;
(5)向过滤后所得滤液中加入 23.4g 水,则最终所得溶液中溶质的质量分数是_______ 。

(1)发生反应的化学方程式为
(2)根据已知条件列出求解 100g 该黄铜样品中锌的质量(x)的比例式为
(3)黄铜样品中锌的质量为
(4)该黄铜样品中铜的质量分数是
(5)向过滤后所得滤液中加入 23.4g 水,则最终所得溶液中溶质的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】微型化学实验使用药品的量很少,产生的废弃物也很少,因此被誉为绿色环保的化学实验。用如图微型仪器完成制取并检验CO2的实验只消耗了0.55 g 10%的盐酸。求:
(1)产生CO2的质量是多少克?________ (结果保留三位小数)
(2)如果10%的盐酸密度为1.1g/cm3,消耗盐酸的体积是多少毫升?_______
(3)通常完成这个实验大约需10%的盐酸5 mL,这是微型实验用药量的多少倍?_________

(1)产生CO2的质量是多少克?
(2)如果10%的盐酸密度为1.1g/cm3,消耗盐酸的体积是多少毫升?
(3)通常完成这个实验大约需10%的盐酸5 mL,这是微型实验用药量的多少倍?

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用石灰石与稀盐酸反应制取二氧化碳。若要制取4.4g二氧化碳,需要溶质的质量分数为10%的盐酸多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】化学小组参与“铅蓄废电池中硫酸回收"的研学项目,回收时需要测定废液中硫酸的质量分数。取100g废液于锥形瓶中,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液至恰好完全反应,共消耗氢氧化钠溶液100g(不考虑杂质的影响)。
请计算:
(1)计算废液中硫酸的质量分数。(写出计算过程)
(2)计算恰好完全反应时,所得溶液的溶质质量分数。(写出计算过程)
(3)若配制氢氧化钠溶液时,用量筒量水时俯视读数,会导致测定废液中硫酸的质量分数结果______ (选填“偏大”、“偏小”或“不变”)。
请计算:
(1)计算废液中硫酸的质量分数。(写出计算过程)
(2)计算恰好完全反应时,所得溶液的溶质质量分数。(写出计算过程)
(3)若配制氢氧化钠溶液时,用量筒量水时俯视读数,会导致测定废液中硫酸的质量分数结果
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】11g食用纯碱中往往会含有少量的氯化钠。化学兴趣小组的同学通过实验来测定某纯碱样品中碳酸钠的质量分数。他们取11g样品放入烧杯中,逐滴加入溶质质量分数为5%的稀盐酸,然后按图1流程进行实验,测得加入稀盐酸的量与产生气体的质量关系如图2所示:___________ 。
(2)图2中,当滴入的稀盐酸至P点时,溶液含有的溶质为___________ (填化学式)。
(3)计算样品中碳酸钠的质量分数(写出过程,结果保留为0.1%)。
(4)某同学用过程②得到的氯化钠晶体质量求样品中碳酸钠的质量,这样算出的结果比实际值___________ (填“大”“小”或“一样”)。
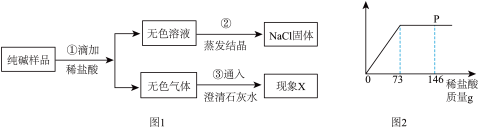
(2)图2中,当滴入的稀盐酸至P点时,溶液含有的溶质为
(3)计算样品中碳酸钠的质量分数(写出过程,结果保留为0.1%)。
(4)某同学用过程②得到的氯化钠晶体质量求样品中碳酸钠的质量,这样算出的结果比实际值
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】上饶玉山县石灰石储量达33亿吨。某兴趣小组取某石灰石样品,粉碎后,分别取样加入不同质量的同种盐酸进行实验,数据记录如下表,请回答有关问题:(杂质不参加反应且难溶于水)
(1)实验时先将石灰石粉碎,其目的是___ ,实验中取用粉碎后的石灰石,需用到的仪器是____ 。
(2)充分反应后,将剩余固体从溶液中分离出来的操作是________ 。
(3)实验后发现,所测剩余固体的质量偏大,从操作角度分析,其原因可能是_______ 。
(4)12g石灰石样品完全反应生成二氧化碳的质量是_____ ?(写出计算过程)
| 实验1 | 实验2 | 实验3 | |
| 石灰石质量/g | 12 | 12 | 12 |
| 加入稀盐酸的质量/g | 30 | 50 | 60 |
| 充分反应后剩余固体质量/g | 6 | 2 | 2 |
(1)实验时先将石灰石粉碎,其目的是
(2)充分反应后,将剩余固体从溶液中分离出来的操作是
(3)实验后发现,所测剩余固体的质量偏大,从操作角度分析,其原因可能是
(4)12g石灰石样品完全反应生成二氧化碳的质量是
您最近一年使用:0次




