铅蓄电池放电过程中发生反应的工作原理为: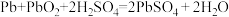 ,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸_____ 克?
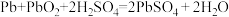 ,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
更新时间:2022-06-10 16:39:16
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】现有20℃100g5%的食盐溶液,试计算:
(1)若使原溶液溶质质量分数变为20%,则需加入多少氯化钠?
(2)若使原溶液溶质质量分数变为10%,则应蒸发掉多少水?
(1)若使原溶液溶质质量分数变为20%,则需加入多少氯化钠?
(2)若使原溶液溶质质量分数变为10%,则应蒸发掉多少水?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】分别对100g 20%的硝酸钾溶液进行如下操作,请计算出所得溶液的溶质质量分数:
(1)加入100g水:________
(2)加入20g硝酸钾:________。
(1)加入100g水:________
(2)加入20g硝酸钾:________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,在 20℃时,称取 5g 样品,加入27g 水完全溶解后,缓慢加入稀盐酸,至恰好完全反应时,用去 10%的稀盐酸 36.5g。(该反应的化学方程式为:NaOH+HCl=NaCl+H2O) 试计算:
(1)样品中氢氧化钠的质量分数。
(2)反应后所得溶液中溶质的质量分数。
(3)已知 20℃时,氯化钠的溶解度为 36 g,试通过简单计算确定反应后所得溶液是否为 20℃时该溶质的饱和溶液。
(1)样品中氢氧化钠的质量分数。
(2)反应后所得溶液中溶质的质量分数。
(3)已知 20℃时,氯化钠的溶解度为 36 g,试通过简单计算确定反应后所得溶液是否为 20℃时该溶质的饱和溶液。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】有一份黄铜(铜锌合金)样品,为确定其组成,某同学将32.5g样品碎片加入100g稀硫酸中,恰好完全反应,放出0.4g气体。试求:
(1)样品中金属锌的质量是_____g。
(2)所用稀硫酸的溶质质量分数_____(写出计算过程)。
(1)样品中金属锌的质量是_____g。
(2)所用稀硫酸的溶质质量分数_____(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向一定质量的稀盐酸中加入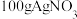 溶液,恰好完全反应,过滤后得
溶液,恰好完全反应,过滤后得 白色沉淀和
白色沉淀和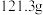 滤液.求稀盐酸中溶质的质量分数
滤液.求稀盐酸中溶质的质量分数______ .
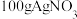 溶液,恰好完全反应,过滤后得
溶液,恰好完全反应,过滤后得 白色沉淀和
白色沉淀和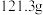 滤液.求稀盐酸中溶质的质量分数
滤液.求稀盐酸中溶质的质量分数
您最近一年使用:0次