国产C919大型客机装有铜镁合金材质的天线。测定某铜镁合金(不含其他成分)中镁的含量,称取铜镁合金样品10g放入烧杯,将100g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下表。
请计算:
(1)表中m=______ g,该铜镁合金样品中镁的质量分数=________ 。
(2)所加稀硫酸中溶质的质量分数。(请写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 25 | 25 | 25 | 25 |
| 剩余固体质量/g | 8.8 | m | 6.6 | 6.6 |
请计算:
(1)表中m=
(2)所加稀硫酸中溶质的质量分数。(请写出计算过程)
更新时间:2022-06-24 12:12:55
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在进行某探究实验时,小芳将98克氯酸钾和二氧化锰的混合物在酒精灯下充分加热后,然后将其在室温下冷却,称量得到剩余的粉末的质量为69.2克。
(1)生成氧气_______ 克;
(2)请问98克氯酸钾和二氧化锰的混合物中氯酸钾多少克?
(1)生成氧气
(2)请问98克氯酸钾和二氧化锰的混合物中氯酸钾多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】贝壳的主要成分是碳酸钙。为了测定某贝壳中碳酸钙的质量分数,小林同学进行了如下实验:将贝壳洗净、干燥并捣碎后,称取12 g 放在烧杯里,然后往烧杯中加入足量的稀盐酸45 g,充分反应后,称得反应剩余物为52.6 g。(假设其他物质不与盐酸反应)
(1)产生二氧化碳气体________g。
(2)计算该贝壳中碳酸钙的质量分数______。
(1)产生二氧化碳气体________g。
(2)计算该贝壳中碳酸钙的质量分数______。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氢化钙(CaH2)是一种常用的储氢材料,其与水反应方程式为:CaH2+2H2O=Ca(OH)2+2H2↑。某化学兴趣小组为了测定氢化钙样品中含CaH2的质量,设计了如下实验:将50g氢化钙样品加入50g水中充分反应(已知氢化钙样品中杂质不参与反应),最终得到剩余物质总质量为96g。计算:
(1)上述实验中生成氢气质量为______ g。
(2)氢化钙样品中含CaH2的质量为多少?
(1)上述实验中生成氢气质量为
(2)氢化钙样品中含CaH2的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】2010年全国人大和政协会议使用了一种含碳酸钙的“石头纸”:为测定其中碳酸钙的含量,课外活动小组的同学称取50g碎纸样品。分别在5只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水反应):
(1)表中X的值为 ;
(2)碳酸钙恰好完全反应时消耗稀盐酸 g;
(3)求样品中碳酸钙的质量分数为多少?
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | X | 3.52 | 3.52 |
(2)碳酸钙恰好完全反应时消耗稀盐酸 g;
(3)求样品中碳酸钙的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为了测定某品牌食用碱(主要成分为碳酸钠,含少量氯化钠杂质)中碳酸钠的质量分数。化学兴趣小组的同学将10.0g食用碱样品加到盛有90.0g水的烧杯中,完全溶解后,往其中逐次滴加溶质质量分数相同的氯化钙溶液,实验数据如下表所示:
请计算:
(1)反应生成沉淀的总质量为______ g。
(2)该品牌食用碱中碳酸钠的质量分数。(写出计算过程)
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入CaCl2溶液的质量/g | 20.0 | 20.0 | 20.0 | 20.0 | 20.0 |
| 反应后溶液的总质量/g | 118.0 | 136.0 | 154.0 | 172.0 | 192.0 |
(1)反应生成沉淀的总质量为
(2)该品牌食用碱中碳酸钠的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】将氯化钠和碳酸钠组成的固体混合物18.9克完全溶解于196.8克水中,向该溶液中 加入一定质量的氯化钡溶液恰好完全反应,滤出19.7克沉淀。若将滤液蒸发100克水后,所得溶液溶质质量分数为10%。
计算:(1)蒸发水后所得溶液的质量。
(2)所用氯化钡溶液中溶质的质量分数。
计算:(1)蒸发水后所得溶液的质量。
(2)所用氯化钡溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某纯碱样品中含有少量氯化钠杂质,称取该样品25g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和氯化钠溶液,反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示,计算:
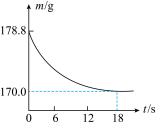
(1)生成二氧化碳的质量
(2)样品中碳酸钠的质量分数

(1)生成二氧化碳的质量
(2)样品中碳酸钠的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】取2g氧化铜固体于烧杯中,向其中加入78g的稀硫酸,恰好完全反应。请计算:所得溶液中溶质的质量分数______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某学习小组同学取一定量木炭粉与氧化镁的固体混合物放入烧杯中,加入200g稀硫酸,恰好完全反应,烧杯中固体的质量随时间变化情况如图所示。请完成下列分析及计算:
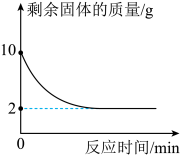
(1)混合物中木炭粉的质量为__________ g。
(2)计算所用稀硫酸的溶质质量分数。

(1)混合物中木炭粉的质量为
(2)计算所用稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某样品为铜和氧化铜的混合物。为测定其中氧化铜的质量分数,取 此样品,将
此样品,将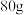 稀硫酸分四次加入样品中;每次充分反应后经过滤、洗涤、干燥等操作后称量剩余固体的质量,所得数据见表:
稀硫酸分四次加入样品中;每次充分反应后经过滤、洗涤、干燥等操作后称量剩余固体的质量,所得数据见表:
回答:
(1)表中n的数值为_______ 。
(2)样品中氧化铜的质量分数是_______ 。
(3)计算稀硫酸的溶质质量分数是多少?
 此样品,将
此样品,将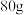 稀硫酸分四次加入样品中;每次充分反应后经过滤、洗涤、干燥等操作后称量剩余固体的质量,所得数据见表:
稀硫酸分四次加入样品中;每次充分反应后经过滤、洗涤、干燥等操作后称量剩余固体的质量,所得数据见表:| 序号 | 加入稀硫酸的质量 | 剩余固体的质量 |
| 第1次 | 20 | 16 |
| 第2次 | 20 | 12 |
| 第3次 | 20 | 8.5 |
| 第4次 | 20 | n |
(1)表中n的数值为
(2)样品中氧化铜的质量分数是
(3)计算稀硫酸的溶质质量分数是多少?
您最近一年使用:0次



