纯碱是一种重要的化工原料,广泛用于玻璃、造纸、纺织和洗涤剂的生产。某化学兴趣小组对纯碱的制备、性质及用途等开展项目式学习。
任务一 了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)纯碱属于______ (填“酸”“碱”或“盐”)。
(2)饱和氯化钠溶液吸收的两种气体是______ (填字母序号)。
A.Cl2 B.NH3 C.SO2 D.CO2
任务二 探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和 。
。
③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性。
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三:______ 。
【实验探究】
【解释与结论】同学们和老师交流,得知 和H2O作用,产生较多的OH-和另一种阴离子。
和H2O作用,产生较多的OH-和另一种阴离子。
【拓展与延伸】结合任务二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是______ 。
任务三 探究纯碱的用途——用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如下表:
【解释与结论】(1)实验①、②、③对比,可得出的结论是______ 。
(2)要证明Na2CO3溶液的溶质质量分数变化与pH变化关系,可选择的3个实验的编号是______ 。
【拓展与应用】下列物质可用于去油污的是______ (填字母序号)。
A.NaCl B.NaOH C.K2CO3 D.CaCO3
任务一 了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”主要化学原理是利用饱和氯化钠溶液吸收两种气体,生成碳酸氢钠和氯化铵(NH4Cl),再加热碳酸氢钠即可制得纯碱。
(1)纯碱属于
(2)饱和氯化钠溶液吸收的两种气体是
A.Cl2 B.NH3 C.SO2 D.CO2
任务二 探究纯碱的性质——Na2CO3溶液呈碱性
【查阅资料】①溶液呈碱性,是因为溶液中存在较多的OH-。
②Na2CO3在水中全部解离出Na+和
 。
。③CaCl2溶液呈中性,Ca2+、Cl-对溶液的酸碱性没有影响。
【提出猜想】猜想一:H2O单独起作用,产生较多的OH-,使溶液呈碱性。
猜想二:Na+与H2O作用,产生较多的OH-,使溶液呈碱性。
猜想三:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| (1)向试管中加入一定量的蒸馏水,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想一不成立 |
| (2)向试管中加入一定量的NaCl溶液,滴入2滴酚酞溶液 | 溶液无明显变化 | 猜想二不成立 |
| (3)①向试管中加入一定量的Na2CO3溶液,滴入2滴酚酞溶液 ②往①所得溶液中逐滴加入CaCl2溶液至过量 | ①溶液由红色变无色 ② | 猜想三成立 |
 和H2O作用,产生较多的OH-和另一种阴离子。
和H2O作用,产生较多的OH-和另一种阴离子。【拓展与延伸】结合任务二的所有信息和结论,运用初中化学所学知识,经过分析推理可得出:Na2CO3溶液中含有的阴离子是
任务三 探究纯碱的用途——用于生产洗涤剂
【查阅资料】Na2CO3可用于生产洗涤剂。Na2CO3溶液呈碱性,可清洗油污,溶液碱性越强,去油污效果越好。
【实验探究】兴趣小组继续对影响Na2CO3溶液去油污效果的因素进行探究。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的Na2CO3溶液,并测定溶液pH,记录数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
| 溶液温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
(2)要证明Na2CO3溶液的溶质质量分数变化与pH变化关系,可选择的3个实验的编号是
【拓展与应用】下列物质可用于去油污的是
A.NaCl B.NaOH C.K2CO3 D.CaCO3
2022·广西·中考真题 查看更多[9]
2022年广西北部湾经济区中考化学真题2023年广西初中学业水平考试化学参考样卷(已下线)考点09 盐和化肥-备战2023年中考化学一轮复习考点帮(全国通用)(已下线)第十一单元 盐 化肥-2022-2023学年九年级化学下册单元检测真题卷(人教版)2023年广西柳州市柳南区壶西实验中学中考模拟化学试题(已下线)第11讲 盐、化肥-备战2023年中考化学一轮复习考点帮(广东专用)2023年广西玉林市兴业县北市镇第二初级中学中考模拟化学试题(已下线)2023年中考押题预测卷01(深圳卷)-化学(已下线)2024年中考风向标-广西-科学探究题
更新时间:2022-06-29 10:34:44
|
相似题推荐
科学探究题
|
困难
(0.15)
解题方法
【推荐1】初中化学课上,同学们利用下列实验探究碱的化学性质:
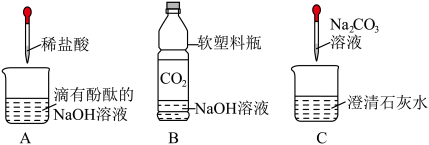
(1)A实验中反应的化学方程式为_____ 。(2)C实验中观察到的现象是 _____ 。
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有_____ 。
老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言:
【实验验证】 同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。
【结论】上述滤液中,还含有____ ,没有 _____ 。

(1)A实验中反应的化学方程式为
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有
老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言:
| 学生甲 | 可能有Ca(OH)2、NaOH | 学生丙 | 可能有Ca(OH)2、CaCl2 |
| 学生乙 | 可能有NaOH、Na2CO3 | 学生丁 | 可能有Na2CO3 |
| 学生戊 | 可能有NaOH | …… | ………… |
【结论】上述滤液中,还含有
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐2】某校甲、乙兴趣小组的同学在“探究纯碱的性质”实验中,分别做了下图所示的四组实验,并将四支试管中的所有物质分别倒入洁净的A、B烧杯中。实验结束后,甲、乙小组同学都观察到烧杯底部有固体不溶物,上层溶液呈红色。
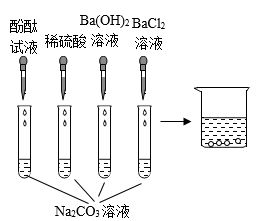
【提出问题】烧杯中的上层溶液的溶质除酚酞外,还含有哪些?
【猜想假设】溶质可能为NaCl、NaOH、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种。分析实验过程以及可能发生的化学反应方程式可知,溶质中一定含有的一种物质是_______ 。
小明同学猜想溶液中的溶质一定含有NaOH和Ba(OH)2中的至少一种。小红同学认为小明同学的猜想是错误的,理由是_______ 。
【查阅资料】
1 HNO3与Na2CO3反应是分步进行的: (先),
(先),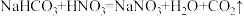 (后),而且NaHCO3的溶解性明显小于Na2CO3。
(后),而且NaHCO3的溶解性明显小于Na2CO3。
2 BaC12溶液呈中性。
【实验探究】
甲组同学:往A烧杯中逐滴滴入稀HNO3,一段时间后,才观察到有气泡产生,溶液变无色。烧杯中固体不溶物的质量,随滴入稀HNO3的质量变化关系如图所示。由此进一步得出溶液中的溶质还含有__ ,一定不含有_______ 和_______ 。

乙组同学:在甲组同学完成实验的基础上,乙组同学进行如下实验:
【学会计算】
甲组同学所做实验中减少的固体前后质量差为9.85克,则反应产生的CO2的质量为_____ g。

【提出问题】烧杯中的上层溶液的溶质除酚酞外,还含有哪些?
【猜想假设】溶质可能为NaCl、NaOH、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种。分析实验过程以及可能发生的化学反应方程式可知,溶质中一定含有的一种物质是
小明同学猜想溶液中的溶质一定含有NaOH和Ba(OH)2中的至少一种。小红同学认为小明同学的猜想是错误的,理由是
【查阅资料】
1 HNO3与Na2CO3反应是分步进行的:
 (先),
(先),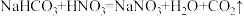 (后),而且NaHCO3的溶解性明显小于Na2CO3。
(后),而且NaHCO3的溶解性明显小于Na2CO3。2 BaC12溶液呈中性。
【实验探究】
甲组同学:往A烧杯中逐滴滴入稀HNO3,一段时间后,才观察到有气泡产生,溶液变无色。烧杯中固体不溶物的质量,随滴入稀HNO3的质量变化关系如图所示。由此进一步得出溶液中的溶质还含有

乙组同学:在甲组同学完成实验的基础上,乙组同学进行如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取B烧杯中的少量溶液于试管中,滴入足量的BaCl2溶液 | 生成白色沉淀, | 溶液中的溶质是酚酞、NaCl、NaOH、Na2CO3 |
| 继续往上述试管中滴入足量的稀HNO3 | 产生少量气泡,白色沉淀部分溶解,溶液变为无色 | 溶液中的溶质是酚酞、NaCl、NaOH、Na2CO3和 |
【学会计算】
甲组同学所做实验中减少的固体前后质量差为9.85克,则反应产生的CO2的质量为
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐3】小丽家里的下水道被毛发、食物残渣等杂物堵塞了,她爸爸买了一瓶管道通回来,经过短时间的浸泡使用,堵塞的下水道很快就疏通了。管道通是怎样使堵塞的下水道重新疏通呢?小丽产生了强烈的好奇,决定与化学兴趣小组的同学对管道通的成分及性质进行研究。

【查阅资料】
1、管道疏通剂的说明书,疏通剂的主要成分是NaOH固体与Al粉
2、NaOH溶液会与Al发生反应生成NaAlO2
【实验模拟】
在实验室里,小丽取出了一些NaOH固体和Al粉混合后,放入盛有水的试管中,观察到反应剧烈,有大量气泡产生,且试管壁发烫。对于壁发烫的原因,学习小组的同学认为可能是______ 的原因,也可能是______ 的原因。
【猜想与假设】
产生的气泡可能是什么气体?同学们纷纷提出了自己的猜想:
1、小李认为该气体是氧气;小张认为是氢气。
2、你认为该气体可能是______ 。
【验证假设】
1、小丽设计了如图所示装置进行实验。
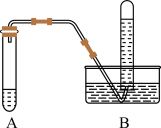
该气体的收集方法叫______ 。
2、小李拿一根带火星的小木条伸到集满气体的B试管中,观察到小木条______ ,
证明他的假设不正确。而现在发现B试管中的气体能被点燃,产生淡蓝色的火焰,该实验现象证明了小张的猜想是正确的。经实验确定A试管中反应后只有NaAlO2一种溶质,写出A试管中反应的化学方程式:______ 。
【原理分析】
对于Al为什么能与氢氧化钠溶液反应生成氢气的原因,大家进一步提出自己的猜想。
小李认为,Al的金属活动性排在H之前,所以置换出NaOH中的“H”。但他的观点遭到大家的反对,因为______ 。
小丽猜想是Al的性质比较特殊的原因,经过网络查找,大家终于弄明白了疏通反应的原理,进一步丰富了自己的化学知识。
【交流反思】
根据上述实验及NaOH的性质,请你提出一条保管或安全使用管道疏通剂的建议:______ 。
【定量分析】

小王在瓶子上发现了这瓶管道疏通剂的标签,于是他们开始了定量研究,他们向烧杯中加入206g水,再加入本品200g。当铝粉全部反应后,求反应后所得溶液中氢氧化钠的质量分数______ 。

【查阅资料】
1、管道疏通剂的说明书,疏通剂的主要成分是NaOH固体与Al粉
2、NaOH溶液会与Al发生反应生成NaAlO2
【实验模拟】
在实验室里,小丽取出了一些NaOH固体和Al粉混合后,放入盛有水的试管中,观察到反应剧烈,有大量气泡产生,且试管壁发烫。对于壁发烫的原因,学习小组的同学认为可能是
【猜想与假设】
产生的气泡可能是什么气体?同学们纷纷提出了自己的猜想:
1、小李认为该气体是氧气;小张认为是氢气。
2、你认为该气体可能是
【验证假设】
1、小丽设计了如图所示装置进行实验。

该气体的收集方法叫
2、小李拿一根带火星的小木条伸到集满气体的B试管中,观察到小木条
证明他的假设不正确。而现在发现B试管中的气体能被点燃,产生淡蓝色的火焰,该实验现象证明了小张的猜想是正确的。经实验确定A试管中反应后只有NaAlO2一种溶质,写出A试管中反应的化学方程式:
【原理分析】
对于Al为什么能与氢氧化钠溶液反应生成氢气的原因,大家进一步提出自己的猜想。
小李认为,Al的金属活动性排在H之前,所以置换出NaOH中的“H”。但他的观点遭到大家的反对,因为
小丽猜想是Al的性质比较特殊的原因,经过网络查找,大家终于弄明白了疏通反应的原理,进一步丰富了自己的化学知识。
【交流反思】
根据上述实验及NaOH的性质,请你提出一条保管或安全使用管道疏通剂的建议:
【定量分析】

小王在瓶子上发现了这瓶管道疏通剂的标签,于是他们开始了定量研究,他们向烧杯中加入206g水,再加入本品200g。当铝粉全部反应后,求反应后所得溶液中氢氧化钠的质量分数
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐1】馒头制作时常加入泡打粉,由于产生二氧化碳气体,使馒头变得松软可口。化学活动课上同学们对泡打粉进行了以下实验探究。
【查阅资料】1、泡打粉又称为发泡粉,某种泡打粉的主要成分是小苏打。
2、碳酸氢钠受热分解为碳酸钠、二氧化碳和水;碳酸钠受热不分解。
【实验探究1】(1)将发泡粉加水溶解,取上层清液,用PH试纸测得其溶液的PH约为11,由此得出的结论是溶液呈______ (填“酸性”或“碱性”)。
【实验探究2】将200g淀粉、等量的水与不同质量的碳酸氢钠混合均匀制成面团进行发酵
【问题与结论】(2)要通过实验③④对比面团发酵程度与碳酸氢钠的质量有关,实验中x=______ ;分析可知碳酸氢钠质量一定时,面团发酵程度与温度的关系是______
【实验探究3】在如图装置的a试管中放碳酸氢钠固体,用酒精灯加热。
【实验现象】a试管固体有剩余,试管口内壁有无色液滴产生,b试管中澄清石灰水变浑浊。

【实验结论】(3)a试管中发生的化学方程式为______
【继续探究】同学们为了确定a试管中剩余白色固体的成分,作出了以下猜想:
猜想①:固体是Na2CO3
猜想②:固体是Na2CO3和NaHCO3的混合物
(4)称量1.68ga试管中剩余白色固体与足量稀盐酸反应,生成mgCO2,当m的取值范围______ ,则猜想②正确。
【拓展延伸】用如图装置分别向等量的碳酸钠和碳酸氢钠固体中逐滴滴加等体积、等浓度的足量稀盐酸进行实验时,实验现象如下:。
CO2:右侧烧杯中开始无气泡,后有气泡产生。
CO2:右侧烧杯中一开始就有气泡产生。
通过数字传感器测得CO2的体积如图:

(5)分析实验现象可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳更快,你判断的理由是______ 。
(6)碳酸钠与稀盐酸反应开始无气泡的化学方程式是______ 。
【查阅资料】1、泡打粉又称为发泡粉,某种泡打粉的主要成分是小苏打。
2、碳酸氢钠受热分解为碳酸钠、二氧化碳和水;碳酸钠受热不分解。
【实验探究1】(1)将发泡粉加水溶解,取上层清液,用PH试纸测得其溶液的PH约为11,由此得出的结论是溶液呈
【实验探究2】将200g淀粉、等量的水与不同质量的碳酸氢钠混合均匀制成面团进行发酵
| 实验方案 | 温度/0C | 碳酸氢钠的质量/g | 现象 |
| ① | 30 | 0.2 | 60分钟面团开始变得松软 |
| ② | 30 | 0.3 | 45分钟面团开始变得松软 |
| ③ | 40 | 0.2 | 30分钟面团开始变得松软 |
| ④ | x | 0.3 | 20分钟面团开始变得松软 |
【实验探究3】在如图装置的a试管中放碳酸氢钠固体,用酒精灯加热。
【实验现象】a试管固体有剩余,试管口内壁有无色液滴产生,b试管中澄清石灰水变浑浊。

【实验结论】(3)a试管中发生的化学方程式为
【继续探究】同学们为了确定a试管中剩余白色固体的成分,作出了以下猜想:
猜想①:固体是Na2CO3
猜想②:固体是Na2CO3和NaHCO3的混合物
(4)称量1.68ga试管中剩余白色固体与足量稀盐酸反应,生成mgCO2,当m的取值范围
【拓展延伸】用如图装置分别向等量的碳酸钠和碳酸氢钠固体中逐滴滴加等体积、等浓度的足量稀盐酸进行实验时,实验现象如下:。
CO2:右侧烧杯中开始无气泡,后有气泡产生。
CO2:右侧烧杯中一开始就有气泡产生。
通过数字传感器测得CO2的体积如图:

(5)分析实验现象可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳更快,你判断的理由是
(6)碳酸钠与稀盐酸反应开始无气泡的化学方程式是
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐2】同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究。
【查阅资料】
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显__________ 色;
酸碱度:NaHCO3溶液___________ Na2CO3溶液(填“>”或”“<”)。
(2)稳定性:按下图,实验中可观察乙烧杯中的石灰水变浑浊,甲烧杯不变,则乙烧杯对应的试管中发生反应的化学方程式为:___________ 。
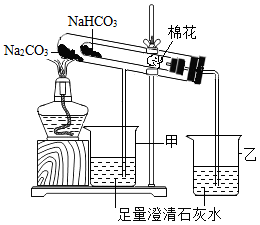
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性___________ (填“强”或“弱”)。
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的__________ 。(选填A、B或C)
A.1.5g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先__________ (选填A或B)A.熄灭酒精灯 B.把甲、乙烧杯移开
(5)小试管内棉花的作用是_____________
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(下图,夹持装置略)
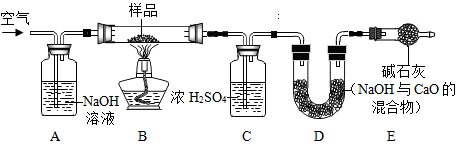
【问题讨论】
(6)实验前先通一段时间的空气的目的是________ ;
(7)A的作用是____________ ,若没有装置E,NaHCO3的质量分数测定结果会_____________ (填“偏大”、“不变”或“偏小”)。
(8)停止加热后,仍继续通入空气一段时间,目的是_____________ 。
【含量测定】
(9)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数。(要有计算过程)_______ 。
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:_____________ 。
【查阅资料】
20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显
酸碱度:NaHCO3溶液
(2)稳定性:按下图,实验中可观察乙烧杯中的石灰水变浑浊,甲烧杯不变,则乙烧杯对应的试管中发生反应的化学方程式为:

结论:在受热条件下,碳酸钠比碳酸氢钠稳定性
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的
A.1.5g B.0.96g C.0.5g
【问题讨论】
(4)实验结束时,应先
(5)小试管内棉花的作用是
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(下图,夹持装置略)

【问题讨论】
(6)实验前先通一段时间的空气的目的是
(7)A的作用是
(8)停止加热后,仍继续通入空气一段时间,目的是
【含量测定】
(9)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数。(要有计算过程)
【知识拓展】
(10)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为:
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐3】在学习盐酸的化学性质时,甲、乙两位同学分别做了稀盐酸和碳酸钠溶液反应的实验(如图1)。

【实验现象】甲同学的实验中溶液有气泡冒出,乙同学的实验中溶液基本无气泡冒出。
【提出问题】乙同学的实验中溶液为什么没有气泡冒出?
【查阅资料】①碳酸钠溶液中滴加少量稀盐酸无气泡,能生成碳酸氢钠和另一种盐
②碳酸氢钠溶液pH约为9.2
【进行实验】同学们设计并进行了如图2所示的实验(装置气密性良好),填入所缺实验现象
(1)边注入边振荡的作用是_________ 。
(2)实验①中细玻璃管中液柱略微升高可能的原因是_________ 。
【实验探究】向一定体积pH=12的碳酸钠溶液中加稀盐酸,在老师的帮助下,同学们利用pH传感器记录反应过程中溶液pH与加入稀盐酸体积的关系,如图3所示:
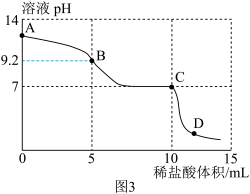
(3)图3中D点溶液中溶质有_______________ 。
(4)分析图表可知,碳酸钠与稀盐酸反应分两步进行:
AB段反应的化学方程式为:_________ 。
BC段反应的化学方程式为: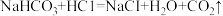
【定量分析】
(5)取10克碳酸钠溶液,逐渐滴加溶质质量分数为7.3%的稀盐酸至5mL(密度约1g/mL)后产生气泡,试计算碳酸钠溶液中Na2CO3的质量为_________ g。
【实验反思】
(6)此反应说明反应物的量不同,产物可能不同,试另举一例:________ 。

【实验现象】甲同学的实验中溶液有气泡冒出,乙同学的实验中溶液基本无气泡冒出。
【提出问题】乙同学的实验中溶液为什么没有气泡冒出?
【查阅资料】①碳酸钠溶液中滴加少量稀盐酸无气泡,能生成碳酸氢钠和另一种盐
②碳酸氢钠溶液pH约为9.2
【进行实验】同学们设计并进行了如图2所示的实验(装置气密性良好),填入所缺实验现象
| 实验编号 | 实验步骤 | 实验现象 |
| ① | 1、用注射器1向小药瓶中缓慢注入少量的稀盐酸,边注入边振荡 | 细玻璃管中液柱略微升高无气泡产生 |
| Ⅱ、换注射器2从瓶中缓慢抽取气体 | 澄清石灰水不变浑浊 | |
| ② | 1、用注射器1向小药瓶中继续注入稀盐酸至较多气泡产生 | 细玻璃管中液柱 |
| Ⅱ、换注射器2从瓶中缓慢抽取气体 | 澄清石灰水变浑浊 |
(2)实验①中细玻璃管中液柱略微升高可能的原因是
【实验探究】向一定体积pH=12的碳酸钠溶液中加稀盐酸,在老师的帮助下,同学们利用pH传感器记录反应过程中溶液pH与加入稀盐酸体积的关系,如图3所示:

(3)图3中D点溶液中溶质有
(4)分析图表可知,碳酸钠与稀盐酸反应分两步进行:
AB段反应的化学方程式为:
BC段反应的化学方程式为:
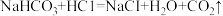
【定量分析】
(5)取10克碳酸钠溶液,逐渐滴加溶质质量分数为7.3%的稀盐酸至5mL(密度约1g/mL)后产生气泡,试计算碳酸钠溶液中Na2CO3的质量为
【实验反思】
(6)此反应说明反应物的量不同,产物可能不同,试另举一例:
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐1】小苏打和食盐是厨房中常见物质,现有一包白色固体,可能由碳酸氢钠、氯化钠中的一种或两种物质组成。某化学兴趣小组的同学展开了系列研究。

(一)定性分析
【实验目的】确定白色固体的组成
【实验方案】如图1所示:
【实验结论】小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤②发生反应的化学方程式是___________ ;
(2)兴趣小组同学认真研究讨论后认为,此方案不能得出小明同学的结论。理由是____________ (用化学方程式表示)。
(二)定量分析
【实验目的】测定该白色固体中碳酸氢钠的质量分数。
【实验方案】该小组利用如图2所示的实验装置(固定装置已略去,装置气密性良好)进行实验,每一步反应均完全进行。
(1)首先称取8g该样品放入装置甲中,然后进行有关实验操作,正确的顺序是___________ (填序号,可重复选择);
a.称量装置丙的质量
b.打开弹簧夹,通入足量的氮气,关闭弹簧夹
c.打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞
(2)装置乙中的浓硫酸具有___________ (填“吸水性”或“酸性”),可以干燥产生的气体;
(3)装置丁的作用是____________ ;
(4)在所有操作、实验步骤均正确的前提下,若测得丙装置的质量增加2.2克,则该白色固体中碳酸氢钠的质量分数为____________ 。
(三) 拓展延伸: 兴趣小组将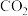 持续通入一定浓度一定量的
持续通入一定浓度一定量的 溶液中, 用数字化实 验技术测定反应过程中溶液的
溶液中, 用数字化实 验技术测定反应过程中溶液的 和温度变化, 结果如图 3、图 4 所示。
和温度变化, 结果如图 3、图 4 所示。
已知: 本实验条件下, 溶液和
溶液和 溶液的
溶液的 分别约为
分别约为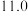 和 8. 5. 则:
和 8. 5. 则:
(1)图 3 中,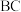 段发生反应的化学方程式为
段发生反应的化学方程式为__________ 。
(2)图 4 中, DE 段温度变化的原因是__________ 。

(一)定性分析
【实验目的】确定白色固体的组成
【实验方案】如图1所示:
【实验结论】小明同学经过上述实验得出结论:该白色固体由碳酸氢钠、氯化钠两种物质组成。
(1)步骤②发生反应的化学方程式是
(2)兴趣小组同学认真研究讨论后认为,此方案不能得出小明同学的结论。理由是
(二)定量分析
【实验目的】测定该白色固体中碳酸氢钠的质量分数。
【实验方案】该小组利用如图2所示的实验装置(固定装置已略去,装置气密性良好)进行实验,每一步反应均完全进行。
(1)首先称取8g该样品放入装置甲中,然后进行有关实验操作,正确的顺序是
a.称量装置丙的质量
b.打开弹簧夹,通入足量的氮气,关闭弹簧夹
c.打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞
(2)装置乙中的浓硫酸具有
(3)装置丁的作用是
(4)在所有操作、实验步骤均正确的前提下,若测得丙装置的质量增加2.2克,则该白色固体中碳酸氢钠的质量分数为
(三) 拓展延伸: 兴趣小组将
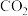 持续通入一定浓度一定量的
持续通入一定浓度一定量的 溶液中, 用数字化实 验技术测定反应过程中溶液的
溶液中, 用数字化实 验技术测定反应过程中溶液的 和温度变化, 结果如图 3、图 4 所示。
和温度变化, 结果如图 3、图 4 所示。已知: 本实验条件下,
 溶液和
溶液和 溶液的
溶液的 分别约为
分别约为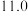 和 8. 5. 则:
和 8. 5. 则:(1)图 3 中,
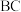 段发生反应的化学方程式为
段发生反应的化学方程式为(2)图 4 中, DE 段温度变化的原因是
您最近一年使用:0次
科学探究题
|
困难
(0.15)
真题
解题方法
【推荐2】2021年12月9日“天宫课堂”开讲,航天员王亚平带来了有趣的“太空泡腾片实验”,地面上的同学同步做了对照实验并进行了如下拓展探究。
【查阅资料】某品牌维生素C泡腾片的主要成分:维生素
辅料:碳酸钠、碳酸钙、碳酸氢钠、蔗糖、柠檬酸、橙味香料等
该泡腾片中含有的营养素除了_______ 外,还含有糖类、无机盐等。
【对照实验】同学们将该泡腾片放入盛有水的烧杯中,观察到与太空中相似的实验现象:有大量气泡产生,同时闻到橙汁香味。从分子的角度解释能闻到橙汁香味的原因,_______ 。
拓展深究一:探究气泡中气体成分,
【提出猜想】该气泡中可能含有CO2.猜想依据是_________ 。
【设计实验】
拓展探究二:探究该泡腾片中二氧化碳源的质量分数ω范围(二氧化碳源是指与酸反应能产生二氧化碳的物质)。
【设计实验】利用下图装置进行探究(装置气密性良好;固定装置已略去;碱石灰是氢氧化钠和生石灰的混合物),步骤如下:Ⅰ.称取10.00g该泡腾片粉末装入烧瓶中,松开弹簧夹K,通入一段时间空气;Ⅱ.称量装置D质量为220.00g,夹上弹簧夹K,滴加足量的稀硫酸;Ⅲ.松开弹簧夹,再通入一段时间空气;Ⅳ.称量装置D质量为220.88g。

【讨论解释】步骤Ⅲ中通入空气的目的是________ 。
【实验结论】该泡腾片中二氧化碳源的质量分数ω范围是_______ 。
【查阅资料】某品牌维生素C泡腾片的主要成分:维生素
辅料:碳酸钠、碳酸钙、碳酸氢钠、蔗糖、柠檬酸、橙味香料等
该泡腾片中含有的营养素除了
【对照实验】同学们将该泡腾片放入盛有水的烧杯中,观察到与太空中相似的实验现象:有大量气泡产生,同时闻到橙汁香味。从分子的角度解释能闻到橙汁香味的原因,
拓展深究一:探究气泡中气体成分,
【提出猜想】该气泡中可能含有CO2.猜想依据是
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 向盛有该泡腾片的试管中加入一定量的水,塞上带导管的橡皮塞,并将导管另一端通入装有澄清石灰水的试管中 | 气泡中含有CO2 |
【设计实验】利用下图装置进行探究(装置气密性良好;固定装置已略去;碱石灰是氢氧化钠和生石灰的混合物),步骤如下:Ⅰ.称取10.00g该泡腾片粉末装入烧瓶中,松开弹簧夹K,通入一段时间空气;Ⅱ.称量装置D质量为220.00g,夹上弹簧夹K,滴加足量的稀硫酸;Ⅲ.松开弹簧夹,再通入一段时间空气;Ⅳ.称量装置D质量为220.88g。

【讨论解释】步骤Ⅲ中通入空气的目的是
【实验结论】该泡腾片中二氧化碳源的质量分数ω范围是
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐3】已知Mg能在CO2中燃烧,根据金属活动性顺序表,Na的金属活动性比Mg强,说明也能在CO2中燃烧。为了验证,实验小组进行了以下实验探究:
【查阅资料】
①金属钠性质活泼,常温下,金属钠极易与氧气反应,生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。金属钠还可以与水剧烈反应,放出氢气。
②Na2CO3溶液显碱性;CaCl2溶液显中性。
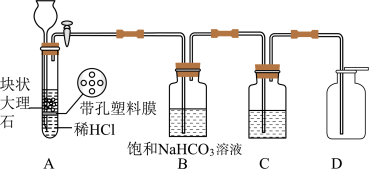
【实验探究一】
步骤1:打开活塞,让A装置中产生的气体依次通过B、C,收集一瓶纯净的CO2气体。
步骤2:将燃烧的钠迅速伸入集气瓶中,观察到钠在CO2中继续燃烧,发光放热,冷却后观察到瓶内附着黑色颗粒,并粘附着白色物质。
【问题讨论】
(1)步骤2中生成的黑色固体成分是碳。
【初步结论】Na能在CO2中燃烧。
【提出问题】白色物质是什么?
【猜想与假设】
猜想一:氧化钠:
猜想二:碳酸钠;
猜想三:氧化钠和碳酸钠的混合物;
猜想四:氢氧化钠。
(2)大家讨论后一致认为猜想四是错误的,理由是___________ 。
【实验探究二】对白色物质是什么进行实验探究,方案设计如下:
方案1:取该样品少量于试管中,加入适量的水。振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色。结论:白色物质中一定有氧化钠。
方案2:取该样品少量于试管中,滴加足量盐酸,溶液中有气泡冒出。
结论:白色物质中一定有___________ 。
方案3:取该样品少量于试管中,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液,出现白色沉淀,过滤,再向滤液中滴加无色酚酞溶液,无明显现象。
【反思与评价】
(3)甲同学思考后提出方案1得出的结论不正确,其理由是___________ 。
(4)方案3中加入过量CaC12溶液的目的是___________ 。
【实验结论】
(5)综上所述,你认为猜想___________ 成立。
(6)请写出Na在CO2中燃烧的化学方程式___________ 。
【查阅资料】
①金属钠性质活泼,常温下,金属钠极易与氧气反应,生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠。金属钠还可以与水剧烈反应,放出氢气。
②Na2CO3溶液显碱性;CaCl2溶液显中性。

【实验探究一】
步骤1:打开活塞,让A装置中产生的气体依次通过B、C,收集一瓶纯净的CO2气体。
步骤2:将燃烧的钠迅速伸入集气瓶中,观察到钠在CO2中继续燃烧,发光放热,冷却后观察到瓶内附着黑色颗粒,并粘附着白色物质。
【问题讨论】
(1)步骤2中生成的黑色固体成分是碳。
【初步结论】Na能在CO2中燃烧。
【提出问题】白色物质是什么?
【猜想与假设】
猜想一:氧化钠:
猜想二:碳酸钠;
猜想三:氧化钠和碳酸钠的混合物;
猜想四:氢氧化钠。
(2)大家讨论后一致认为猜想四是错误的,理由是
【实验探究二】对白色物质是什么进行实验探究,方案设计如下:
方案1:取该样品少量于试管中,加入适量的水。振荡,过滤,向滤液中加入无色酚酞试液,观察到溶液变成红色。结论:白色物质中一定有氧化钠。
方案2:取该样品少量于试管中,滴加足量盐酸,溶液中有气泡冒出。
结论:白色物质中一定有
方案3:取该样品少量于试管中,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液,出现白色沉淀,过滤,再向滤液中滴加无色酚酞溶液,无明显现象。
【反思与评价】
(3)甲同学思考后提出方案1得出的结论不正确,其理由是
(4)方案3中加入过量CaC12溶液的目的是
【实验结论】
(5)综上所述,你认为猜想
(6)请写出Na在CO2中燃烧的化学方程式
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
解题方法
【推荐1】化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀。
[提出问题]灰白色沉淀是什么?
[猜想假设]珊珊认为灰白色沉淀可能为碳酸镁,其他同学认为不需要实验就能否定珊珊的猜想,理由是_________ 。
月月认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。丹丹认为灰白色沉淀为脱落的镁粉细颗粒。
[探究实验 1]
基于以上探究与分析,原有猜想均遭到了否定。
[探究实验 2]她们又另取灰白色沉淀放入试管中加热,无明显现象,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了_______ 气体,再将湿润的蓝色石蕊试纸悬于试管口,试纸变_______ 色。
[实验结论]同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀。
[查阅资料]碱式氯化镁存在多种组成结构,化学式通式可表示为 Mgx(OH)yClz﹒mH2O (其中 2x-y-z=0,0≤m≤6)。
碱式氯化镁受热能分解,生成 MgO、 H2O 和上述气体。
[探究实验 3]为进一步确定碱式氯化镁的化学式,同学们进行了如下实验:
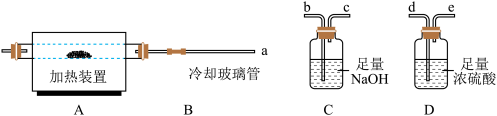
(1)若只通过测定装置 C、D 的增重来确定 m,则装置的连接顺序为 a→_______ (用接口处的小写字母表示)。
(2)图中冷却玻璃管B能降低气体的温度,但不能液化水蒸气。若取消冷却玻璃管B后进行实验,测定的m值将________ (填“偏大”、“偏小”或“不变”)。
(3)加热前先通入N2排尽装置中的空气,称取 C、D 的初始质量后,再持续通入N2,持续通入N2的原因是:
①_____________ ;
②______________ 。
(4)将 20.65g 的 Mgx(OH)yClz﹒mH2O 放在加热装置中充分加热,完全分解后测得装置 C、D 分别增重 3.65g 和 9g,则该碱式氯化镁的化学式为_________________ 。
[提出问题]灰白色沉淀是什么?
[猜想假设]珊珊认为灰白色沉淀可能为碳酸镁,其他同学认为不需要实验就能否定珊珊的猜想,理由是
月月认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。丹丹认为灰白色沉淀为脱落的镁粉细颗粒。
[探究实验 1]
| 实验操作 | 实验现象 | 实验结论 |
| ①取试管中的上层清液,加入适量的氯化镁固体 | 月月猜想错误 | |
| ②取适量的灰白色沉淀,加入 | 没有气泡冒出 | 丹丹猜想错误 |
[探究实验 2]她们又另取灰白色沉淀放入试管中加热,无明显现象,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了
[实验结论]同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀。
[查阅资料]碱式氯化镁存在多种组成结构,化学式通式可表示为 Mgx(OH)yClz﹒mH2O (其中 2x-y-z=0,0≤m≤6)。
碱式氯化镁受热能分解,生成 MgO、 H2O 和上述气体。
[探究实验 3]为进一步确定碱式氯化镁的化学式,同学们进行了如下实验:

(1)若只通过测定装置 C、D 的增重来确定 m,则装置的连接顺序为 a→
(2)图中冷却玻璃管B能降低气体的温度,但不能液化水蒸气。若取消冷却玻璃管B后进行实验,测定的m值将
(3)加热前先通入N2排尽装置中的空气,称取 C、D 的初始质量后,再持续通入N2,持续通入N2的原因是:
①
②
(4)将 20.65g 的 Mgx(OH)yClz﹒mH2O 放在加热装置中充分加热,完全分解后测得装置 C、D 分别增重 3.65g 和 9g,则该碱式氯化镁的化学式为
您最近一年使用:0次
科学探究题
|
困难
(0.15)
名校
【推荐2】兴趣小组的同学查出胃药碱式碳酸镁有多种不同的组成,如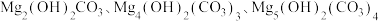 等,小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:
等,小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:

(1)实验步骤①按图组装置后,首先进行的操作是_____________ ;
实验步骤②称取样品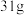 ,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为
,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为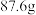 ,装碱石灰的U型管D的质量为
,装碱石灰的U型管D的质量为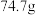 ;
;
(2)实验步骤③打开活塞__________ ,关闭__________ ,缓慢鼓入空气数分钟;
(3)实验步骤④关闭活塞________ ,打开_________ ,点燃酒精灯加热至不再产生气体为止;
(4)实验步骤⑤打开活塞 ,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为
,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为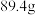 ,U型管D的质量为
,U型管D的质量为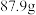 ,则该碱式碳酸镁的化学式为
,则该碱式碳酸镁的化学式为__________ ;
小明设计了两套方案(忽略装置中原来的气体)
(5)方案I只测定分解生成的 的质量,连接方案是
的质量,连接方案是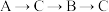 ,则B中的药品是
,则B中的药品是________ ,最后连接的C中的药品是____________ 。

方案Ⅱ:向一定质量的干燥样品中加入足量稀硫酸,通过测定产生 气体体积,装置如图2所示;
气体体积,装置如图2所示;
(6)为了减小实验误差,试分析量气装置中液体的选择原则____________ ,量气装置读数时应__________ (填序号),最后平视凹液面最低处读数;
①先使量气装置两侧液面相平,再恢复至室温
②先恢复至室温,再使量气装置两侧液面相平
(7)橡胶管a连接分液漏斗和锥形瓶,试推测橡胶管a的作用:__________ ,___________ ;
(8)反应后读数时,若量气装置右侧液面高于左侧(其它操作均正确),可能会导致测定的气体体积_____________ (填“偏大”或“偏小”)。
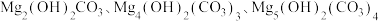 等,小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:
等,小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:
(1)实验步骤①按图组装置后,首先进行的操作是
实验步骤②称取样品
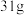 ,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为
,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为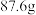 ,装碱石灰的U型管D的质量为
,装碱石灰的U型管D的质量为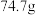 ;
;(2)实验步骤③打开活塞
(3)实验步骤④关闭活塞
(4)实验步骤⑤打开活塞
 ,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为
,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为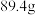 ,U型管D的质量为
,U型管D的质量为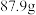 ,则该碱式碳酸镁的化学式为
,则该碱式碳酸镁的化学式为小明设计了两套方案(忽略装置中原来的气体)
(5)方案I只测定分解生成的
 的质量,连接方案是
的质量,连接方案是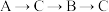 ,则B中的药品是
,则B中的药品是
方案Ⅱ:向一定质量的干燥样品中加入足量稀硫酸,通过测定产生
 气体体积,装置如图2所示;
气体体积,装置如图2所示;(6)为了减小实验误差,试分析量气装置中液体的选择原则
①先使量气装置两侧液面相平,再恢复至室温
②先恢复至室温,再使量气装置两侧液面相平
(7)橡胶管a连接分液漏斗和锥形瓶,试推测橡胶管a的作用:
(8)反应后读数时,若量气装置右侧液面高于左侧(其它操作均正确),可能会导致测定的气体体积
您最近一年使用:0次
科学探究题
|
困难
(0.15)
解题方法
【推荐3】某化学兴趣小组的同学在做氢氧化钙与稀盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
Ⅰ.定性探究
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
猜想Ⅰ:溶液中的溶质只有___________________
猜想Ⅱ:溶液中的溶质有CaCl2、HCl
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl
(1)请写出该反应的化学方程式_________________________ 。经过讨论,同学们直接得
出不合理的猜想是哪一种并说出理由_____________________________________ 。为了验
证余下的哪一种猜想是正确的,同学们又做了以下实验。
【进行实验】
(2)
(3)操作②有气泡生成的化学方程式为_________________________ 。
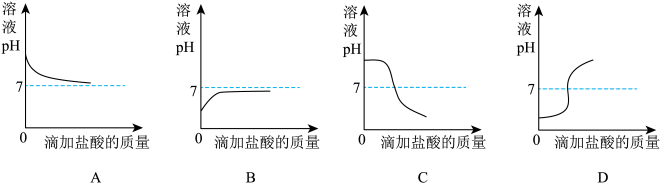
(4)下列曲线能够表示所做实验中溶液pH变化趋势的是________ (填序号)。
【反思交流】
(5)要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的_______________ ,然后过滤。
II.定量探究
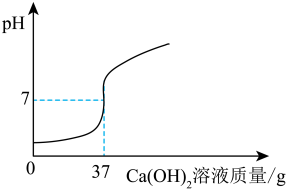
(6)兴趣小组同学想对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钙溶液进行中和,如下图所示.请你计算废水中盐酸的溶质质量分数__________ .(写出具体的计算过程 )
Ⅰ.定性探究
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
猜想Ⅰ:溶液中的溶质只有
猜想Ⅱ:溶液中的溶质有CaCl2、HCl
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl
(1)请写出该反应的化学方程式
出不合理的猜想是哪一种并说出理由
证余下的哪一种猜想是正确的,同学们又做了以下实验。
【进行实验】
(2)
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞溶液 | 猜想Ⅲ不正确 | |
| ②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钠 | 有气泡产生 | 猜想 猜想 |
(3)操作②有气泡生成的化学方程式为
(4)下列曲线能够表示所做实验中溶液pH变化趋势的是

【反思交流】
(5)要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的
II.定量探究
(6)兴趣小组同学想对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钙溶液进行中和,如下图所示.请你计算废水中盐酸的溶质质量分数

您最近一年使用:0次



