某化学兴趣小组测定假黄金(铜锌合金)的组成,称取 25g 假黄金置于烧杯中,用 80g 稀硫酸分 4 次加入,实验数据记录如下:
试分析并计算:
(1)25g 假黄金中锌的质量是______ g。
(2)当加入______ g 稀硫酸时,25g 假黄金中的锌恰好完全反应。
(3)求第二次实验后所得溶液的溶质质量分数。(精确到 0.01%)
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀硫酸的质量(g) | 20 | 20 | 20 | 20 |
| 残留金属的质量(g) | 21.75 | 18.5 | 15.25 | 15.25 |
(1)25g 假黄金中锌的质量是
(2)当加入
(3)求第二次实验后所得溶液的溶质质量分数。(精确到 0.01%)
更新时间:2022-06-29 18:21:46
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】化学小组为测定某硫酸铜溶液中溶质的质量分数,向等质量的两份氯化钡溶液中分别加入一定质量的硫酸铜溶液,充分反应后过滤,有关实验数据见下表。请计算:
(1)50g氯化钡溶液完全反应生成沉淀的质量是______ g;
(2)该硫酸铜溶液中溶质的质量分数。
| 氯化钡溶液质量/g | 50 | 50 |
| 硫酸铜溶液质量/g | 20 | 50 |
| 过滤后滤液质量/g | 67.67 | 95.34 |
(2)该硫酸铜溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】化学兴趣小组的同学用一瓶含有少量氯化钠和氯化钙的固体混合物进行下列实验:取样品14 g,放入烧杯中,加入96 g碳酸钠溶液恰好完全反应后过滤,称得滤液的总质量为100 g。

(1)根据质量守恒定律,可知生成沉淀的质量为___________________________。
(2)固体混合物中氯化钙的质量是___________?
(3)所得滤液中溶质的质量分数是__________?

(1)根据质量守恒定律,可知生成沉淀的质量为___________________________。
(2)固体混合物中氯化钙的质量是___________?
(3)所得滤液中溶质的质量分数是__________?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%-4.3%,钢中碳的含量为0.03%-2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示,注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为_________ g。
(2)通过计算判断样品是钢还是生铁____________ ?(计算结果保留到0%)
(3)反应后得到的溶液中溶质的质量分数____________ 。(计算结果保留到0.1%)
| 烧杯质量 | 样品的质量 | 稀盐酸的质量 | 烧杯+剩余物的总质量 |
| 50g | 5.8g | 94.6g | 150.2g |
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为
(2)通过计算判断样品是钢还是生铁
(3)反应后得到的溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐1】有一份铜锌合金粉末样品(设只含铜、锌),为认识其组成等,某学习小组进行了以下探究,请参与并完成有关计算:
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。该样品中铜的质量分数为______。
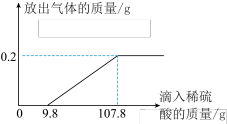
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。_______
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。该样品中铜的质量分数为______。
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
| 实验序号 | ① | ② | ③ |
| 样品的质量/g | 10 | 20 | 30 |
| 生成气体的质量/g | 0.1 | 0.2 | 0.25 |
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。_______
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】碳酸氢钠受热易分解,充分加热24.8g含碳酸钠的碳酸氢钠固体,完全反应后剩余固体的质量为18. 6g,则生成二氧化碳的质量为_____ g;将50g镁、锌的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐)。则反应产生氢气的质量是_____g。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐1】湿法冶金是我国古代劳动人民智慧的结晶.若向ag含杂质的铁粉中(假设杂质不溶于水,也不与其他物质反应)加入l60g溶质的质量分数为l0%的硫酸铜溶液,恰好完全反应后,过滤得到6.8g干燥固体,同时得到一种不饱和溶液(滤液损失忽略不计).
请回答下列问题:
(1)写出上述反应的化学方程式 ;
(2)根据硫酸铜质量列出求解样品中铁的质量(x)的比例式 ;
(3)a的数值为 ;
(4)若向反应后的滤液中加入40.8g水,则所得溶液中溶质的质量分数为 ;
(5)工业上若要得到120t上述铁粉,需要含杂质(杂质不含铁元素)20%的赤铁矿的质量是 .
请回答下列问题:
(1)写出上述反应的化学方程式 ;
(2)根据硫酸铜质量列出求解样品中铁的质量(x)的比例式 ;
(3)a的数值为 ;
(4)若向反应后的滤液中加入40.8g水,则所得溶液中溶质的质量分数为 ;
(5)工业上若要得到120t上述铁粉,需要含杂质(杂质不含铁元素)20%的赤铁矿的质量是 .
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】现有氢氧化镁和硫酸钡组成的固体混合物,某化学兴趣小组为确定其中硫酸钡的质量分数,将四等分混合物样品放入四个烧杯中,在分别加入一定量同浓度的稀盐酸进行4次实验,完全反应后测得数据如下表;
(1)表格中x的数值为
(2)该稀盐酸中溶质的质量分数为
(3)请分析实验数据,若将20g该固体样品中的Mg(OH)2,恰好完全反应,应加入该稀盐酸的质量为 ,求恰好完全反应后所得溶液中氯化镁的质量分数(保留到0.1%)
| 实验 | 第一组 | 第二组 | 第三组 | 第四组 |
| 固体样品质量/g | 20 | 20 | 20 | 20 |
| 稀盐酸质量/g | 40 | 80 | 120 | 160 |
| 剩余固体质量/g | 15.36 | 10.72 | x | 8.40 |
(1)表格中x的数值为
(2)该稀盐酸中溶质的质量分数为
(3)请分析实验数据,若将20g该固体样品中的Mg(OH)2,恰好完全反应,应加入该稀盐酸的质量为 ,求恰好完全反应后所得溶液中氯化镁的质量分数(保留到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为了测定某产品中碳酸钡的质量分数进行了如下实验。取一定量的样品和 溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录如下表: (假设反应匀速进行;称量时间间隔相等,杂质不溶于水,也不与稀盐酸反应,烧杯的质量为
溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录如下表: (假设反应匀速进行;称量时间间隔相等,杂质不溶于水,也不与稀盐酸反应,烧杯的质量为 )
)
请计算: (反应方程式为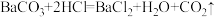 )
)
(1)表中的“ ”为____________;
”为____________;
(2)求该产品中碳酸钡的质量分数;
(3)当产品中碳酸钡与稀盐酸恰好完全反应时,求所得溶液中溶质的质量分数。
 溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录如下表: (假设反应匀速进行;称量时间间隔相等,杂质不溶于水,也不与稀盐酸反应,烧杯的质量为
溶质质量分数为10%的稀盐酸放入烧杯中。在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录如下表: (假设反应匀速进行;称量时间间隔相等,杂质不溶于水,也不与稀盐酸反应,烧杯的质量为 )
)请计算: (反应方程式为
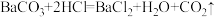 )
)| 反应时间 |  |  |  |  |  |
| 烧杯和药品质量/g | 516.6 | 507.8 | m | 503.4 | 503.4 |
(1)表中的“
 ”为____________;
”为____________;(2)求该产品中碳酸钡的质量分数;
(3)当产品中碳酸钡与稀盐酸恰好完全反应时,求所得溶液中溶质的质量分数。
您最近一年使用:0次