硫酸是化学实验室中常用的试剂,也是重要的化工原料,试回答下列问题:
(1)浓硫酸具有强烈的腐蚀性。如果不慎将浓硫酸沾到皮肤上,应立即用大量的水冲洗,然后涂上3%~5%的_______ (填化学式)溶液,以防灼伤皮肤。
(2)用硫单质制取硫酸的转化流程示意图如下:

在S、SO2、SO3、H2SO4四种物质中,硫元素的化合价表现为+4价的物质是_______ (填化学式)。写出上述转化流程步骤②中所发生反应的化学方程式_______ 。
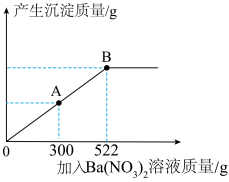
(3)现取100g稀硫酸倒入烧杯中,慢慢向烧杯中加入溶质质量分数为10%的Ba(NO3)2溶液,反应过程中产生沉淀的质量与所加入Ba(NO3)2溶液的质量关系如图所示。
试回答:
①当加入Ba(NO3)2溶液300g时(即图中A点),烧杯中溶液里大量存在的酸根离子是_______ (填离子符号)。
②当加入Ba(NO3)2溶液522g时(即图中B点),恰好完全反应,试通过计算求产生沉淀的总质量。(计算结果精确至0.1g)。
(1)浓硫酸具有强烈的腐蚀性。如果不慎将浓硫酸沾到皮肤上,应立即用大量的水冲洗,然后涂上3%~5%的
(2)用硫单质制取硫酸的转化流程示意图如下:

在S、SO2、SO3、H2SO4四种物质中,硫元素的化合价表现为+4价的物质是
(3)现取100g稀硫酸倒入烧杯中,慢慢向烧杯中加入溶质质量分数为10%的Ba(NO3)2溶液,反应过程中产生沉淀的质量与所加入Ba(NO3)2溶液的质量关系如图所示。

试回答:
①当加入Ba(NO3)2溶液300g时(即图中A点),烧杯中溶液里大量存在的酸根离子是
②当加入Ba(NO3)2溶液522g时(即图中B点),恰好完全反应,试通过计算求产生沉淀的总质量。(计算结果精确至0.1g)。
更新时间:2022-06-28 14:36:14
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】(1)用化学用语填空:
① 氖气____________________ ;
② 氧化铜中铜元素的化合价为 + 2 价___________________ ;
③ 保持水的化学性质的最小微粒_________________ ;
④ 硫酸铁__________________ 。
(2)世界长寿乡—蕉岭,是一个美丽宜居的好地方。蕉岭长寿的关键因子是水土富硒,硒元素具有抗衰老、抑制癌细胞生长的功能,其元素符号为Se。
①硒原子的结构示意图为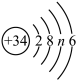 n 的值为
n 的值为___________ ;
②硒原子在化学反应中得到电子形成离子,其离子符号是_____________ 。
① 氖气
② 氧化铜中铜元素的化合价为 + 2 价
③ 保持水的化学性质的最小微粒
④ 硫酸铁
(2)世界长寿乡—蕉岭,是一个美丽宜居的好地方。蕉岭长寿的关键因子是水土富硒,硒元素具有抗衰老、抑制癌细胞生长的功能,其元素符号为Se。
①硒原子的结构示意图为
 n 的值为
n 的值为②硒原子在化学反应中得到电子形成离子,其离子符号是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】回答小练问题:
(1)如图所示,A,C为无色液体,B,D,E为无色气体,它们之间发生如下变化,其中B是人类生存的最主要的气体,请你根据所学的化学知识作出推断:
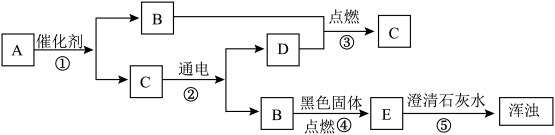
①写出所推断物质的化学式:A______ 、C______ 、D______ 。
②写出过程④化学反应的符号表达式:______ 。
(2)空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。
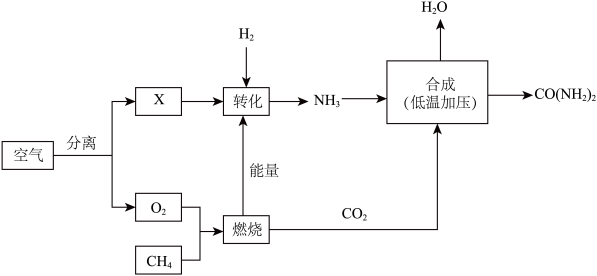
①X是空气中含量最多的气体,则“转化”过程的基本反应类型是______ 。
②在“燃烧”过程中,氧元素的化合价的变化是:由______ 价→______ 价。
(1)如图所示,A,C为无色液体,B,D,E为无色气体,它们之间发生如下变化,其中B是人类生存的最主要的气体,请你根据所学的化学知识作出推断:

①写出所推断物质的化学式:A
②写出过程④化学反应的符号表达式:
(2)空气是宝贵的自然资源,如图是以空气等为原料合成尿素[CO(NH2)2]的流程。

①X是空气中含量最多的气体,则“转化”过程的基本反应类型是
②在“燃烧”过程中,氧元素的化合价的变化是:由
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
解题方法
【推荐3】核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题。
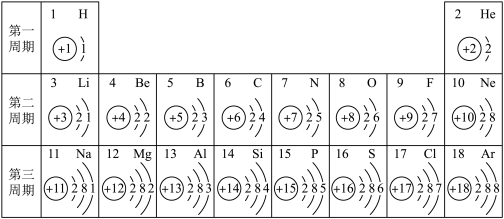
(1)2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为______ ,核外电子数为______ 。
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是_________ 。
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质______ 、氧化物______ 、酸______ 、碱______ 、盐______ 。
(4)以钠和氯为例,简述结构与性质的关系。________________________ 。
(5)国产C919大型客机上使用了大量的铝合金。工业上用电解氧化铝(Al2O3)得到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(在答题卡上写出计算过程)

(1)2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为“镆”。此元素原子的核电荷数为
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质
(4)以钠和氯为例,简述结构与性质的关系。
(5)国产C919大型客机上使用了大量的铝合金。工业上用电解氧化铝(Al2O3)得到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(在答题卡上写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
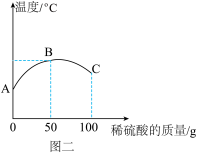
【推荐1】某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐次加入质量分数为9.8%的稀硫酸,测出溶液的pH随加入稀硫酸的质量变化关系如图一所示。用温度计测量溶液温度变化如图二所示(不考虑反应过程中热量损失)。试回答:
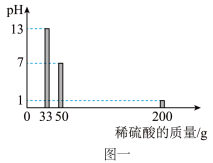
(1)当pH=_________ 时,溶液中所含的溶质只有Na2SO4。
(2)浓硫酸常用作O2、CO2等气体干燥剂,说明浓硫酸具有_________ 性,此过程发生的是_________ 变化。(填“物理”或“化学”)
(3)根据图二温度变化情况,可以判断该反应是_________ 反应。(填“吸热”或“放热”)
(4)计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。


(1)当pH=
(2)浓硫酸常用作O2、CO2等气体干燥剂,说明浓硫酸具有
(3)根据图二温度变化情况,可以判断该反应是
(4)计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】在学习了金属的化学性质后,科学老师布置了一项课外学习任务:调查化工颜料店出售 的涂料添加剂“银粉”是什么金属?某学习小组通过调查,分别获得了“银粉”是银粉、铝粉、 锌粉这三种不同结果。为了确定究竟是哪一种金属,学习小组同学将一小包“银粉”带回实 验室,进行了如下实验和分析。(相关反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑;2Al+6HCl=2AlCl3+3H2↑)
(1)取少量“银粉”于试管中,滴加适量盐酸,观察到有 1 产生,说明“银粉”一定不是银。
(2)为了进一步确定“银粉”是铝还是锌,学习小 组通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图像。
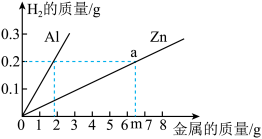
取1.8克“银粉”(杂质忽略不计)加入到50克稀盐酸中,恰好完全反应,生成氢气0.2克。根据上图可知,“银粉”是 2 。计算实验中所用稀盐酸的溶质质量分数 3 。
(1)取少量“银粉”于试管中,滴加适量盐酸,观察到有
(2)为了进一步确定“银粉”是铝还是锌,学习小 组通过理论计算,获得两种金属分别与足量盐酸反应产生氢气的质量关系,并绘制成如图所示图像。

取1.8克“银粉”(杂质忽略不计)加入到50克稀盐酸中,恰好完全反应,生成氢气0.2克。根据上图可知,“银粉”是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】金属在生产、生活中有广泛的应用,认识金属的性质有利于我们更好地利用金属。
(1)第19届杭州亚运会主火炬——“薪火”,其金属部分采用1070铝合金旋压成型工艺,铝合金与纯铝相比的优点是______ (一条即可);科研团队借鉴汽车发动机的喷油器,为主火炬设计出雾化系统,使甲醇在加压至19米高空后,也能完美地配合点火时刻。从促进燃料充分燃烧角度看﹐燃料雾化的作用是______ 。
(2)铁是应用最广泛的金属。实验室用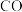 还原氧化铁模拟工业炼铁,其装置如图所示:
还原氧化铁模拟工业炼铁,其装置如图所示:______ ;
②写出B装置玻璃管内发生反应的化学方程式______ ﹔
③从环保角度考虑,该装置尚有不足之处,请你提出改进措施______ (写一种即可)。
(3)将一定量的锌粉加入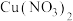 和
和 的混合溶液中,充分反应后过滤,可以得到溶液和滤渣。
的混合溶液中,充分反应后过滤,可以得到溶液和滤渣。
①若所得滤液呈蓝色,写出一定发生反应的化学方程式______ ;
②若过滤后所得固体(已洗涤﹑干燥)的质量等于加入锌粉的质量。请写出所得溶液中一定含有的溶质的化学式______ 。
(4)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”方法:“熬胆矾铁釜,久之亦化为铜”。即在硫酸铜溶液中加入铁,得到铜。现用足量铁与100g16%的 溶液反应,请计算可得到铜的质量。
溶液反应,请计算可得到铜的质量。
(1)第19届杭州亚运会主火炬——“薪火”,其金属部分采用1070铝合金旋压成型工艺,铝合金与纯铝相比的优点是
(2)铁是应用最广泛的金属。实验室用
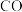 还原氧化铁模拟工业炼铁,其装置如图所示:
还原氧化铁模拟工业炼铁,其装置如图所示: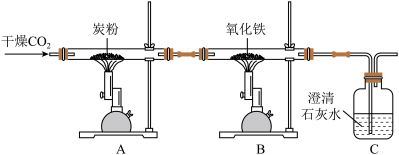
②写出B装置玻璃管内发生反应的化学方程式
③从环保角度考虑,该装置尚有不足之处,请你提出改进措施
(3)将一定量的锌粉加入
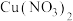 和
和 的混合溶液中,充分反应后过滤,可以得到溶液和滤渣。
的混合溶液中,充分反应后过滤,可以得到溶液和滤渣。①若所得滤液呈蓝色,写出一定发生反应的化学方程式
②若过滤后所得固体(已洗涤﹑干燥)的质量等于加入锌粉的质量。请写出所得溶液中一定含有的溶质的化学式
(4)北宋沈括所著的《梦溪笔谈》中记载了“湿法炼铜”方法:“熬胆矾铁釜,久之亦化为铜”。即在硫酸铜溶液中加入铁,得到铜。现用足量铁与100g16%的
 溶液反应,请计算可得到铜的质量。
溶液反应,请计算可得到铜的质量。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】无明显现象反应的可视化是一项重要的课题。
(1)某化学研究小组以“探究CO2与NaOH是否反应”为主题展开化学反应可视化研究,设计了如下两个实验。
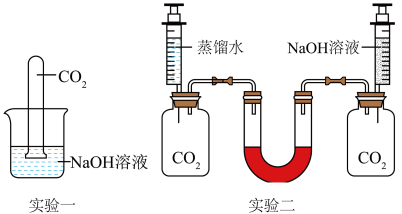
实验一:将一支充满CO2的试管倒扣在盛有NaOH溶液的烧杯中,观察试管中的液面变化情况。
实验二:向两个装湖CO2的同样规格的瓶中分别注入等体积的蒸水和NaOH溶液,充分反应后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况。
试回答下列问题:
①在实验中,需要提前配制NaOH溶液并制备CO2。配制NaOH溶液时,若不慎将氢氧化钠沾到皮肤上,应立即用大量水冲洗,然后涂______ (填“碳酸氢钠”“硼酸”“硫酸”之一)溶液;实验室用石灰石和稀盐酸制备CO2的化学方程式为______ 。
②实验二中若观察到U型管______ (填“左”或“右”)端液面升高,则证明溶液中的NaOH与CO2发生了化学反应。
③与实验一相比,小组同学认为实验二更合理,因为它排除了______ (填化学式)对实验的干扰。
(2)为测定某Na2CO3溶液的溶质质量分数,某小组同学取100g该溶液,向其中逐滴加入溶质质量分数为17.1%的Ba(OH)2溶液,反应中生成沉淀的质量与加入Ba(OH)2溶液的质量关系如图所示。
试回答:
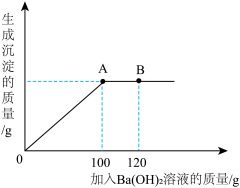
①当加入Ba(OH)2溶液120g时(即B点),所得溶液中一定存在的溶质是______ (填化学式)。
②当加入Ba(OH)2溶液100g时(即A点),恰好完全反应。试通过计算,求所取Na2CO3溶液的溶质质量分数______ 。(计算结果精确至0.1%)
(1)某化学研究小组以“探究CO2与NaOH是否反应”为主题展开化学反应可视化研究,设计了如下两个实验。

实验一:将一支充满CO2的试管倒扣在盛有NaOH溶液的烧杯中,观察试管中的液面变化情况。
实验二:向两个装湖CO2的同样规格的瓶中分别注入等体积的蒸水和NaOH溶液,充分反应后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况。
试回答下列问题:
①在实验中,需要提前配制NaOH溶液并制备CO2。配制NaOH溶液时,若不慎将氢氧化钠沾到皮肤上,应立即用大量水冲洗,然后涂
②实验二中若观察到U型管
③与实验一相比,小组同学认为实验二更合理,因为它排除了
(2)为测定某Na2CO3溶液的溶质质量分数,某小组同学取100g该溶液,向其中逐滴加入溶质质量分数为17.1%的Ba(OH)2溶液,反应中生成沉淀的质量与加入Ba(OH)2溶液的质量关系如图所示。
试回答:

①当加入Ba(OH)2溶液120g时(即B点),所得溶液中一定存在的溶质是
②当加入Ba(OH)2溶液100g时(即A点),恰好完全反应。试通过计算,求所取Na2CO3溶液的溶质质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】某工厂生产的粗盐样品含有氯化钠和氯化镁两种物质,为了测定该粗盐样品中氯化钠的质量分数,该厂检测员称取20g该样品,完全溶解在127.8g水中,向所得溶液滴加氢氧化钠溶液。实验需要配置氢氧化钠溶液,实验操作示意图如下图所示,请回答:
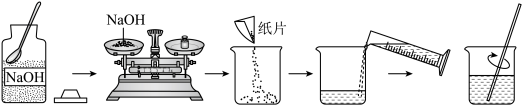
(1)图甲中有一处明显错误是____________ 。
(2)配置一定质量分数的氢氧化钠溶液,下列操作可能会导致所配溶液浓度偏大的是 (填序号,双选)
(3)向所得样品溶液中加入氢氧化钠溶液,产生的沉淀质量与加入氢氧化钠溶液质量的关系如图所示,请计算样品中氯化钠的质量分数(写出计算过程)
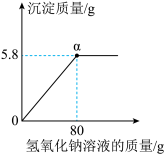
(4)取图乙中α点溶液过滤,将滤液进行蒸发,溶液蒸干后所得的氯化钠固体比原20g粗盐样品所含氯化钠的质量____________ (填“偏大”“偏小”或“不变”)

(1)图甲中有一处明显错误是
(2)配置一定质量分数的氢氧化钠溶液,下列操作可能会导致所配溶液浓度偏大的是 (填序号,双选)
| A.使用量筒量取液体时俯视读数 | B.装瓶时有部分液体溅出 |
| C.溶解时所用烧杯内壁有水珠 | D.使用生锈的砝码称量样品 |

(4)取图乙中α点溶液过滤,将滤液进行蒸发,溶液蒸干后所得的氯化钠固体比原20g粗盐样品所含氯化钠的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
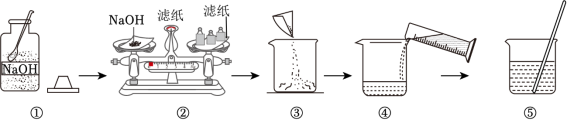
【推荐3】实验室配制100g质量分数为10%的氢氧化钠溶液,主要步骤如下。
(1)配制上述溶液时,所需水的质量为______ g。
(2)步骤②中存在错误,应将氢氧化钠固体放在烧杯中称量,原因是氢氧化钠固体具有______ 性,使用滤纸称量时,可能会有部分氢氧化钠粘在滤纸上,导致配制的溶液中溶质质量分数______ (填“偏大”“偏小”或“不变”)。
(3)步骤⑤中玻璃棒的作用是______ 。
(4)取所配制的氢氧化钠溶液40g于烧杯中,滴入两滴酚酞溶液并搅拌,再逐滴滴加稀盐酸,边滴边搅拌,至溶液恰好变成无色。计算消耗的稀盐酸中溶质的质量(写出计算过程)。
(1)配制上述溶液时,所需水的质量为
(2)步骤②中存在错误,应将氢氧化钠固体放在烧杯中称量,原因是氢氧化钠固体具有
(3)步骤⑤中玻璃棒的作用是
(4)取所配制的氢氧化钠溶液40g于烧杯中,滴入两滴酚酞溶液并搅拌,再逐滴滴加稀盐酸,边滴边搅拌,至溶液恰好变成无色。计算消耗的稀盐酸中溶质的质量(写出计算过程)。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】铁及其化合物是中学化学学习和研究的重要内容。
(1)在进行铁丝在氧气中燃烧的实验时,集气瓶底放少量的水或砂子目的是_____ 。在生活中为防止家中的菜刀生锈,可采取的方法是_____ 。
(2)活性铁粉常用作脱氧保鲜剂,原理是铁和氧气、水反应生成氢氧化铁,该反应的化学方程式为_____ ;单质铁可以和硫酸铁溶液反应生成硫酸亚铁,化学反应方程式为_____ 。
(3)生物浸出技术在金属冶炼中应用广泛。嗜热细菌在酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2)产生硫酸盐,进而生产铜和绿矾(硫酸亚铁晶体),主要流程如图。
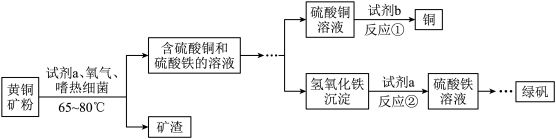
①若反应①的另一种产物最终也可制得绿矾,则试剂b为_____ ;若反应②为中和反应,写出该反应的化学方程式:_____ 。
②现有100t杂质质量分数为8%的黄铜矿(杂质不参与反应且不溶于水),经上述流程制得硫酸铁溶液,再向硫酸铁溶液中加入足量的铁粉,请计算能制得硫酸亚铁的质量__ 。
(1)在进行铁丝在氧气中燃烧的实验时,集气瓶底放少量的水或砂子目的是
(2)活性铁粉常用作脱氧保鲜剂,原理是铁和氧气、水反应生成氢氧化铁,该反应的化学方程式为
(3)生物浸出技术在金属冶炼中应用广泛。嗜热细菌在酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2)产生硫酸盐,进而生产铜和绿矾(硫酸亚铁晶体),主要流程如图。

①若反应①的另一种产物最终也可制得绿矾,则试剂b为
②现有100t杂质质量分数为8%的黄铜矿(杂质不参与反应且不溶于水),经上述流程制得硫酸铁溶液,再向硫酸铁溶液中加入足量的铁粉,请计算能制得硫酸亚铁的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和的目标。
(1)造成温室效应加剧的主要原因是煤、石油和______ 等化石燃料的过度使用。为了减缓大气中二氧化碳的增加,我们生活中可以______ (任写一条)。
(2)某兴趣小组在实验室中制取纯净、干燥的CO2,并探究CO2的性质。
根据下图回答问题:

Ⅰ、仪器x的名称是______ 。
Ⅱ、实验室中制取纯净、干燥的CO2,应选择的实验装置从左到右依次是______ (填写编号),如何证明二氧化碳已收集满______ 。
Ⅲ、要证明二氧化碳可以与水作用,请利用以上装置设计实验______ 。
Ⅳ、将二氧化碳通入氢氧化钠溶液中无明显现象,为了探究它们是否发生了化学反应,兴趣小组同学设计了如图装置(图甲)测定二氧化碳浓度的变化,并绘制成曲线(图乙)。

分析:二氧化碳与氢氧化钠发生反应的时间段为______ 。mn段二氧化碳浓度不变的原因是______ 。
(3)二氧化碳的资源化利用是实现碳减排的重要途径。近年,我国科学家合成了一种新型催化剂,可以将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为______ 。
(4)实验室用100g含杂质(杂质不和稀盐酸反应) 20%的石灰石与稀盐酸充分反应,生成二氧化碳气体多少?(写出计算过程)
(1)造成温室效应加剧的主要原因是煤、石油和
(2)某兴趣小组在实验室中制取纯净、干燥的CO2,并探究CO2的性质。
根据下图回答问题:

Ⅰ、仪器x的名称是
Ⅱ、实验室中制取纯净、干燥的CO2,应选择的实验装置从左到右依次是
Ⅲ、要证明二氧化碳可以与水作用,请利用以上装置设计实验
Ⅳ、将二氧化碳通入氢氧化钠溶液中无明显现象,为了探究它们是否发生了化学反应,兴趣小组同学设计了如图装置(图甲)测定二氧化碳浓度的变化,并绘制成曲线(图乙)。

分析:二氧化碳与氢氧化钠发生反应的时间段为
(3)二氧化碳的资源化利用是实现碳减排的重要途径。近年,我国科学家合成了一种新型催化剂,可以将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为
(4)实验室用100g含杂质(杂质不和稀盐酸反应) 20%的石灰石与稀盐酸充分反应,生成二氧化碳气体多少?(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
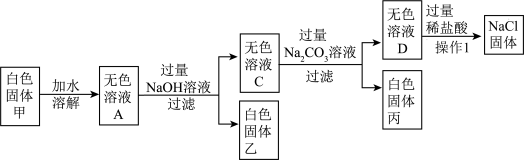
【推荐3】某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaC12和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:______ 。
(2)写出操作1的名称______ ,白色固体乙的化学式______ 。
(3)写出生成白色固体丙的化学方程式______ 。
(4)向无色溶液D中加入过量稀盐酸的目的是______ 。
(5)经过上述实验验证,白色固体甲的成分为______ 。
(6)该同学为了进一步确定固体混合物的组成,另取样品100.0g,按照上述流程图进行实验,白色固体乙5.8g,白色固体丙19.7g,则样品中NaC1的质量分数为______ (计算结果精确至0.1)。
(2)写出操作1的名称
(3)写出生成白色固体丙的化学方程式
(4)向无色溶液D中加入过量稀盐酸的目的是
(5)经过上述实验验证,白色固体甲的成分为
(6)该同学为了进一步确定固体混合物的组成,另取样品100.0g,按照上述流程图进行实验,白色固体乙5.8g,白色固体丙19.7g,则样品中NaC1的质量分数为
您最近一年使用:0次



