纯碱样品中含有少量的氯化钠,某同学为测定该纯碱(Na2CO3)样品中碳酸钠的含量,他取该纯碱样品11g,全部溶解在100g水中,再加入150.7g氯化钡溶液,恰好完全反应,过滤,得到19.7g沉淀(不考虑过程中物质质量的损失)。请计算:
(1)纯碱样品中碳酸钠的质量______ g;
(2)反应后所得溶液的质量为______ g;
(3)样品中碳酸钠的质量分数为多少? (计算结果保留到0.1%)
(1)纯碱样品中碳酸钠的质量
(2)反应后所得溶液的质量为
(3)样品中碳酸钠的质量分数为多少? (计算结果保留到0.1%)
2022·广西·三模 查看更多[1]
更新时间:2022-07-02 23:51:36
|
相似题推荐
计算题
|
适中
(0.65)
真题
【推荐1】某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
问:
A.表中m的值为 ;
B.原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 20 | 20 | 20 | 20 |
| 加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
问:
A.表中m的值为 ;
B.原固体混合物中MgCl2的质量分数是多少?(要求写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】钢铁的生产和使用是人类文明和社会进步的一个重要标志。化学兴趣小组同学为测定某钢铁厂生铁样品中铁的质量分数,取样品进行实验,实验过程及测得数据如下(杂质不溶于水,也不与酸反应,杂质中不含铁元素):

(1)用托盘天平称量14g样品时,若发现天平指针向右偏转,此时应该采取的操作是___________ 。
(2)反应已经结束的标志是___________ 。
(3)计算该钢铁厂生铁样品中铁的质量分数。(要求写出计算过程)
(4)若工业上用含氧化铁80%的赤铁矿1000t(假设炼制过程中铁矿石的利用率为90%)能炼出上述生铁的质量为___________ t。

(1)用托盘天平称量14g样品时,若发现天平指针向右偏转,此时应该采取的操作是
(2)反应已经结束的标志是
(3)计算该钢铁厂生铁样品中铁的质量分数。(要求写出计算过程)
(4)若工业上用含氧化铁80%的赤铁矿1000t(假设炼制过程中铁矿石的利用率为90%)能炼出上述生铁的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】纯碱常会含有少量的氯化钠(其它杂质忽略不计)。取6g纯碱样品放在烧杯中并不断滴入稀盐酸。当稀盐酸滴加至35g时,烧杯内溶液的总质量为38.8g(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示。请计算:
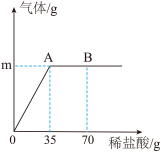
(1)Na2CO3由 种元素组成,碳、氧元素质量比是 。
(2)A点产生气体的质量m是 g。
(3)纯碱样品中碳酸钠的质量分数。(精确到0.1%)

(1)Na2CO3由 种元素组成,碳、氧元素质量比是 。
(2)A点产生气体的质量m是 g。
(3)纯碱样品中碳酸钠的质量分数。(精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】2018年10月3日,搜狐网报道,中国居然用铝合金造军舰,外形十分科幻和美军的几乎一模一样。为测定建造军舰的材料某铝合金中铝的质量分数,兴趣小组同学称取该样品20g铝合金粉末于烧杯中,将400g稀硫酸分四次加入,充分反应,测得实验数据如下表所示:(假设该铝合金中只有铝能与稀硫酸反应,其他成分不与稀硫酸反应)
(1)实验中m的数值_____。
(2)该铝合金样品中铝的质量分数为_____?(写出计算过程)
(3)第三次加入稀硫酸后,溶液的成分是_______。
| 实验 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量(g) | 100 | 100 | 100 | 100 |
| 烧杯中剩余物的质量(g) | 119.2 | 218.4 | 318.0 | m |
(1)实验中m的数值_____。
(2)该铝合金样品中铝的质量分数为_____?(写出计算过程)
(3)第三次加入稀硫酸后,溶液的成分是_______。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐1】向60gNa2CO3溶液中逐滴加入一定溶质质量分数的CaCl2溶液。实验过程中生成沉淀的质量与加入CaCl2溶液的质量关系如图所示。
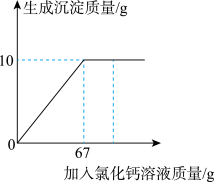
(1)恰好完全反应时,生成沉淀的质量为_________g。
(2)计算恰好完全反应时,所得溶液中溶质的质量分数为__________________。

(1)恰好完全反应时,生成沉淀的质量为_________g。
(2)计算恰好完全反应时,所得溶液中溶质的质量分数为__________________。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸铜是重要的化工原料,广泛用作纺织品媒染剂、农用杀虫剂、消毒剂、饲料添加剂及工业镀铜等。工业上常用含铜废料与稀硫酸和氧气在加热条件下反应制得硫酸铜,反应的化学方程式为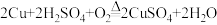 。试计算:
。试计算:
(1)硫酸铜中铜、硫元素的质量比是___________ 。
(2)若要配制10t19.6%的稀硫酸溶液,需要98%的浓硫酸的质量是多少?需要水的质量是多少?
(3)假设配制好的稀硫酸与含一定量铜的废料恰好完全反应(含铜废料中的杂质不溶于水也不与稀硫酸反应),求反应后所得溶液的溶质质量分数(计算结果保留一位小数)。
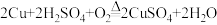 。试计算:
。试计算:(1)硫酸铜中铜、硫元素的质量比是
(2)若要配制10t19.6%的稀硫酸溶液,需要98%的浓硫酸的质量是多少?需要水的质量是多少?
(3)假设配制好的稀硫酸与含一定量铜的废料恰好完全反应(含铜废料中的杂质不溶于水也不与稀硫酸反应),求反应后所得溶液的溶质质量分数(计算结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某兴趣小组向一定量黄铜(铜锌合金)中逐渐加入稀盐酸制取氢气。将150g稀盐酸分三次加入,每次生成气体的质量如下表所示:
计算:
(1)共制得氢气的质量是_______ g。
(2)所用稀盐酸溶质的质量分数。
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸质量/g | 50 | 50 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.1 |
(1)共制得氢气的质量是
(2)所用稀盐酸溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某校化学研究性学习小组的同学,通过实验测定石灰石中碳酸钙的含量,取100 g石灰石样品(杂质不与酸或水反应)放入烧杯中并加入300 g稀盐酸,恰好完全反应。把产生的二氧化碳气体用足量的氢氧化钠溶液吸收,同时测量3分钟内氢氧化钠溶液增重的质量,结果如下表:
试完成下列问题:
(1)请在坐标纸上,以反应时间为横轴,以产生二氧化碳气体的质量为纵轴,画出产生气体的质量随反应时间变化的关系曲线。
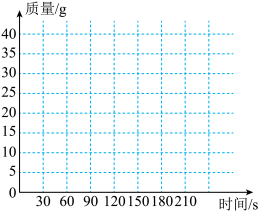
(2)从表中可以看出,100 g石灰石与足量稀盐酸反应生成的二氧化碳最多是______g。
| 时间/s | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
| 质量/g | 0 | 15 | 25 | 30 | 33 | 33 | 33 |
试完成下列问题:
(1)请在坐标纸上,以反应时间为横轴,以产生二氧化碳气体的质量为纵轴,画出产生气体的质量随反应时间变化的关系曲线。

(2)从表中可以看出,100 g石灰石与足量稀盐酸反应生成的二氧化碳最多是______g。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在牙膏中,常用轻质碳酸钙粉末等作摩擦剂。已知某品牌牙膏中的摩擦剂是碳酸钙,化学兴趣小组用一定浓度的稀盐酸测定该牙膏中碳酸钙的含量(查阅资料知牙膏中的其他成分不与盐酸发生反应)。该小组取用4g牙膏置于小烧杯内并加入20g水,充分搅拌后,称量烧杯及内容物总质量为45.3g。再将20g稀盐酸分5次加入小烧杯内,充分反应后分别称量烧杯及内容物质量变化情况。测得如下数据:
______ 。
(2)牙膏中的碳酸钙完全反应时生成CO2的质量为_______ g。
(3)通过表格数据计算该牙膏中碳酸钙的质量分数。(写出详细的计算过程)
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸质量/g | 5 | 5 | 5 | 5 |
| 烧杯及内容物质量/g | 49.97 | 54.64 | 59.53 | 64.53 |

(2)牙膏中的碳酸钙完全反应时生成CO2的质量为
(3)通过表格数据计算该牙膏中碳酸钙的质量分数。(写出详细的计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
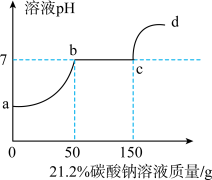
(1)c→d段溶液的pH大于7的原因是___________ 。
(2)反应到b点时,生成的气体的质量是多少?___________ (写出计算过程)

(1)c→d段溶液的pH大于7的原因是
(2)反应到b点时,生成的气体的质量是多少?
您最近一年使用:0次


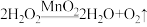 ,该同学将50g过氧化氢溶液和1g二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g。求:
,该同学将50g过氧化氢溶液和1g二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g。求:

