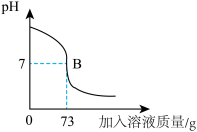
如图是小潘同学在做氢氧化钠和稀盐酸反应时得到的的pH曲线图,此实验是将_______ 溶液(填“氢氧化钠”或“稀盐酸”)滴入另一种溶液中。此实验取用氢氧化钠溶液的质量为40克,所用的稀盐酸溶液的溶质的质量分数为10%,求该氢氧化钠溶液中溶质的质量分数为多少?_____

更新时间:2022-07-07 12:28:11
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】请分析如图所示的实验过程和数据,并进行计算。

(1)生成氢气的质量为______ g。
(2)求反应后所得溶液中溶质的质量分数。

(1)生成氢气的质量为
(2)求反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】2023年政府工作报告提出深入推进环境污染防治。某污水处理厂用含NaOH的碱性废水处理19.6t溶质质量分数为10%的硫酸废水(其它物质不参与反应),溶液pH的变化曲线如图所示。请回答下列问题: 的废水,在不用pH检测器和指示剂的情况下,判断废水呈中性的依据是
的废水,在不用pH检测器和指示剂的情况下,判断废水呈中性的依据是______ 。
(2)计算处理后废水呈中性时,溶液中溶质的质量分数_____ (写出计算过程,结果精确到0.1%)。
(3)若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,所得溶液的溶质成分是_______ 。(填化学式)。
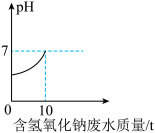
 的废水,在不用pH检测器和指示剂的情况下,判断废水呈中性的依据是
的废水,在不用pH检测器和指示剂的情况下,判断废水呈中性的依据是(2)计算处理后废水呈中性时,溶液中溶质的质量分数
(3)若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,所得溶液的溶质成分是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】化学小组开展“酸与碱之间发生的反应”探究实验活动,方案如下:取一洁净的锥形瓶,往其中加入30g氢氧化钠溶液,然后逐滴滴入质量分数为9.8%的稀硫酸至恰好完全反应,锥形瓶及溶液总质量随加入稀硫酸质量的变化关系如图所示。

(1)为了获取酸能与碱反应的证据,滴加稀硫酸前,锥形瓶中还需加入的是________ 。
(2)反应过程中溶液中的粒子数目不断减少的是________。(填序号)
(3)a的值是________ 。
(4)求反应后溶液中溶质的质量分数。(写出详细计算过程)

(1)为了获取酸能与碱反应的证据,滴加稀硫酸前,锥形瓶中还需加入的是
(2)反应过程中溶液中的粒子数目不断减少的是________。(填序号)
A. | B. | C. | D. |
(4)求反应后溶液中溶质的质量分数。(写出详细计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】实验室欲测定一瓶标签破损的稀盐酸的溶质质量分数。现取10g稀盐酸样品,将5%的氢氧化钠溶液逐滴加入样品中,边加边搅拌,随着氢氧化钠溶液加入,溶液液的pH的变化如图所示。试回答:
(1)a点溶液中含有的溶质有___________ 。
(2)当pH=7时,消耗氢氧化钠溶液中溶质NaOH的质量为___________ 。
(3)计算pH=7时,生成溶液中溶质的质量分数。(小数点后保留一位小数)
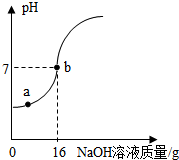
(1)a点溶液中含有的溶质有
(2)当pH=7时,消耗氢氧化钠溶液中溶质NaOH的质量为
(3)计算pH=7时,生成溶液中溶质的质量分数。(小数点后保留一位小数)

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】人体内胃酸过多,会引起胃溃疡。下图为某抗酸药包装标签上的部分文字,请回答下列问题。

(1)胃酸的主要成分是_______ (填化学式)。
(2)氢氧化铝在物质分类中属于_______ 。
(3)该药需“咀嚼后吞服”的原因为_______ ,吞服该药物后胃液的pH值将迅速_______ (填“升高”、“降低”)。
(4)某同学取一片药片(质量0.5g),捣碎后加20mL蒸馏水溶解,再加入含HCl质量为0.33g的稀盐酸恰好完全反应(假设其他成分不反应),试根据化学方程式计算该药片中氢氧化铝的质量是否达到标定____ (保留小数点后两位数)。

(1)胃酸的主要成分是
(2)氢氧化铝在物质分类中属于
(3)该药需“咀嚼后吞服”的原因为
(4)某同学取一片药片(质量0.5g),捣碎后加20mL蒸馏水溶解,再加入含HCl质量为0.33g的稀盐酸恰好完全反应(假设其他成分不反应),试根据化学方程式计算该药片中氢氧化铝的质量是否达到标定
您最近一年使用:0次




