张老师在课堂上做了这样一个实验:往半瓶矿泉水中加入一片维C泡腾片,立即产生大量气泡,片刻成为一瓶可口的饮料。同学们对此产生了极大的兴趣,在张老师的指导下进行了如下的探究:
【提出问题】该气体的成分是什么?
【查阅资料】维C泡腾片是一种保健药品,其主要成分有维生素C(C6H8O6)、碳酸氢钠(NaHCO3)和柠檬酸(C6H8O7),柠檬酸是一种酸。
【提出猜想】甲同学根据质量守恒定律认为该气体可能是CO2、CO、H2、O2中的一种或几种,而乙同学还从保健药品安全角度考虑,由于CO、H2属于易燃易爆气体,且_____ (填“CO”或“H2”)有毒,所以不可能含有CO和H2,认为该气体只可能是CO2、O2中的一种或两种。
【进行实验】丙同学将产生的气体通入澄清石灰水中,观察到澄清石灰水变浑浊。丁同学用带火星的木条检验该矿泉水瓶内的气体,没有观察到带火星的木条复燃。
【得出结论】根据丙同学和丁同学的实验,张老师组织学生讨论后认为:由丙同学的实验可知,该气体中肯定含有CO2,此过程中反应的化学方程式为_____ ;由于同学的实验不能确定该气体中是否含有O2,理由是 _____ 。根据有关资料和实验证明,该气体中只含CO2。
【拓展延伸】为了测定某维C泡腾片中碳酸氢钠的含量,张老师引导学生设计了如下实验装置(仪器固定装置及止水夹等均已略去)并进行实验。有关实验数据为:维C泡腾片2片(每片维C泡腾片的质量为4.00g),盛有碱石灰(碱石灰是一种干燥剂,可吸收CO2气体和水蒸气)的干燥管a质量增加了0.88g。
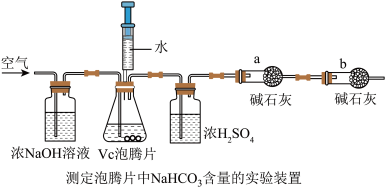
(1)碳酸氢钠(NaHCO3)俗称_____ ,可与酸反应产生二氧化碳。NaHCO3与稀盐酸反应的化学方程式为 _____ 。
(2)该实验中维C泡腾片反应完毕后通入空气的目的是_____ ;装置中干燥管b的作用是 _____ 。
(3)根据实验数据,可计算出该维C泡腾片中碳酸氢钠的含量为_____ 。
(4)如果撤去装置中盛有浓硫酸的洗气瓶,则测定结果_____ (填“偏高”“偏低”或“无影响”)
【提出问题】该气体的成分是什么?
【查阅资料】维C泡腾片是一种保健药品,其主要成分有维生素C(C6H8O6)、碳酸氢钠(NaHCO3)和柠檬酸(C6H8O7),柠檬酸是一种酸。
【提出猜想】甲同学根据质量守恒定律认为该气体可能是CO2、CO、H2、O2中的一种或几种,而乙同学还从保健药品安全角度考虑,由于CO、H2属于易燃易爆气体,且
【进行实验】丙同学将产生的气体通入澄清石灰水中,观察到澄清石灰水变浑浊。丁同学用带火星的木条检验该矿泉水瓶内的气体,没有观察到带火星的木条复燃。
【得出结论】根据丙同学和丁同学的实验,张老师组织学生讨论后认为:由丙同学的实验可知,该气体中肯定含有CO2,此过程中反应的化学方程式为
【拓展延伸】为了测定某维C泡腾片中碳酸氢钠的含量,张老师引导学生设计了如下实验装置(仪器固定装置及止水夹等均已略去)并进行实验。有关实验数据为:维C泡腾片2片(每片维C泡腾片的质量为4.00g),盛有碱石灰(碱石灰是一种干燥剂,可吸收CO2气体和水蒸气)的干燥管a质量增加了0.88g。

(1)碳酸氢钠(NaHCO3)俗称
(2)该实验中维C泡腾片反应完毕后通入空气的目的是
(3)根据实验数据,可计算出该维C泡腾片中碳酸氢钠的含量为
(4)如果撤去装置中盛有浓硫酸的洗气瓶,则测定结果
2022·湖南株洲·中考真题 查看更多[11]
2022年湖南省株洲市中考化学真题(已下线)专题11 碳和碳的氧化物-2022年中考化学真题分项汇编(全国通用)(第03期)(已下线)专题18 科学探究题-2022年中考化学真题分项汇编(全国通用)(第03期)(已下线)第4单元 燃料及其燃烧(B卷·能力检测练)-【单元测试】2022-2023学年九年级化学上册分层训练AB卷(沪教版·上海)(已下线)第六单元 碳和碳的氧化物(测试)-2023年中考化学一轮复习讲练测(人教版)(已下线)单元复习06 碳和碳的氧化物【过习题】 -2022-2023学年九年级化学上册单元复习过过过(人教版)2023年辽宁省沈阳初中学业水平仿真化学试题一(已下线)黄金卷03-【赢在中考·黄金8卷】备战2023年中考化学全真模拟卷(陕西专用)2023年山东省潍坊市学业水平模拟化学试题六(已下线)专题22 科学探究-学易金卷:三年(2021-2023)中考化学真题分项汇编(湖南专用)(已下线)第六单元 碳和碳的氧化物【过习题】-2023-2024学年九年级化学单元复习过过过(人教版)
更新时间:2022-07-26 08:38:19
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某同学在查看饼干配料表时,发现饼干的膨松剂有的含有碳酸氢钠,而有的含有碳酸氢铵。他深感好奇,碳酸氢铵是一种肥料,怎么也可以做膨松剂呢?为此,他进行如下探究。
查阅资料:①2NaHCO3 Na2CO3+H2O+CO2↑;NH4HCO3
Na2CO3+H2O+CO2↑;NH4HCO3 NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。
②膨松剂的主要成分为碳酸氢铵(NH4HCO3),其他成分受热不分解。
任务一:初识膨松剂
(1)膨松剂能使食品变松软、蓬松。碳酸氢钠可用作膨松剂,其俗名是___________ 。
任务二:比较膨松效果
(2)通过以上实验发现,实验2中烘焙的面团更大更松软,原因是反应相同质量碳酸氢钠和碳酸氢铵,后者___________ 。
任务三:测定某品牌膨松剂中碳酸氢铵的质量分数
甲同学认为,该膨松剂中可能含有水分,会影响实验结果。故他提出可以通过测定反应后生成的某物质质量来达到实验目的。
查阅资料:碱石灰是NaOH与CaO的固体混合物;氨气不与碱石灰反应,能与浓硫酸发生化合反应。
根据资料,他设计了如图所示实验装置及主要步骤(B、C、D中药品均足量)。
步骤2:打开弹簧夹,通入氮气一段时间后,关闭弹簧夹;
步骤3:称量装置C的质量为m1g;
步骤4:点燃酒精灯,充分反应后停止加热;
步骤5:……;
步骤6:再次称量装置C的质量为m2g。
(3)装置B中发生反应的化学方程式为___________ (写1个即可)。
(4)该膨松剂中碳酸氢铵的质量分数为___________ (用代数式表示)。
(5)关于该实验,下列说法正确的是___________ (填标号)。
a.步骤5为打开弹簧夹,继续通入氮气一段时间后,关闭弹簧夹
b.若去掉步骤5,会使实验结果偏小
c.若去除装置D,会使实验结果偏小
d.若将图中装置BC对调,也可以达到实验目的
查阅资料:①2NaHCO3
 Na2CO3+H2O+CO2↑;NH4HCO3
Na2CO3+H2O+CO2↑;NH4HCO3 NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。②膨松剂的主要成分为碳酸氢铵(NH4HCO3),其他成分受热不分解。
任务一:初识膨松剂
(1)膨松剂能使食品变松软、蓬松。碳酸氢钠可用作膨松剂,其俗名是
任务二:比较膨松效果
| 步骤 | 实验1 | 实验2 |
| 称量 | 10%面粉、0.5g碳酸氢钠置于蒸发皿中 | 10%面粉、0.5g碳酸氢铵置于蒸发皿中 |
| 烘焙 | 模拟烘焙过程,用酒精灯加热约3min,熄灭酒精灯,停止实验 | |
(2)通过以上实验发现,实验2中烘焙的面团更大更松软,原因是反应相同质量碳酸氢钠和碳酸氢铵,后者
任务三:测定某品牌膨松剂中碳酸氢铵的质量分数
甲同学认为,该膨松剂中可能含有水分,会影响实验结果。故他提出可以通过测定反应后生成的某物质质量来达到实验目的。
查阅资料:碱石灰是NaOH与CaO的固体混合物;氨气不与碱石灰反应,能与浓硫酸发生化合反应。
根据资料,他设计了如图所示实验装置及主要步骤(B、C、D中药品均足量)。
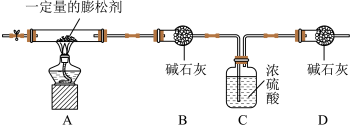
步骤2:打开弹簧夹,通入氮气一段时间后,关闭弹簧夹;
步骤3:称量装置C的质量为m1g;
步骤4:点燃酒精灯,充分反应后停止加热;
步骤5:……;
步骤6:再次称量装置C的质量为m2g。
(3)装置B中发生反应的化学方程式为
(4)该膨松剂中碳酸氢铵的质量分数为
(5)关于该实验,下列说法正确的是
a.步骤5为打开弹簧夹,继续通入氮气一段时间后,关闭弹簧夹
b.若去掉步骤5,会使实验结果偏小
c.若去除装置D,会使实验结果偏小
d.若将图中装置BC对调,也可以达到实验目的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】铜制器物在潮湿环境中表面会产生绿色的锈迹,俗称铜绿。某化学学习小组对铜绿成分产生了浓厚兴趣。
【提出问题】铜绿中除铜元素外还有其它什么元素?
【查阅资料】①无水硫酸铜遇水变蓝色;
②碳与一般的酸不反应;
③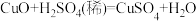 。
。
【实验探究】该小组同学找到了一些铜绿粉末并进行了如下实验:
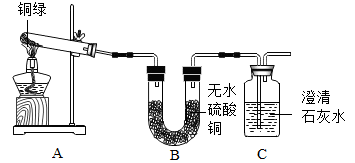
【观察分析】
A.装置中绿色粉末变为黑色;
B.装置中无水硫酸铜变为蓝色;
C.装置中产生的气体使澄清石灰水变浑浊,该反应的化学方程式为_________________ 。
【实验结论】铜绿中除铜元素外还有:_________________ 、_________________ 和碳等元素。
【交流讨论】根据铜绿的组成,小组同学对A装置中产生的黑色粉末的成分有如下两种不同的猜想;
(1)全部为CuO (2)CuO和C的混合物
【深入探究】
【实验结论】化学学习小组同学通过实验证明猜想(1)正确。
【反思应用】根据铜绿中所含元素,可知铜生锈不仅与空气中的氧气、水有关,还可能与空气中的_________________ 等有关;要保护博物馆里的青铜器,减缓生锈,我们可以减少青铜器与_________________ 接触。
【提出问题】铜绿中除铜元素外还有其它什么元素?
【查阅资料】①无水硫酸铜遇水变蓝色;
②碳与一般的酸不反应;
③
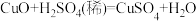 。
。【实验探究】该小组同学找到了一些铜绿粉末并进行了如下实验:

【观察分析】
A.装置中绿色粉末变为黑色;
B.装置中无水硫酸铜变为蓝色;
C.装置中产生的气体使澄清石灰水变浑浊,该反应的化学方程式为
【实验结论】铜绿中除铜元素外还有:
【交流讨论】根据铜绿的组成,小组同学对A装置中产生的黑色粉末的成分有如下两种不同的猜想;
(1)全部为CuO (2)CuO和C的混合物
【深入探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量黑色粉末于试管中,滴加足量的稀硫酸 | 若黑色粉末全部溶解,且溶液由无色变蓝色 | 则:猜想 |
| ②取少量黑色粉末于试管中,滴加足量的稀硫酸 | 若 | 则:猜想(2)正确 |
【实验结论】化学学习小组同学通过实验证明猜想(1)正确。
【反思应用】根据铜绿中所含元素,可知铜生锈不仅与空气中的氧气、水有关,还可能与空气中的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】类比法是化学研究物质的重要方法之一,草酸(H2C2O4)的化学性质与碳酸相似,受热分解后得到三种氧化物。某兴趣小组对草酸的有关性质进行了探究。
【提出猜想】分解得到的三种氧化物可能是CO2、CO和______ (填化学式)。该猜想的依据______ 。
【阅读资料】1、无水硫酸铜是一种白色粉末,遇水变成蓝色。
Ⅱ、向氯化钯溶液中通入CO,会产生黑色沉淀。
【实验探究】兴趣小组为验证猜想,将草酸受热后得到的气体,依次通过如图的A、B、C装置。
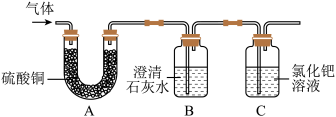
【实验结论】当观察到装置A中变蓝、B中变浑浊、C中______ 的实验现象时,证明猜想是正确的。写出B中发生反应的化学方程式______ 。
【实验反思】①根据实验结论,从环保角度考虑,实验中还有一个缺陷,处理方法是______ 。
②草酸受热分解化学方程式为______ 。
【提出猜想】分解得到的三种氧化物可能是CO2、CO和
【阅读资料】1、无水硫酸铜是一种白色粉末,遇水变成蓝色。
Ⅱ、向氯化钯溶液中通入CO,会产生黑色沉淀。
【实验探究】兴趣小组为验证猜想,将草酸受热后得到的气体,依次通过如图的A、B、C装置。

【实验结论】当观察到装置A中变蓝、B中变浑浊、C中
【实验反思】①根据实验结论,从环保角度考虑,实验中还有一个缺陷,处理方法是
②草酸受热分解化学方程式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组在学习盐的知识时,发现碳酸钠和碳酸钙的组成很相似,他们想知道碳酸钠与稀盐酸反应是否也生成二氧化碳,于是做了如图所示实验.
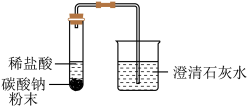
(1)当观察到试管中有气泡产生,烧杯中出现_____ 现象时,由此可以得出结论:碳酸钠与稀盐酸反应也生成二氧化碳,烧杯中发生反应的化学方程式为_____ 。
(2)实验结束后,同学们将试管中的物质倒入烧杯中,发现烧杯中的白色沉淀明显增加,于是他们将烧杯内的物质进行过滤,对所得滤液中的溶质进行了探究。
【问题】滤液中溶质的成分有哪些?
【猜想】甲的猜想:滤液中的溶质是NaCl、NaOH
乙的猜想:滤液中的溶质是NaCl、NaOH、Na2CO3
丙的猜想:滤液中的溶质是NaCl、NaOH、_____ 。
【实验】
【拓展】乙想进一步验证溶质中的氢氧化钠,他的实验方案是:_____ ,(要求写出药品名称、操作步骤、实验现象)。

(1)当观察到试管中有气泡产生,烧杯中出现
(2)实验结束后,同学们将试管中的物质倒入烧杯中,发现烧杯中的白色沉淀明显增加,于是他们将烧杯内的物质进行过滤,对所得滤液中的溶质进行了探究。
【问题】滤液中溶质的成分有哪些?
【猜想】甲的猜想:滤液中的溶质是NaCl、NaOH
乙的猜想:滤液中的溶质是NaCl、NaOH、Na2CO3
丙的猜想:滤液中的溶质是NaCl、NaOH、
【实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,通入二氧化碳气体 | 丙的猜想不成立 | |
| 另取少量滤液于试管中,加入适量的 | 甲的猜想不成立 乙的猜想成立 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组用下图所示装置制备 CO2,并对 Mg 在 CO2 中燃烧生成的白色固体物质进行探究。
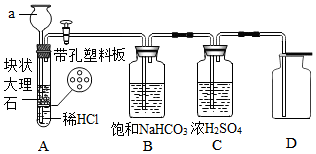
【实验过程】连接好装置并检查装置的气密性,装入药品。打开活塞,让 A 中产生的气体依次通 过 B、C,待气体充满集气瓶后,用坩埚钳夹住长的用砂纸打磨干净的镁条,将镁条点燃后迅速插入到正不断通入 CO2 的集气瓶中,待反应结束后,关闭活塞,即可看到集气瓶内壁和底部有白色固体和黑色固体物质出现。
【查阅资料】①饱和 NaHCO3溶液可以吸收 HCl 而不吸收 CO2;
②MgO、Mg(OH)2、MgCO3均为白色固体。
(1)装置 B 中发生反应的化学方程式是______________ ;
(2)检验 D 中已经充满 CO2的方法是______________ ;
(3)白色固体物质是什么?甲同学提出了三种猜想:
猜想Ⅰ:白色固体物质是 MgO
猜想Ⅱ:白色固体物质是 Mg(OH)2
猜想Ⅲ:白色固体物质是 MgCO3
①上述猜想中,你认为不合理的猜想是______________ (填Ⅰ或Ⅱ或Ⅲ),理由是______________ ;
②乙同学取 D 中的白色固体于试管中,向其中加入足量的稀硫酸,固体溶解,无气泡产生, 据此可知猜想______________ (填Ⅰ或Ⅱ或Ⅲ)是合理的,则镁在 D 中发生反应的化学方程式是_______________ 。

【实验过程】连接好装置并检查装置的气密性,装入药品。打开活塞,让 A 中产生的气体依次通 过 B、C,待气体充满集气瓶后,用坩埚钳夹住长的用砂纸打磨干净的镁条,将镁条点燃后迅速插入到正不断通入 CO2 的集气瓶中,待反应结束后,关闭活塞,即可看到集气瓶内壁和底部有白色固体和黑色固体物质出现。
【查阅资料】①饱和 NaHCO3溶液可以吸收 HCl 而不吸收 CO2;
②MgO、Mg(OH)2、MgCO3均为白色固体。
(1)装置 B 中发生反应的化学方程式是
(2)检验 D 中已经充满 CO2的方法是
(3)白色固体物质是什么?甲同学提出了三种猜想:
猜想Ⅰ:白色固体物质是 MgO
猜想Ⅱ:白色固体物质是 Mg(OH)2
猜想Ⅲ:白色固体物质是 MgCO3
①上述猜想中,你认为不合理的猜想是
②乙同学取 D 中的白色固体于试管中,向其中加入足量的稀硫酸,固体溶解,无气泡产生, 据此可知猜想
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
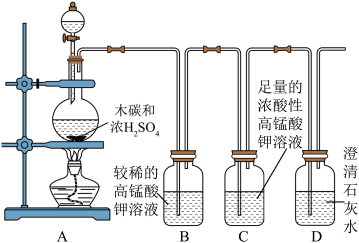
【推荐3】某课外化学兴趣小组发现木炭与浓硫酸加热后产生了气体,该气体有刺激性气味,能使澄清的石灰水变浑浊。同学们在老师的指导下对该气体成分进行了探究。
【提出问题】该气体的成分是什么?
【提出猜想】
猜想一:该气体是CO2 猜想二:该气体是SO2 猜想三:该气体是SO2和CO2
【查阅资料】
①SO2能与酸性高锰酸钾溶液反应,使其褪色;CO2不能与酸性高锰酸钾溶液反应,使其褪色。
②SO2和CO2都能使澄清石灰水变浑浊。
【实验设计】
(1)装置B中酸性高锰酸钾溶液颜色变浅,说明气体中含有___________ (填名称)。装置B后面加装C装置的作用是___________ 。
(2)装置D中澄清石灰水变浑浊,说明气体中含有___________ 。(填化学式)
【实验结论】猜想三成立。
【反思交流】
(3)若装置D位置换到A B之间,其他装置位置不变。对实验分析正确的是___________。
(4)有同学认为,木炭与浓硫酸加热后生成的产物中,除上述已验证的物质外,至少还有一种产物,其可能是___________。
(5)大量的二氧化硫排放到空气中易导致___________ 。(填一种大气污染的名称)
【提出问题】该气体的成分是什么?
【提出猜想】
猜想一:该气体是CO2 猜想二:该气体是SO2 猜想三:该气体是SO2和CO2
【查阅资料】
①SO2能与酸性高锰酸钾溶液反应,使其褪色;CO2不能与酸性高锰酸钾溶液反应,使其褪色。
②SO2和CO2都能使澄清石灰水变浑浊。
【实验设计】
(1)装置B中酸性高锰酸钾溶液颜色变浅,说明气体中含有
(2)装置D中澄清石灰水变浑浊,说明气体中含有
【实验结论】猜想三成立。
【反思交流】
(3)若装置D位置换到A B之间,其他装置位置不变。对实验分析正确的是___________。
| A.若澄清石灰水变浑浊,酸性高锰酸钾溶液颜色变浅也能证明猜想三成立 |
| B.若澄清石灰水变浑浊,酸性高锰酸钾溶液颜色变浅只能得出气体中含有SO2 |
(4)有同学认为,木炭与浓硫酸加热后生成的产物中,除上述已验证的物质外,至少还有一种产物,其可能是___________。
| A.NH3 | B.H2O | C.NO2 | D.N2 |
(5)大量的二氧化硫排放到空气中易导致
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小红和小丽在探究碱的化学性质时,将稀盐酸滴入到氢氧化钠溶液中,意外地看到有气泡产生,她认为氢氧化钠溶液已经变质了。用化学方程式表示氢氧化钠溶液变质的原因:__________ 。
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:_________ 。
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化。
小红认为小丽的实验方案不合理,理由是:________ 。
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
【提出问题】变质后的氢氧化钠溶液中的溶质是什么?
【猜想假设】小丽对变质后的氢氧化钠溶液中的溶质成分做出了两种猜想:
猜想一:碳酸钠;
猜想二:
【实验设计】为验证上述猜想哪个正确,小丽设计了如下方案:取少量氢氧化钠溶液样品于试管中,滴加几滴无色酚酞溶液,观察溶液颜色变化。
小红认为小丽的实验方案不合理,理由是:
【实验与结论】小红另外设计并完成了实验,请你帮她填写下面的实验报告:
| 实验步骤 | 实验现象 | 结论 |
| 步骤1:取少量氢氧化钠溶液样品于试管中,向其中滴加过量的氯化钙溶液 | 猜想一正确 | |
| 步骤2:取步骤1反应后的溶液测定溶液的pH,具体方法是 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】某化学学习小组在老师的指导下,对白色粉笔的成分进行探究。
【提出问题】白色粉笔的主要成分是什么呢?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
【猜想与假设】同学分别做出如下猜想:
A 碳酸钙 B 氢氧化钙 C 硫酸钙 D 氯化钙 E 硝酸钙
同学们根据老师提示并讨论,立即否定了B的猜想,你认为理由是________ .
【查阅资料】
(1)硫酸钙是自然界中石膏矿的主要成分,为白色固体,微溶于水.
(2)室温下几种物质的溶解度
【进行实验】
请写出③中发生反应的化学方程式___________ .
【拓展延伸】为了测定生石膏的组成(CaSO4·xH2O),即测定x的值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下,并利用数据绘制的图象如图所示。
查阅资料:含结晶水的硫酸钙有两种组成形式,在加热过程中,分步失去结晶水,最终得到硫酸钙固体。
(1)AB段固体质量不变的原因__________ 。
(2)利用实验数据,计算x=________ .
(3)图中CD段固体物质的化学式_____________ .
【提出问题】白色粉笔的主要成分是什么呢?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
【猜想与假设】同学分别做出如下猜想:
A 碳酸钙 B 氢氧化钙 C 硫酸钙 D 氯化钙 E 硝酸钙
同学们根据老师提示并讨论,立即否定了B的猜想,你认为理由是
【查阅资料】
(1)硫酸钙是自然界中石膏矿的主要成分,为白色固体,微溶于水.
(2)室温下几种物质的溶解度
| 物质 | 碳酸钙 | 氯化钙 | 硫酸钙 | 硝酸钙 |
| 溶解度/g | 0.0013 | 74.5 | 0.3 | 138 |
【进行实验】
| 实验操作 | 现象 | 结论 | |
| ① | 取少量白色粉笔研碎于试管中,加入 | 无现象 | A不成立 |
| ② | 取少量白色粉笔研碎于烧杯中,加入少量水,搅拌 | 固体没有明显减少 | |
| ③ | 将②进行 | 产生白色沉淀,沉淀不消失 | C成立 |
请写出③中发生反应的化学方程式
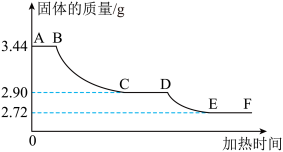
【拓展延伸】为了测定生石膏的组成(CaSO4·xH2O),即测定x的值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下,并利用数据绘制的图象如图所示。
查阅资料:含结晶水的硫酸钙有两种组成形式,在加热过程中,分步失去结晶水,最终得到硫酸钙固体。
实验顺序 (按序延长加热时间) | 固体质量/g | |
加热前 | 加热后 | |
1 | 3.44 | 3.26 |
2 | 3.44 | 3.12 |
3 | 3.44 | 2.90 |
4 | 3.44 | 2.90 |
5 | 3.44 | 2.80 |
6 | 3.44 | 2.78 |
7 | 3.44 | 2.72 |
8 | 3.44 | 2.72 |

(1)AB段固体质量不变的原因
(2)利用实验数据,计算x=
(3)图中CD段固体物质的化学式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图)。
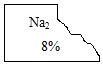
【猜想与假设】
小宁:可能是氢氧化钠溶液
小静:可能是(1)__________ 溶液
小致:可能是(2)__________ 溶液
小远同学认为小宁的猜想不可能,原因是(3)__________ 。
【实验探究】
【反思与评价】
标签为什么会破损,小静同学想测定该溶液的酸碱度,她的操作步骤是:(6)__________ 。测得溶液的pH,(7) __________ (选填>7,=7或<7),溶液显 __________ 性(选填酸性、中性或碱性)致使标签破损。

【猜想与假设】
小宁:可能是氢氧化钠溶液
小静:可能是(1)
小致:可能是(2)
小远同学认为小宁的猜想不可能,原因是(3)
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| 取该溶液少许,滴加(4) | 有气泡产生 | (5) |
【反思与评价】
标签为什么会破损,小静同学想测定该溶液的酸碱度,她的操作步骤是:(6)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】学习化学的重要途径之一是科学探究,请你完成以下探究活动。
【探究活动一】现有含有泥沙等不溶性杂质和少量Na2SO4、MgCl2、CaCl2等可溶性杂质的粗盐样品,某实验小组对粗盐样品进行提纯,并利用所得精盐配制氯化钠溶液。
步骤如下:取样加足量水溶解,先加入过量Ba(OH)2溶液,再加入过量的Na2CO3溶液,充分反应后过滤,得到滤渣和滤液,向滤液中加入足量稀盐酸后,蒸发结晶,得到精盐。
回答下列问题:
(1)Na2CO3溶液的作用是___________ 。
(2)滤渣的成分有___________ 种。
(3)写出加入稀盐酸后发生反应的化学方程式___________ 。
(4)利用所得精盐配制50g质量分数为15%的氯化钠溶液,需要NaCl的质量为___________ 。
(5)对配制溶液进行检测发现质量分数偏大,其原因可能为___________。
【探究活动二】化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶液,同学们对溶质的成分产生了探究的欲望。
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】猜想一:NaOH溶液部分变质 猜想二:NaOH溶液完全变质
【实验探究】
(6)氢氧化钠溶液变质的原因为___________ (用化学方程式表示)。
(7)小华设计了如下实验进行探究,请根据表中内容填写:
若步骤一与步骤二顺序调换___________ (填“是”或“否”)得出正确结论
【实验反思】
(8)下列物质中不能替代步骤一中所加试剂的是___________ (填序号)。
①BaCl2溶液 ②Ca(NO3)2溶液 ③Ca(OH)2溶液 ④Ba(OH)2溶液
(9)步骤二中用另外一种试剂代替酚酞溶液也能得出同样的结论,发生反应的化学方程式___ 。
【探究活动一】现有含有泥沙等不溶性杂质和少量Na2SO4、MgCl2、CaCl2等可溶性杂质的粗盐样品,某实验小组对粗盐样品进行提纯,并利用所得精盐配制氯化钠溶液。
步骤如下:取样加足量水溶解,先加入过量Ba(OH)2溶液,再加入过量的Na2CO3溶液,充分反应后过滤,得到滤渣和滤液,向滤液中加入足量稀盐酸后,蒸发结晶,得到精盐。
回答下列问题:
(1)Na2CO3溶液的作用是
(2)滤渣的成分有
(3)写出加入稀盐酸后发生反应的化学方程式
(4)利用所得精盐配制50g质量分数为15%的氯化钠溶液,需要NaCl的质量为
(5)对配制溶液进行检测发现质量分数偏大,其原因可能为___________。
| A.称量时药品和砝码放反了 | B.取水时俯视读数 |
| C.砝码生锈 | D.装瓶时有少量溶液洒 |
【探究活动二】化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶液,同学们对溶质的成分产生了探究的欲望。
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】猜想一:NaOH溶液部分变质 猜想二:NaOH溶液完全变质
【实验探究】
(6)氢氧化钠溶液变质的原因为
(7)小华设计了如下实验进行探究,请根据表中内容填写:
| 实验步骤 | 现象 | 结论 | |
| 步骤一 | 取少量NaOH溶液样品于试管中,向其中滴加足量的氯化钙溶液。 | 产生白色沉淀 | 猜想 |
| 步骤二 | 过滤,向滤液中滴加酚酞溶液。 | 酚酞溶液变红 | |
【实验反思】
(8)下列物质中不能替代步骤一中所加试剂的是
①BaCl2溶液 ②Ca(NO3)2溶液 ③Ca(OH)2溶液 ④Ba(OH)2溶液
(9)步骤二中用另外一种试剂代替酚酞溶液也能得出同样的结论,发生反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】今年,我们偃师市的好多农村也通上了天然气,某化学兴趣小组的同学对天然气(主要成分是甲烷)燃烧的产物产生了兴趣,设计实验探究:
【提出问题】天然气燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃统生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人缺氧中毒。
【猜想与假设】猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
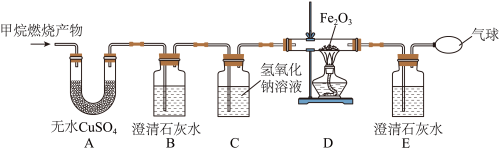
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想_____ 成立。
(2)实验过程中B装置的作用是_____ ;该反应的化学方程式是_____ 。
(3)D装置中发生反应的化学方程式是_____ 。
(4)实验过程中用纯净O2,而不用空气的原因是_____ 。
(5)实验过程中B、C装置的顺序不能颠倒,原因是_____ 。
(6)【反思与交流】日常生活中,使用含碳燃料一定要注意通风,防止_____ 中毒。
(7)实验所需纯净的O2,可用氯酸钾制备,请计算制备4.85gO2需要多少氯酸钾?_____ (写出计算过程,计算结果保留一位小数)
【提出问题】天然气燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃统生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人缺氧中毒。
【猜想与假设】猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:

(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想
(2)实验过程中B装置的作用是
(3)D装置中发生反应的化学方程式是
(4)实验过程中用纯净O2,而不用空气的原因是
(5)实验过程中B、C装置的顺序不能颠倒,原因是
(6)【反思与交流】日常生活中,使用含碳燃料一定要注意通风,防止
(7)实验所需纯净的O2,可用氯酸钾制备,请计算制备4.85gO2需要多少氯酸钾?
您最近一年使用:0次
【推荐3】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图1),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
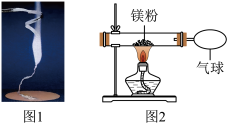
(1)请写出镁条燃烧的化学方程式______ ;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:______ ;
(3)小红按图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】①氮化镁中氮元素的化合价是______ ;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:______ 。
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:______ 。

(1)请写出镁条燃烧的化学方程式
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:
(3)小红按图2装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 向一干净试管中加入少量黄色固体,并加入少量水,试管口放湿润的红色石蕊试纸,观察现象。 |
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:
③同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识:
您最近一年使用:0次



