(已知:氯化钠在 20℃时的溶解度是36g,在90℃的溶解度是39g)
(1)将26%的氯化钠溶液与10%的氯化钠溶液等质量混合后升温至90℃溶质质量分数是________
(2)取上述溶液10g与28%的氯化钠溶液90g混合后降温到20℃,此时溶液的溶质质量分数是_________ (精确到0.1%)
(1)将26%的氯化钠溶液与10%的氯化钠溶液等质量混合后升温至90℃溶质质量分数是
(2)取上述溶液10g与28%的氯化钠溶液90g混合后降温到20℃,此时溶液的溶质质量分数是
更新时间:2022-08-07 05:47:57
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】鲁巴同学在实验室用一定量的氯酸钾和二氧化锰混合物制取氧气,加热至固体质量不再减少时,称得固体残渣质量为20.4g,为了分离出二氧化锰,她向残渣中加入40℃的水30g,充分溶解,第一次过滤后得到滤液A和8.4g残渣,她又向残渣中加入40℃的水10g,充分溶解,第二次过滤后得到滤液B和5.5g残渣(已知:氯酸钾、氯化钾易溶于水,二氧化锰难溶于水。假设在实验过程中药品无损失)。请回答下列问题:
(1)上述反应的方程式为______ ;
(2)5.5g残渣的成分是______ (填化学式);
(3)40℃时,在10g的水中最多能溶解氯化钾的质量为______ g。
(1)上述反应的方程式为
(2)5.5g残渣的成分是
(3)40℃时,在10g的水中最多能溶解氯化钾的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】如表是 NaCl、NH4Cl 在不同温度时的溶解度。
(1)以上两种物质的溶解度受温度影响较大的是_____。
(2)40℃时,将 40.6g NaCl 加入到 100g 水中,充分搅拌使之溶解,所得溶液的质量为_____g。
(3)20℃时,NaCl 饱和溶液的溶质质量分数为(精确到小数点后 1 位)。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(1)以上两种物质的溶解度受温度影响较大的是_____。
(2)40℃时,将 40.6g NaCl 加入到 100g 水中,充分搅拌使之溶解,所得溶液的质量为_____g。
(3)20℃时,NaCl 饱和溶液的溶质质量分数为(精确到小数点后 1 位)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】氯化钠、碳酸钠不同温度下的溶解度如下表所示,请回答下列问题:
(1)20℃时,30g碳酸钠和30g氯化钠的固体混合物加入到100g水中,充分搅拌后_____(填“是”或“否”)有固体剩余。
(2)生活在盐湖附近的人们“夏天晒盐(氯化钠)”、“冬天捞碱(碳酸钠)”,其冬天捞碱依据的原理是___________(填“蒸发结晶”或“降温结晶”)。
(3)将300g碳酸钠溶液和150g石灰水溶液混合后,恰好完全反应,过滤,得到白色沉淀50g,则所得的滤液中溶质的质量分数多少_____________?。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 碳酸钠 | 7.0 | 12.5 | 21.5 | 39.7 | 49.0 |
| 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | |
(1)20℃时,30g碳酸钠和30g氯化钠的固体混合物加入到100g水中,充分搅拌后_____(填“是”或“否”)有固体剩余。
(2)生活在盐湖附近的人们“夏天晒盐(氯化钠)”、“冬天捞碱(碳酸钠)”,其冬天捞碱依据的原理是___________(填“蒸发结晶”或“降温结晶”)。
(3)将300g碳酸钠溶液和150g石灰水溶液混合后,恰好完全反应,过滤,得到白色沉淀50g,则所得的滤液中溶质的质量分数多少_____________?。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】按照我国《食品添加剂使用标准(GB2760﹣2014)》,合理使用SO2不会对人体健康造成危害。如葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化。《标准》中部分食品SO2的最大残留量如表:
兴趣小组同学用高锰酸钾溶液对某品牌白葡萄酒中SO2的残留量进行测定(SO2能使高锰酸钾溶液褪色),反应的化学原理为: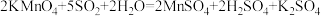 。
。
实验步骤如下:
步骤1:配制高锰酸钾溶液:将20g7.9%高锰酸钾溶液稀释成0.395%的高锰酸钾溶液,需要加水___________ g。
步骤2:取10g0.395%的高锰酸钾溶液于烧杯中,缓缓加入该品牌白葡萄酒,边加边搅拌,当加入100mL白葡萄酒时,高锰酸钾溶液恰好褪色。
通过计算说明该品牌葡萄酒中SO2的残留量是否符合标准___________ 。
| 食品 | 蜜饯 | 葡萄酒 | 巧克力 | 果蔬汁 |
| 最大残留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.05g/kg |
兴趣小组同学用高锰酸钾溶液对某品牌白葡萄酒中SO2的残留量进行测定(SO2能使高锰酸钾溶液褪色),反应的化学原理为:
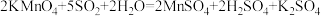 。
。实验步骤如下:
步骤1:配制高锰酸钾溶液:将20g7.9%高锰酸钾溶液稀释成0.395%的高锰酸钾溶液,需要加水
步骤2:取10g0.395%的高锰酸钾溶液于烧杯中,缓缓加入该品牌白葡萄酒,边加边搅拌,当加入100mL白葡萄酒时,高锰酸钾溶液恰好褪色。
通过计算说明该品牌葡萄酒中SO2的残留量是否符合标准
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】氯化钠是工农业生产和生活中的重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题:
(1)m=______ 。
(2)农业上常用16%的氯化钠溶液选种。实验室有100g溶质质量分数为20%的氯化钠溶液,欲将其稀释成可以选种的溶液,需加水的体积是多少?(水的密度为1g/mL,请写出计算过程)
| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
① | 10 | 2 | 12 |
② | 10 | 3 | 13 |
③ | 10 | 4 | 13.6 |
④ | 10 | 5 | m |
(2)农业上常用16%的氯化钠溶液选种。实验室有100g溶质质量分数为20%的氯化钠溶液,欲将其稀释成可以选种的溶液,需加水的体积是多少?(水的密度为1g/mL,请写出计算过程)
您最近一年使用:0次




