计算:84消毒液是一种广泛灭菌消毒剂,常用于学校、幼儿园、车站等公共场所,其有效成分为次氯酸钠(NaClO)工业制取次氯酸钠的化学方程式是Cl2+2NaOH=NaClO+NaCl+H2O。
(1)次氯酸钠中,氯元素的化合价为_____ 。
(2)次氯酸钠能与水反应生成次氯酸,次氯酸很不稳定,在光照的条件下,发生如下反应:2HClO 2HCl+X↑,X的化学符号是
2HCl+X↑,X的化学符号是 _____ ,该反应的基本反应类型为 _____ 。
(3)根据化学方程式计算,要制得74.5g次氯酸钠需要Cl2的质量是多少?
(1)次氯酸钠中,氯元素的化合价为
(2)次氯酸钠能与水反应生成次氯酸,次氯酸很不稳定,在光照的条件下,发生如下反应:2HClO
 2HCl+X↑,X的化学符号是
2HCl+X↑,X的化学符号是 (3)根据化学方程式计算,要制得74.5g次氯酸钠需要Cl2的质量是多少?
更新时间:2022-08-10 09:42:22
|
相似题推荐
【推荐1】《功勋》讲述了共和国勋章获得者的精彩故事——黄旭华的潜艇梦。

(1)黄旭华被誉为中国核潜艇之父。“氧烛”常用作潜艇紧急供氧设备(如图)。使用时,产氧药块中的氯酸钠(NaClO3)受热并在二氧化锰的催化下生成氯化钠并放出氧气。该反应的符号表达式为:_______ ,属于_______ (填基本反应类型)反应。
(2)某型号“氧烛"中约含氯酸钠(NaClO3)10.65 kg,宪全反应后氯酸钠中氧元素全部转化为氧气,理论上可生成_______ kg 氧气。

(1)黄旭华被誉为中国核潜艇之父。“氧烛”常用作潜艇紧急供氧设备(如图)。使用时,产氧药块中的氯酸钠(NaClO3)受热并在二氧化锰的催化下生成氯化钠并放出氧气。该反应的符号表达式为:
(2)某型号“氧烛"中约含氯酸钠(NaClO3)10.65 kg,宪全反应后氯酸钠中氧元素全部转化为氧气,理论上可生成
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】为了节能减排,科学家发明了一种以某种镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4]为原料的新型绿色水泥。全球镁硅酸盐储量丰富,新型绿色水泥不必担心原材料,推广潜力很大。新型绿色水泥与传统水泥对比如图。
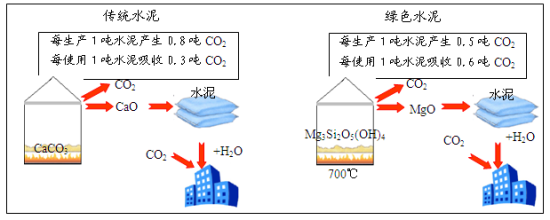
(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3 CaO+ CO2↑ Mg3Si2O5(OH)4
CaO+ CO2↑ Mg3Si2O5(OH)4 3MgO + 2SiO2 + 2H2O↑
3MgO + 2SiO2 + 2H2O↑
以上两个反应都属于___ (填写基本反应类型)。
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放___ 吨二氧化碳。
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?已知该石灰石中碳酸钙含量为80%,杂质不反应。

(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3
 CaO+ CO2↑ Mg3Si2O5(OH)4
CaO+ CO2↑ Mg3Si2O5(OH)4 3MgO + 2SiO2 + 2H2O↑
3MgO + 2SiO2 + 2H2O↑以上两个反应都属于
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?已知该石灰石中碳酸钙含量为80%,杂质不反应。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】汽车的安全气囊内有叠氮化钠(NaN3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊。
(1)叠氮化钠分解的原理可表示为:2NaN3 3N2↑+2X,X的化学式是
3N2↑+2X,X的化学式是_______ 。NaN3中氮元素的质量分数为________ (精确到0.1%)。
(2)某安全气囊中有130g叠氮化钠,若完全反应可生成氮气的质量是多少?________
(1)叠氮化钠分解的原理可表示为:2NaN3
 3N2↑+2X,X的化学式是
3N2↑+2X,X的化学式是(2)某安全气囊中有130g叠氮化钠,若完全反应可生成氮气的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业上用N2和H2合成NH3,进而制备出尿素是人类科学技术的一项重大突破。
(1)N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的__________ (选填“物理”或“化学”)性质;
(2)一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为__________ (填化学式);

NH3与氰酸(HOCN)反应生成尿素CO(NH2)2;
(3)尿素可用于做氮肥,也可用于去除大气污染物中的NO,其化学反应为 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
解:设需要10%的尿素溶液的质量为x。

①的数值为_______
列出比例式,求解__________
求算10%的尿素溶液的质量m为__________ (列式并计算出结果)
答:略。
(1)N2可通过分离液态空气获得,该方法利用了N2和O2沸点的差异。沸点属于物质的
(2)一定条件下,向容器中充入一定量的N2和H2,充分反应生成NH3。反应前后物质的变化如图,图中X代表的分子为

NH3与氰酸(HOCN)反应生成尿素CO(NH2)2;
(3)尿素可用于做氮肥,也可用于去除大气污染物中的NO,其化学反应为
 。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)
。若去除废气中6gNO,理论上所需质量分数为10%的尿素溶液的质量是多少?(请补全计算过程)解:设需要10%的尿素溶液的质量为x。

①的数值为
列出比例式,求解
求算10%的尿素溶液的质量m为
答:略。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知2.45g氯酸钾与适量二氧化锰加热至完全反应可生成氧气0.96g。小明同学在实验室用4.9g氯酸钾和1g二氧化锰的混合物共热至不再产生气体为止。请问:
(1)小明将反应后试管中的剩余物质倒入水中(二氧化锰难溶于水),过滤、烘干,能得到黑色固体_____ 克。
(2)小明可收集到多少克氧气?
(3)这些氧气的体积是多少升?(氧气的密度约为1.43g/L)(计算结果保留2位小数)
(1)小明将反应后试管中的剩余物质倒入水中(二氧化锰难溶于水),过滤、烘干,能得到黑色固体
(2)小明可收集到多少克氧气?
(3)这些氧气的体积是多少升?(氧气的密度约为1.43g/L)(计算结果保留2位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室里用过氧化氢溶液和二氧化锰混合制氧气.现将1.0g二氧化锰放入盛有20.0g过氧化氢溶液的锥形瓶中,立即塞紧带导管的橡胶塞,反应结束,剩余物的质量为20.2g。请计算:
(1)生成氧气的质量为_________ g。
(2)计算参加反应的过氧化氢的质量。
(3)计算过氧化氢溶液中过氧化氢的质量分数。
(1)生成氧气的质量为_________ g。
(2)计算参加反应的过氧化氢的质量。
(3)计算过氧化氢溶液中过氧化氢的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为了研究图1装置的工作原理,在装置左侧连接压强传感器,测定制取氢气过程中的压强变化,结果如图2所示。

(1)图二中cd段变化对应的实验操作是_______ 。
(2)实验室用锌粒和稀硫酸制取 氢气,求参加反应的锌粒的质量。
氢气,求参加反应的锌粒的质量。

(1)图二中cd段变化对应的实验操作是
(2)实验室用锌粒和稀硫酸制取
 氢气,求参加反应的锌粒的质量。
氢气,求参加反应的锌粒的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】氮元素有多种化合价,也能形成多种常见的物质。如:N2、NH4Cl、N2O3、NO2、NO等。试回答相关问题:
(1)将上述五种含氮物质按氮元素化合价由高到低排列_____。
(2)氮气(N2)的相对分子质量为_____。
(3)氯化铵(NH4Cl)中各元素的质量比为_____。
(4)计算五氧化二氮(N2O5)中氮元素的质量分数(精确到0.1%)。_____
(1)将上述五种含氮物质按氮元素化合价由高到低排列_____。
(2)氮气(N2)的相对分子质量为_____。
(3)氯化铵(NH4Cl)中各元素的质量比为_____。
(4)计算五氧化二氮(N2O5)中氮元素的质量分数(精确到0.1%)。_____
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨全不怕,要留清白在人间。”《石灰吟》一诗借物喻人,托物寄怀,此诗涉及石灰石的相关变化,石灰石的主要成分是碳酸钙(CaCO3),请回答下列问题。
(1)碳酸钙的相对分子质量是_______ ;碳酸钙中碳元素的化合价为_______ ;碳酸钙是属于_______ (填序号:A.混合物B.氧化物C.化合物D.单质E.纯净物)。
(2)碳酸钙中钙元素和氧元素的质量比为_______ (填最简整数比)。
(3)碳酸钙也可以用作补钙剂,如图为某钙片的商品信息标签,若某同学每天服用一片这种钙片,他每天至少摄入钙元素的质量为多少?(写出计算过程)
| xx钙片 【主要成分】碳酸钙维生素D 【功效】补钙 【规格】3g/片 每片中含:碳酸钙≥2g 【食用方法】嚼服 |
(2)碳酸钙中钙元素和氧元素的质量比为
(3)碳酸钙也可以用作补钙剂,如图为某钙片的商品信息标签,若某同学每天服用一片这种钙片,他每天至少摄入钙元素的质量为多少?(写出计算过程)
您最近一年使用:0次

 2B(OH)3+3H2↑,请计算:
2B(OH)3+3H2↑,请计算: Mg+Cl2↑。请计算:
Mg+Cl2↑。请计算:

