某兴趣小组在实验室用氯化钙溶液测定某未知浓度的碳酸钠溶液的溶质质量分数。实验过程和数据如下:将50g碳酸钠溶液和55g氯化钙溶液混合,恰好完全反应后过滤,得到100g 滤液和一定质量的滤渣。请计算:
(1)反应生成的滤渣质量是______ g。
(2)求该碳酸钠溶液的溶质质量分数。
(1)反应生成的滤渣质量是
(2)求该碳酸钠溶液的溶质质量分数。
更新时间:2022-09-26 09:39:02
|
相似题推荐
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】工业上侯氏制碱法得到的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,实验数据如下表:
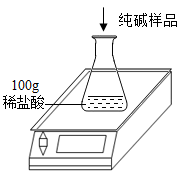
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是__g.
(2)计算纯碱样品中碳酸钠的质量分数是_______?(计算结果精确到0.1%)
(3)计算所用稀盐酸的质量分数是____________?

| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(2)计算纯碱样品中碳酸钠的质量分数是_______?(计算结果精确到0.1%)
(3)计算所用稀盐酸的质量分数是____________?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
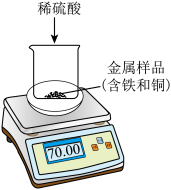
【推荐2】某金属加工厂有大量的成分为铁、铜的金属粉末。为测定该铁、铜金属粉末中铜粉的含量,取20g样品于烧杯中并称量,如图所示,将150g稀硫酸等分为三份依次加入烧杯中,反应过程中记录天平示数如表所示。请计算:
(1)反应过程产生氢气的总质量是_________ g。
(2)样品中铜粉的质量分数。
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 天平示数(g) | 119.75 | 169.50 | 219.50 |
(1)反应过程产生氢气的总质量是
(2)样品中铜粉的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】.某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数, 20℃时,称取该产品样品 26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和 NaCl 溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。

(1)该纯碱样品中 Na2CO3的质量分数_________ 。
(2)根据条件,此题还可求算出下列中的 (只填字母标号,不计算,可多选)。

(1)该纯碱样品中 Na2CO3的质量分数
(2)根据条件,此题还可求算出下列中的 (只填字母标号,不计算,可多选)。
| A.该纯碱样品中 NaCl 的质量分数 |
| B.反应所用稀盐酸的溶质质量分数 |
| C.反应后所得溶液中 NaCl 的质量分数 |
| D.反应生成水的质量 |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】 某化工厂排放的废水中含有一定量的氢氧化钾,为了回收利用,欲用2%的稀盐酸测定废水中的氢氧化钾含量(废水中其他杂质不与盐酸反应,反应的化学方程式为:HCl+KOH=KCl+H2O)
(1)用10 g30%的浓盐酸配制成2%的稀盐酸,需加水________g。
(2)取20g废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3g,求废水中氢氧化钾的质量分数。
(1)用10 g30%的浓盐酸配制成2%的稀盐酸,需加水________g。
(2)取20g废水于锥形瓶中,逐滴加入2%的稀盐酸,至恰好完全反应时,消耗稀盐酸7.3g,求废水中氢氧化钾的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室中稀硫酸因标签破损,需测定其质量分数。某化学兴趣小组的同学取该稀硫酸样品100g,逐滴加入质量分数为16%的NaOH溶液,溶液的pH随加入NaOH溶液质量的变化如下图所示。求稀硫酸中溶质的质量分数。
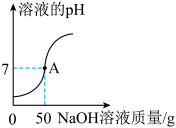

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】分析数据,获得信息实验室现有硫酸铜和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸铜的质量分数。先称取该混合物样品 25g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液 100g 平均分四次加入其中,充分振荡,相关实验数据记录如下:
请回答下列问题:
(1)上表中 X 的数值为_____________;
(2)计算原固体混合物样品中硫酸铜的质量分数为_____________? (写出计算步骤)
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
| 生成沉淀的质量/g | 4.9 | 9.8 | X | 14.7 |
请回答下列问题:
(1)上表中 X 的数值为_____________;
(2)计算原固体混合物样品中硫酸铜的质量分数为_____________? (写出计算步骤)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某纯碱样品的主要成分是碳酸钠(Na2CO3)和氯化钠(NaC1),为测定该纯碱样品中碳酸钠的质量,小明进行如下实验:
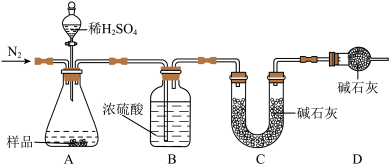
(1)现取一定量的纯碱产品,按照如图装置进行实验,C装置增重4.4g,试计算该产品中碳酸钠的质量(写出计算过程)。
(2)实验装置中若去除B装置,可能造成的影响是______ 。

(1)现取一定量的纯碱产品,按照如图装置进行实验,C装置增重4.4g,试计算该产品中碳酸钠的质量(写出计算过程)。
(2)实验装置中若去除B装置,可能造成的影响是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】电导率是衡量电解质溶液导电能力大小的物理量.溶液电导率大小变化可以反映电解质溶液中离子浓度的大小变化。下图是向100mL一定溶质质量分数的Ba(OH)2溶液中分别滴加稀H2SO4溶液和稀Na2SO4溶液的过程中溶液电导率随时间变化图。回答下列问题。
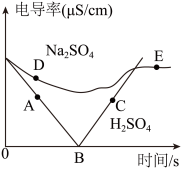
(1)写出Ba(OH)2与H2SO4反应的化学方程式_______________。
(2)若在图中A-E各点对应的溶液中滴加酚酞,则溶液呈红色的有____________。
(3) D-→E的反应过程中,溶液中数目始终增多的微粒有___________。
(4)经测定,B点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数__________(写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。

(1)写出Ba(OH)2与H2SO4反应的化学方程式_______________。
(2)若在图中A-E各点对应的溶液中滴加酚酞,则溶液呈红色的有____________。
(3) D-→E的反应过程中,溶液中数目始终增多的微粒有___________。
(4)经测定,B点时消耗稀H2SO4溶液50mL,且过滤后滤液质量为147. 67g。请计算原Ba(OH)2溶液的溶质质量分数__________(写出计算过程,各种稀溶液的密度都可看成1g·mL-1)。
您最近一年使用:0次

 。现将15.6g过氧化钠固体投入67.6g过量的水中充分反应,试计算:
。现将15.6g过氧化钠固体投入67.6g过量的水中充分反应,试计算:

