计算下列问题
(1)图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷(白磷在40℃时可以燃烧),将它放在盛有沸水的上方,进行实验。请完成实验报告:
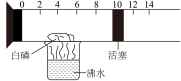
①实验现象:白磷着火燃烧,___________ 放出热量,生成白色固体:活塞先向右移,后向左移,最后停在刻度约为___________ (填整数)的位置上。反应的符号表达式是:___________ 。
②实验结论:空气的成分按体积计算,测定氧气约占空气的___________ 。
(2)富马酸亚铁(C4H2FeO4)可用于缺铁性贫血症的治疗,请计算:
富马酸亚铁中铁元素的质量分数是___________ (计算结果精确到0.1%)
(3)计算60kgNH4NO3中含氮元素多少kg?(写出计算过程)
(1)图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷(白磷在40℃时可以燃烧),将它放在盛有沸水的上方,进行实验。请完成实验报告:

①实验现象:白磷着火燃烧,
②实验结论:空气的成分按体积计算,测定氧气约占空气的
(2)富马酸亚铁(C4H2FeO4)可用于缺铁性贫血症的治疗,请计算:
富马酸亚铁中铁元素的质量分数是
(3)计算60kgNH4NO3中含氮元素多少kg?(写出计算过程)
更新时间:2022-11-23 09:15:31
|
相似题推荐
综合应用题
|
较易
(0.85)
解题方法
【推荐1】“逐梦苍穹之上,拥抱星辰大海”,嫦娥探月、天舟升空、蛟龙潜海,都离不开化学。
(1)运载火箭使用的燃料有煤油、液氢等,生产煤油的原料是_______ (填“煤”或“石油”),氢气目前没有广泛应用的原因有_______ (填字母序号)。
A.制取成本高
B.产物无污染
C.热值高
D.贮存困难
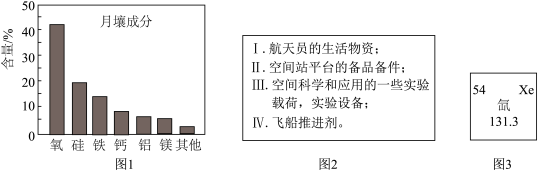
(2)嫦娥5号月球探测器带回的月壤样品成分分析结果如图1,这里的“氧、硅、铁..”是指_______ (填“分子”、“原子”或“元素”)。
(4)5月11日,天舟六号货运飞船成功对接中国太空站,如图2是此次运送的物资单。
①生活物资中包含约70公斤的新鲜水果,可以为宇航员补充的营养素是_______ ,调节新陈代谢、维持身体健康。
②氙气是空间站电推进系统的“燃料”,氙在元素周期表中的信息如图3,下列说法不正确的是_______ 。
A.氙的元素符号是Xe
B.氙原子的质子数是54
C.氙属于金属元素
D.氙的相对原子质量是131.3
(5)“蛟龙”号潜水器使用钛合金,工业上用钛铁矿(主要成分FeTiO3)制备金属钛和纳米级Fe3O4的工艺流程如图所示(部分产物略):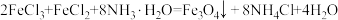
①步骤①反应前需将钛铁矿粉碎的目的是_______ 。
②步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3的_______ 不同。
③反应③属于_______ (填基本反应类型)。
④向FeCl2和盐酸的溶液中通入O2可生成FeCl3和H2O,该反应的化学方程式为_______ 。
⑤步骤⑤需要控制反应温度为不宜过高,其原因是_______ 。“溶解”时,实际投放的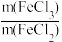 小于理论值,其原因是
小于理论值,其原因是_______ 。
(1)运载火箭使用的燃料有煤油、液氢等,生产煤油的原料是
A.制取成本高
B.产物无污染
C.热值高
D.贮存困难
(2)嫦娥5号月球探测器带回的月壤样品成分分析结果如图1,这里的“氧、硅、铁..”是指
| A.无气体对流 | B.微重力 |
①生活物资中包含约70公斤的新鲜水果,可以为宇航员补充的营养素是
②氙气是空间站电推进系统的“燃料”,氙在元素周期表中的信息如图3,下列说法不正确的是
A.氙的元素符号是Xe
B.氙原子的质子数是54
C.氙属于金属元素
D.氙的相对原子质量是131.3
(5)“蛟龙”号潜水器使用钛合金,工业上用钛铁矿(主要成分FeTiO3)制备金属钛和纳米级Fe3O4的工艺流程如图所示(部分产物略):
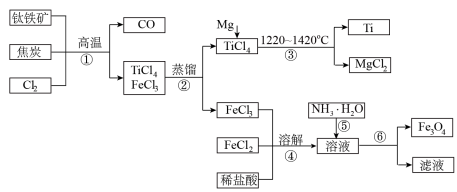
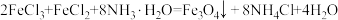
①步骤①反应前需将钛铁矿粉碎的目的是
②步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3的
③反应③属于
④向FeCl2和盐酸的溶液中通入O2可生成FeCl3和H2O,该反应的化学方程式为
⑤步骤⑤需要控制反应温度为不宜过高,其原因是
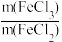 小于理论值,其原因是
小于理论值,其原因是
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐2】《环境空气质量标准》中增加了PM2.5监测指标,PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响更大,主要来源之一是煤、石油等燃料的燃烧。
(1)下列措施能减少PM2.5污染的是 。
(2)下表是福州某日的空气质量日报,三个空气质量监测项目中,会导致酸雨形成的是______ 。
(3)下列有关空气的说法不正确的是 。
(4)安装尾气催化净化装置可以减少汽车尾气对空气污染,其反应原理是利用一氧化碳和一氧化氮在催化剂存在的条件下反应生成氮气和二氧化碳,写出该反应的化学方程式______ 。
(1)下列措施能减少PM2.5污染的是 。
| A.鼓励少开私家车,坐公交车出行 | B.鼓励使用太阳能热水器 |
| C.鼓励用煤火力发电 | D.露天焚烧垃圾、秸秆等 |
| 空气质量监测项目 | 空气质量指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒物 | 65 | Ⅱ | 良 |
| 二氧化硫 | 16 | ||
| 二氧化氮 | 20 |
| A.空气中氮气的质量分数是78% |
| B.二氧化碳是温室效应的主要气体,属于空气污染物 |
| C.空气与人呼出的气体相比:氧气的含量减少,水蒸气和二氧化碳的含量都增大 |
| D.稀有气体可以做为焊接保护气,说明在一般情况下,稀有气体化学性质比较稳定 |
您最近一年使用:0次
综合应用题
|
较易
(0.85)
解题方法
【推荐3】建立宏观、微观和符号之间的联系是化学学科的特点。
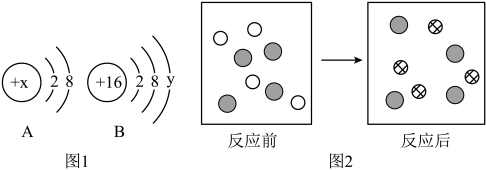
(1)图1分别表示微粒A B的结构示意图,回答下列问题:
①若微粒A是带两个单位正电荷的阳离子,则x的值为____________ ;
②由B原子结构示意图推知,该元素处于元素周期表的第____________ 周期;
③若x=13,则A、B所对应的元素形成化合物的化学式为____________ 。
(2)在硫酸铜溶液中加入过量铁粉的实验中:
①宏观现象:可以观察到溶液颜色变化的现象是____________ ;
②符号表达:写出该反应的化学方程式:___________ ;
③微观理解:图2表示反应前后溶液中的主要离子,已知反应前溶液中含有铜离子、硫酸根离子。则 表示相应离子的符号是
表示相应离子的符号是____________ 。

(1)图1分别表示微粒A B的结构示意图,回答下列问题:
①若微粒A是带两个单位正电荷的阳离子,则x的值为
②由B原子结构示意图推知,该元素处于元素周期表的第
③若x=13,则A、B所对应的元素形成化合物的化学式为
(2)在硫酸铜溶液中加入过量铁粉的实验中:
①宏观现象:可以观察到溶液颜色变化的现象是
②符号表达:写出该反应的化学方程式:
③微观理解:图2表示反应前后溶液中的主要离子,已知反应前溶液中含有铜离子、硫酸根离子。则
 表示相应离子的符号是
表示相应离子的符号是
您最近一年使用:0次
综合应用题
|
较易
(0.85)
【推荐1】在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
(1)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有_____ (填字母序号)。
a.金属原料的成本 b.生产过程中的能耗与污染 c.金属的回收利用
(2)比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学成分的角度分析“磁铁矿作炼铁原料更具优势”,其原因是_____ 。
(3)钛和钛合金是21世纪重要的金属材料。钛合金制品放在海水中数年取出后仍光亮如新,是因为其_____ (填字母序号)非常好。
a.可塑性 b.机械性能 c.抗腐蚀性能
(4)某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如下图所示。
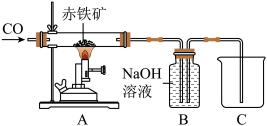
I.为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应_____ 。
II.装置A玻璃管中发生反应的化学方程式是_____ 。
III.装置B除了吸收CO2气体外,还有_____ 作用。
(1)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有
a.金属原料的成本 b.生产过程中的能耗与污染 c.金属的回收利用
(2)比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学成分的角度分析“磁铁矿作炼铁原料更具优势”,其原因是
(3)钛和钛合金是21世纪重要的金属材料。钛合金制品放在海水中数年取出后仍光亮如新,是因为其
a.可塑性 b.机械性能 c.抗腐蚀性能
(4)某兴趣小组在实验室中利用CO气体模拟炼铁的原理,如下图所示。

I.为了避免装置A中玻璃管在加热时可能发生爆炸,加热前应
II.装置A玻璃管中发生反应的化学方程式是
III.装置B除了吸收CO2气体外,还有
您最近一年使用:0次
综合应用题
|
较易
(0.85)
【推荐2】黑木耳是一种营养丰富的食用菌,含有人体必需的钙、铁、胡萝卜素、维生素等营养物质,经常食用可补充人体对铁等微量元素的需求。其中营养成分的具体含量如资料卡片所示。请根据资料回答下列问题:

(1)黑木耳中所含的铁是指___ (填字母序号).
A. 分子 B.原子 C.元素
(2)硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一,请根据其化学式计算:
①硫酸亚铁的相对分子质量为___ ,
②硫酸亚铁中铁、硫、氧三种元素的质量比为___ ;
③与200g干黑木耳中的铁元素质量相等的硫酸亚铁的质量为___ mg.

(1)黑木耳中所含的铁是指
A. 分子 B.原子 C.元素
(2)硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一,请根据其化学式计算:
①硫酸亚铁的相对分子质量为
②硫酸亚铁中铁、硫、氧三种元素的质量比为
③与200g干黑木耳中的铁元素质量相等的硫酸亚铁的质量为
您最近一年使用:0次
综合应用题
|
较易
(0.85)
名校
解题方法
【推荐1】氧气是一种化学性质比较活泼的气体,它可以和许多物质发生反应:

(1)上述三个反应相同是 。(填字母序号)
(2)甲实验,既证明了氧气约占空气总体积的 ,也证明了氮气的化学性质是
,也证明了氮气的化学性质是______________________ 。
(3)乙实验,发生反应的文字表达式是______________________ 。
(4)在做丙实验时,螺旋状铁丝上需系一根火柴,其作用是_________________________________ 。
(5)在做乙、丙两个实验时,事先都需在集气瓶底部装少量水,其作用___________ (选填“相同”或“不相同”),丙中水的作用是____________________________________________ 。
(6)铁丝在空气中不能燃烧,而在纯净的氧气中可以剧烈燃烧,说明可燃物燃烧的剧烈程度与___________ 有关。

(1)上述三个反应相同是 。(填字母序号)
| A.都是化合反应 | B.都是氧化反应 |
| C.生成物都是固体 | D.都需要点燃 |
 ,也证明了氮气的化学性质是
,也证明了氮气的化学性质是(3)乙实验,发生反应的文字表达式是
(4)在做丙实验时,螺旋状铁丝上需系一根火柴,其作用是
(5)在做乙、丙两个实验时,事先都需在集气瓶底部装少量水,其作用
(6)铁丝在空气中不能燃烧,而在纯净的氧气中可以剧烈燃烧,说明可燃物燃烧的剧烈程度与
您最近一年使用:0次
综合应用题
|
较易
(0.85)
【推荐2】空气中氧气含量测定再认识。
(1)利用图1实验装置测定了空气组成的科学家是_______ 。
(2)用图2所示的方法测定空气中氧气的含量,红磷燃烧的化学方程式为________ 。为保证测定结果更准确,实验中所装红磷必须_______ 。
(3)【实验探究】
同学们查阅资料发现白磷40℃即可燃烧,燃烧产物与红磷相同,于是利用图3改进装置重新探究。先在容积为200.0mL的集气瓶中装进50.0mL的水,再在量筒内装入100.0mL的水。然后按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
①实验中没有用到止水夹,只需要在集气瓶里预先装50mL的水,在实验过程中既能够加快集气瓶冷却又能吸收有毒的白烟,还起到的作用是__________ 。
②实验结束时,量筒内剩余水的体积是73.0mL,则计算出空气中氧气体积分数为_________ ,造成这个结果的可能原因是___________ 。
(1)利用图1实验装置测定了空气组成的科学家是
(2)用图2所示的方法测定空气中氧气的含量,红磷燃烧的化学方程式为
(3)【实验探究】
同学们查阅资料发现白磷40℃即可燃烧,燃烧产物与红磷相同,于是利用图3改进装置重新探究。先在容积为200.0mL的集气瓶中装进50.0mL的水,再在量筒内装入100.0mL的水。然后按图连好仪器,按下热的玻璃棒,白磷立即被点燃。
①实验中没有用到止水夹,只需要在集气瓶里预先装50mL的水,在实验过程中既能够加快集气瓶冷却又能吸收有毒的白烟,还起到的作用是
②实验结束时,量筒内剩余水的体积是73.0mL,则计算出空气中氧气体积分数为
您最近一年使用:0次
综合应用题
|
较易
(0.85)
【推荐3】空气是一种宝贵的自然资源,请沿用科学家认识事物的方式认识“空气”。
Ⅰ.从分类角度:洁净的空气属于_____ (填“混合物”或“纯净物”)。
Ⅱ.从微观角度:用“ ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。
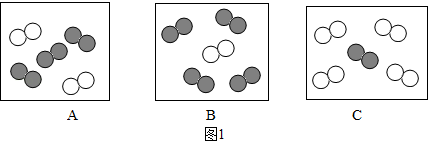
已知:同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图1中可表示空气微观模型的是_____ (填“选项字母”)。
Ⅲ.从变化角度:如图2是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
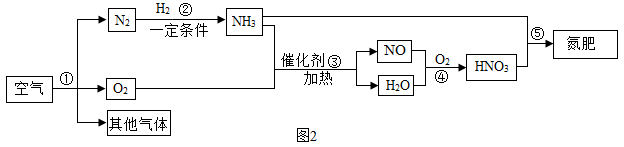
(1)步骤①中发生的是_____ 变化(填“物理”或“化学”)。
(2)写出步骤②中发生反应的文字表达式_______________ 。
(3)绿色化学的实质是从源头上消除污染的环境友好化学,从微观上看是化学反应中原子的利用率达到100%的化学,以实现零排放。在我们已经学过的化学反应类型中化合反应符合这一要求,则上述流程中,符合绿色化学反应理念的反应有_____ 个。
(4)在该氮肥生产的工业流程五个步骤中,其中步骤③和④两步发生的反应的共同点是:两个反应都是_____ 反应。
(5)在化工生产中,常常为了达到目的,需要使用催化剂,下列有关催化剂的说法中,正确的是_____
A化工生产中所使用的催化剂都是用二氧化锰
B化工生产中使用催化剂的目的都是为了加快化学反应速率
C化工生产中使用催化剂是为了得到更多的化工产品
D化工生产中使用的催化剂可重复使用。
Ⅳ.从定量的角度: 用图3所示实验装置测定空气中氧气含量,图4是实验过程中集气瓶内压强变化曲线。
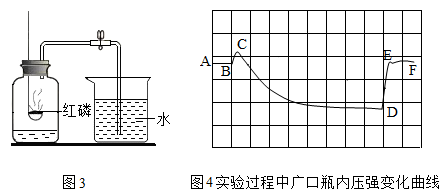
下列说法错误的是________
A图3中发生反应的符号表达式为:P+O2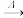 PO2
PO2
B图4中BC段气压变化的原因是烧杯中水进入广口瓶
C图4中CD段气压变化的原因是温度降低至室温、瓶中氧气被消耗
D图4中DE段气压变化的原因是红磷燃烧放热,瓶塞被冲开。
E实验前广口瓶内空气体积为V,烧杯中水的体积为V1;实验后烧杯中剩余水的体积为V2.计算空气中氧气体积分数的表达式为: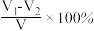 。
。
Ⅰ.从分类角度:洁净的空气属于
Ⅱ.从微观角度:用“
 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子。
”表示氧原子。已知:同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图1中可表示空气微观模型的是

Ⅲ.从变化角度:如图2是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:

(1)步骤①中发生的是
(2)写出步骤②中发生反应的文字表达式
(3)绿色化学的实质是从源头上消除污染的环境友好化学,从微观上看是化学反应中原子的利用率达到100%的化学,以实现零排放。在我们已经学过的化学反应类型中化合反应符合这一要求,则上述流程中,符合绿色化学反应理念的反应有
(4)在该氮肥生产的工业流程五个步骤中,其中步骤③和④两步发生的反应的共同点是:两个反应都是
(5)在化工生产中,常常为了达到目的,需要使用催化剂,下列有关催化剂的说法中,正确的是
A化工生产中所使用的催化剂都是用二氧化锰
B化工生产中使用催化剂的目的都是为了加快化学反应速率
C化工生产中使用催化剂是为了得到更多的化工产品
D化工生产中使用的催化剂可重复使用。
Ⅳ.从定量的角度: 用图3所示实验装置测定空气中氧气含量,图4是实验过程中集气瓶内压强变化曲线。

下列说法错误的是
A图3中发生反应的符号表达式为:P+O2
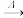 PO2
PO2B图4中BC段气压变化的原因是烧杯中水进入广口瓶
C图4中CD段气压变化的原因是温度降低至室温、瓶中氧气被消耗
D图4中DE段气压变化的原因是红磷燃烧放热,瓶塞被冲开。
E实验前广口瓶内空气体积为V,烧杯中水的体积为V1;实验后烧杯中剩余水的体积为V2.计算空气中氧气体积分数的表达式为:
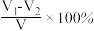 。
。
您最近一年使用:0次




