2022年北京冬奥会举世瞩目,新能源的开发利用践行了我国“绿色办奥”的理念,请回答下列问题。
(1)“雪如意”国家跳台滑雪中心,采用了地表水收集技术,可用积雪融化形成的雪水造雪。雪融化成水,发生变化的是______(填序号,下同)。
(2)北京冬奥会采用CO2跨临界直冷制冰技术(如图一所示)。

①液态CO2蒸发吸热实现制冷,使水变成冰。此过程中,CO2的化学性质并没有改变,原因是______ (从微观的角度解释)。
②超临界状态CO2通过冷却器实现循环,并释放热量为场馆除湿、供热。此技术的优点是______ (写出1点即可)。
(3)场馆“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电。
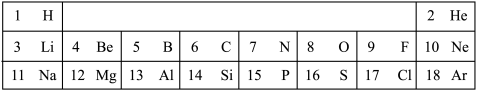
①根据图二信息判断,下列说法正确的是______ 。
A.Te的相对原子质量是127.6g
B.Te原子核内的质子数是52
C.CdTe中Te的化合价是-2价
D.符号“Cd”表示镉元素;一个镉原子;金属镉
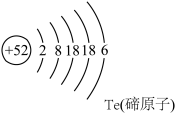
②下图是元素周期表(部分)与碲原子结构示意图。碲元素化学性质与图中______ 元素化学性质相似。碲元素与13号元素形成的化合物化学式为:______ 。
(1)“雪如意”国家跳台滑雪中心,采用了地表水收集技术,可用积雪融化形成的雪水造雪。雪融化成水,发生变化的是______(填序号,下同)。
| A.分子种类 | B.分子间隔 | C.分子质量 |
(2)北京冬奥会采用CO2跨临界直冷制冰技术(如图一所示)。

①液态CO2蒸发吸热实现制冷,使水变成冰。此过程中,CO2的化学性质并没有改变,原因是
②超临界状态CO2通过冷却器实现循环,并释放热量为场馆除湿、供热。此技术的优点是
(3)场馆“冰丝带”是由3360块发电玻璃拼成。发电玻璃是在普通玻璃上覆盖一层碲化镉(化学式CdTe)。碲化镉在弱光照射下也能持续发电。
①根据图二信息判断,下列说法正确的是
A.Te的相对原子质量是127.6g
B.Te原子核内的质子数是52
C.CdTe中Te的化合价是-2价
D.符号“Cd”表示镉元素;一个镉原子;金属镉
②下图是元素周期表(部分)与碲原子结构示意图。碲元素化学性质与图中


更新时间:2022-12-27 21:28:13
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】2023年6月,中国航天捷报频传,神舟十六号顺利升天,神舟十五号成功返回,航天梦,照亮中国科技兴国路,请回答下列问题:
(1)下表为航天器所用的燃料和氧化剂,请回答:
①上述所有物质中属于混合物的有________ (填名称),属于单质的有________ (填化学式)。
②标出高氯酸铵(NH4ClO4)中氯元素的化合价________ 。
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:________ 。
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:
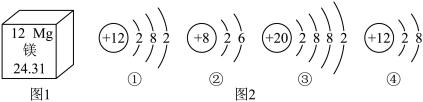
①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为________ 。
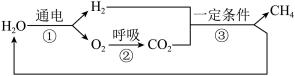
②图2为几种粒子的结构示意图,其中属于同种元素的是________ (填序号,下同),与镁元素化学性质相似的是________ 。
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是________ (填化学式),请写出反应③的化学方程式________ ,空间站内所需要的氧气来自水的电解,若实验室用10%的NaOH溶液配制200g4%的NaOH溶液用于电解实验,则需要10%的NaOH溶液________ g。
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是________ ,此外,在航天服生命保障系统中还常用过氧化钠吸收航天员呼出的CO2,反应原理为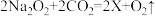 则X的化学式
则X的化学式________ ,若一定时间内航天员所排出CO2的质量为110g,若将其完全吸收,则同时产生氧气的体积为________ 升(通常状况下的氧气密度约为1.4g/L,计算结果精确到0.1),航天员在空间站内不需要穿笨重的航天服也能正常地生活和工作,则空间站为航天员提供的必要条件是________ 。
A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是________ ,返回舱的返回动力来自液氢和液氧,在即将着陆前要迅速释放剩余的燃料,这样做的目的是________ 。(答一点即可)
(1)下表为航天器所用的燃料和氧化剂,请回答:
| 一级火箭 | 二级火箭 | 三级火箭 | 固体燃料 | |
| 燃料 | 煤油 | 液氢 | 偏二甲肼(液态) | 铝粉 |
| 氧化剂 | 液氧 | 液氧 | 四氧化二氮(液态) | 高氯酸铵 |
②标出高氯酸铵(NH4ClO4)中氯元素的化合价
③火箭中偏二甲肼(C2H8N2)与四氧化二氮(N2O4)点燃后,反应生成空气中最多气体和另外两种氧化物,并放出大量的热,请写出其化学方程式为:
(2)宇宙飞船所用的新型材料里其中应用了镁锂合金,请回答下列问题:


①图1为镁在元素周期表中的部分信息,则镁的相对原子质量为
②图2为几种粒子的结构示意图,其中属于同种元素的是
(3)天宫空间站中水气整合系统简易流程如图,该过程中,可循环利用的化合物是
(4)航天员出舱需携带高压氧气罐,并将氧气罐集成到舱外航天服上,氧气可以压缩储存在氧气罐中的微观实质是
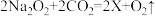 则X的化学式
则X的化学式A.适宜的温度B.纯氧环境 C.饮用水 D.与地球相仿的气压
(5)神舟号载人飞船返回舱返回时,与大气剧烈摩擦,舱表面会产生数千度的高温,此时,舱表面的“烧蚀层”会汽化燃烧保护返回舱不因高温而烧毁。从燃烧的条件解释返回舱不会被烧毁的原因可能是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】水是生活中最常见的物质之一,也是实验室常用的试剂。
(1)长期饮用硬水会影响人体健康,检验自来水是否为硬水常用的物质是___ 。
(2)某工厂用电解水的方法制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味(每个具有鱼腥气味的气体分子由三个原子构成)。从元素守恒角度分析,该鱼腥气味的气体是____ (填化学式)。
(3)硫酸钠溶于水能离解出自由移动的____ 、____ (填符号),因此硫酸钠溶液能导电。
(4)电解水时,在水中加入少量硫酸钠可增强导电性。某兴趣小组把4.0g硫酸钠固体加入86.8g水中,充分溶解后进行电解。一段时间后停止通电,在试管A中收集到1.2g气体(装置如图)。回答下列问题:

①B管中收集到的气体是____ 。
②结合方程式计算,电解后溶液中硫酸钠的质量分数____ 。(写出计算过程)
(1)长期饮用硬水会影响人体健康,检验自来水是否为硬水常用的物质是
(2)某工厂用电解水的方法制取氧气,发现氧气的产量略小于理论值,且所得氧气中有淡淡的鱼腥气味(每个具有鱼腥气味的气体分子由三个原子构成)。从元素守恒角度分析,该鱼腥气味的气体是
(3)硫酸钠溶于水能离解出自由移动的
(4)电解水时,在水中加入少量硫酸钠可增强导电性。某兴趣小组把4.0g硫酸钠固体加入86.8g水中,充分溶解后进行电解。一段时间后停止通电,在试管A中收集到1.2g气体(装置如图)。回答下列问题:

①B管中收集到的气体是
②结合方程式计算,电解后溶液中硫酸钠的质量分数
您最近一年使用:0次
【推荐3】“化”说冬奥会,低碳向未来。
(1)智慧场馆“黑科技”。
①国家游泳中心采用二氧化碳跨临界(气态变为液态)直冷技术将“水立方”转换为“冰立方”。对该过程中的二氧化碳和水的分析正确的是_____ (填标号);
A.水分子体积变小 B.二氧化碳分子停止运动 C.两种分子的间隔均改变
②速滑馆采用“冰丝带”设计可减少使用约三万吨钢材。工业上将生铁冶炼成钢的原理是_____ 。
(2)巧用节能新工艺。
①为减少碳排放,多个赛区使用氢燃料车辆。氢燃料属于清洁能源的理由是_____ ;
②中国自主研发的锂离子动力电池,在-40℃环境下可一键启动新能源汽车。如图为锂在元素周期表中信息,锂元素的相对原子质量为_____ ;

③本次赛场实现所有场馆100%使用绿色电力,减排二氧化碳约33万吨,则可减少燃烧煤(含杂质约28%)_____ 万吨。
(1)智慧场馆“黑科技”。
①国家游泳中心采用二氧化碳跨临界(气态变为液态)直冷技术将“水立方”转换为“冰立方”。对该过程中的二氧化碳和水的分析正确的是
A.水分子体积变小 B.二氧化碳分子停止运动 C.两种分子的间隔均改变
②速滑馆采用“冰丝带”设计可减少使用约三万吨钢材。工业上将生铁冶炼成钢的原理是
(2)巧用节能新工艺。
①为减少碳排放,多个赛区使用氢燃料车辆。氢燃料属于清洁能源的理由是
②中国自主研发的锂离子动力电池,在-40℃环境下可一键启动新能源汽车。如图为锂在元素周期表中信息,锂元素的相对原子质量为

③本次赛场实现所有场馆100%使用绿色电力,减排二氧化碳约33万吨,则可减少燃烧煤(含杂质约28%)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】氧及其化合物与生产生活密切相关,是化学学习和研究的重要内容。
(1)如何验证一瓶无色气体是氧气?
(2)可燃物燃烧的剧烈程度与氧气浓度或接触面积等因素有关,请任举一例加以说明。
(3)下图所示是几种物质在氧气中燃烧的实验装置,请完成下列各题。

①乙中观察到的现象为________ 。
②请写出丙中发生反应的文字表达式________ 。
③这三个实验中集气瓶的底部都加了少量的水,丙中水的作用是什么________
④分析这三个反应有什么共同点________ 。(写两点即可)
⑤氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应,这与氧原子结构中的________ 有关。
(4)求Fe3O4中铁元素的质量分数。(保留一位小数)
(1)如何验证一瓶无色气体是氧气?
(2)可燃物燃烧的剧烈程度与氧气浓度或接触面积等因素有关,请任举一例加以说明。
(3)下图所示是几种物质在氧气中燃烧的实验装置,请完成下列各题。

①乙中观察到的现象为
②请写出丙中发生反应的文字表达式
③这三个实验中集气瓶的底部都加了少量的水,丙中水的作用是什么
④分析这三个反应有什么共同点
⑤氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应,这与氧原子结构中的
(4)求Fe3O4中铁元素的质量分数。(保留一位小数)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表中部分元素的原子结构示意图,请利用表格信息回答相关问题。

(1)决定元素种类的是_______ (填字母,下同);与元素化学性质的关系最密切的是______ 。
A.原子核内的质子数B.原子核内的中子数
C.原子核外的最外层电子数D.元素的相对原子质量
(2)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质_________ 、氧化物_______ 、酸_______ 、碱________ 、盐________
(3)铝在氧气中燃烧生成氧化铝。请利用化学方程式计算,27g铝完全燃烧,消耗氧气的质量是多少________ ?(在答题纸上写出完整计算过程)

(1)决定元素种类的是
A.原子核内的质子数B.原子核内的中子数
C.原子核外的最外层电子数D.元素的相对原子质量
(2)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质
(3)铝在氧气中燃烧生成氧化铝。请利用化学方程式计算,27g铝完全燃烧,消耗氧气的质量是多少
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】甜瓜珍品——江西梨瓜以“脆、甜、香”而闻名。梨瓜中含有丰富的蛋白质、粗纤维、维生素、钙、磷、铁、镁、钾、硒等人体所需的营养素;

(1)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝_______ 防止腐烂;
(2)梨瓜适宜生长在pH为6.0-6.8的土壤中,实验室测定溶液pH的操作方法是_______________ ;
(3)如图为硒元素的某些信息,硒原子核内有_______ 个质子,硒原子的相对原子质量是_____ ,硒原子在化学反应中易_______ (填“得到”或“失去”)电子。

(1)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝
(2)梨瓜适宜生长在pH为6.0-6.8的土壤中,实验室测定溶液pH的操作方法是
(3)如图为硒元素的某些信息,硒原子核内有
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】“微观一宏观一符号”是化学独特的表示物质及其变化的方法。
(1)硒元素有防癌、抗癌作用。硬元素的部分信息如图1所示。
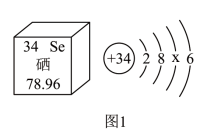
①图中x=_________ 。
②硒离子的化学符号为_________ 。
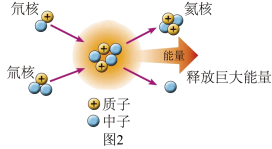
(2)氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个氦核,如图2所示,下列说法正确的是______。
(3)元素周期表中部分元素的信息如图3。
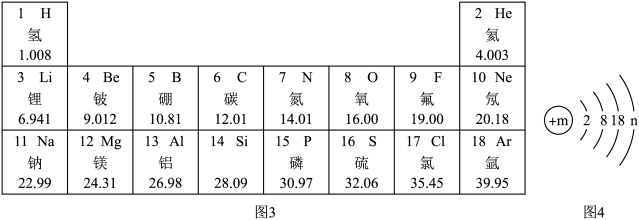
①第14号元素属于____ (选填“金属”或“非金属”)元素。
②11号和17号元素组成的物质由_______ (选填“分子”“原子”或“离子”)构成。
(4)已知如图4所示的原子对应的元素在元素周期表中位于铝元素的正下方,且与铝元素的化学性质相似,则m的值为________ 。
(1)硒元素有防癌、抗癌作用。硬元素的部分信息如图1所示。


①图中x=
②硒离子的化学符号为
(2)氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个氦核,如图2所示,下列说法正确的是______。
| A.该变化涉及的元素种类有三种 | B.该变化不属于化学变化范畴 |
| C.氘、氚两种原子的质子数相同 | D.氘和氚两种原子的质量相等 |
(3)元素周期表中部分元素的信息如图3。

①第14号元素属于
②11号和17号元素组成的物质由
(4)已知如图4所示的原子对应的元素在元素周期表中位于铝元素的正下方,且与铝元素的化学性质相似,则m的值为
您最近一年使用:0次
【推荐2】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)工业上生产尿素[CO(NH2)2]的反应微观示意图如图:
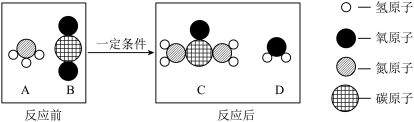
①从宏观的角度看,图中四种物质属于氧化物的有_____ (填字母序号)
②写出工业上生产尿素的化学方程式_____ 。
(2)如表是元素周期表中第2、3周期的元素,请回答有关问题。
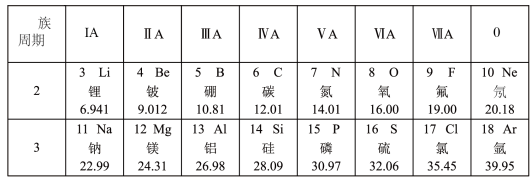
①下列各组具有相似化学性质的元素是______ (填字母序号);
A.Na、Cl B.O、S C.F、Cl D.Cl、Ar
②写出一条第三周期元素原子的核外电子排布规律______
③某粒子的结构示意图为 ,当x﹣y=8时,该粒子的符号为
,当x﹣y=8时,该粒子的符号为_____ ;
④具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是_____ (填字母序号)。
A.NO和O2 B.CO和N2 C.SO2和CO2 D. 和
和
(1)工业上生产尿素[CO(NH2)2]的反应微观示意图如图:

①从宏观的角度看,图中四种物质属于氧化物的有
②写出工业上生产尿素的化学方程式
(2)如表是元素周期表中第2、3周期的元素,请回答有关问题。

①下列各组具有相似化学性质的元素是
A.Na、Cl B.O、S C.F、Cl D.Cl、Ar
②写出一条第三周期元素原子的核外电子排布规律
③某粒子的结构示意图为
 ,当x﹣y=8时,该粒子的符号为
,当x﹣y=8时,该粒子的符号为④具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是
A.NO和O2 B.CO和N2 C.SO2和CO2 D.
 和
和
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物有着广泛的应用。
(1)在元素周期表中,硫元素的信息如图所示。下列从图中获得的信息不正确的是______(填字母)。

(2)含硫元素的物质间可发生以下转化: ,其中,反应①硫在氧气中燃烧产生的火焰是
,其中,反应①硫在氧气中燃烧产生的火焰是______ 色的:请你写出符合反应④转化的一个化学方程式______ 。
(3)pH<5.6的降水被称为酸雨,它会使土壤酸化,施用适量______ 可改良土壤酸性。
①正常的雨水也略显酸性,主要原因是什么______ ?
②酸雨的危害很大,硫酸型酸雨的形成有以下两种途径:

SO2通入碘水(I2的水溶液)会生成硫酸(H2SO4)和氢碘酸(HI),我们可利用此原理来测定空气中SO2的含量。请写出该反应的化学方程式______ 。
(4)为减少大气污染,火力发电厂常使用石灰石浆吸收废气中的二氧化硫,其反应原理是 。若1000kg废气中含有1.6kg的二氧化藏,则至少需要含90%碳酸钙的石灰石多少kg才能将其完全吸收?(写出解题过程,计算结果保留一位小数)
。若1000kg废气中含有1.6kg的二氧化藏,则至少需要含90%碳酸钙的石灰石多少kg才能将其完全吸收?(写出解题过程,计算结果保留一位小数)
(1)在元素周期表中,硫元素的信息如图所示。下列从图中获得的信息不正确的是______(填字母)。

| A.在硫原子的核外电子排布中a=2、b=8 |
| B.硫原子在化学反应中易获得2个电子生成S2- |
| C.硫原子里,质子数=中子数=电子数=16 |
| D.一个硫原子的相对原子质量是32.06g |
(2)含硫元素的物质间可发生以下转化:
 ,其中,反应①硫在氧气中燃烧产生的火焰是
,其中,反应①硫在氧气中燃烧产生的火焰是(3)pH<5.6的降水被称为酸雨,它会使土壤酸化,施用适量
①正常的雨水也略显酸性,主要原因是什么
②酸雨的危害很大,硫酸型酸雨的形成有以下两种途径:

SO2通入碘水(I2的水溶液)会生成硫酸(H2SO4)和氢碘酸(HI),我们可利用此原理来测定空气中SO2的含量。请写出该反应的化学方程式
(4)为减少大气污染,火力发电厂常使用石灰石浆吸收废气中的二氧化硫,其反应原理是
 。若1000kg废气中含有1.6kg的二氧化藏,则至少需要含90%碳酸钙的石灰石多少kg才能将其完全吸收?(写出解题过程,计算结果保留一位小数)
。若1000kg废气中含有1.6kg的二氧化藏,则至少需要含90%碳酸钙的石灰石多少kg才能将其完全吸收?(写出解题过程,计算结果保留一位小数)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】国将在2030年前实现“碳达峰”:2060年前实现“碳中和”。为了实现“双碳”目标,全社会各个领域开始行动起来。
I、二氧化碳的产生
(1)自然界中动植物呼吸是二氧化碳的主要来源之一。火山爆发时,碳酸类矿物(如碳酸钙)的岩层高温分解也会产生二氧化碳,写出碳酸钙分解的化学方程式:______ 。
(2)化石燃料的利用使大气中二氧化碳的浓度逐年上升。下列物质中,不属于化石燃料的是______ 。
a.煤b.氢气c.石油d.天然气
Ⅱ、二氧化碳的捕集
(3)自然界中消耗二氧化碳的主要途径有______ 。(只答一点即可)
(4)化学链燃烧技术有利于高效捕集CO2,流程如下图所示:

①写出“空气反应器”中Fe3O4在加热条件下与氧气反应的化学方程式:______ 。
②该流程中可循环利用的物质有______ 。
③与CO、H2直接在空气中燃烧相比,从燃料反应器排放出的CO2浓度更高的原因是______ 。
Ⅲ、二氧化碳的应用
2021年9月,中国科学家发表了利用CO2、H2人工合成淀粉的成果。合成步骤如下图所示:

(5)淀粉是由分子构成的有机物,从微观角度分析,直链淀粉和支链淀粉的性质不同,原因是______ 。
(6)步骤I中的反应为: ,现有6.6gCO2,最多能生成甲醇(CH3OH)的质量是多少?(写出计算过程)
,现有6.6gCO2,最多能生成甲醇(CH3OH)的质量是多少?(写出计算过程)
I、二氧化碳的产生
(1)自然界中动植物呼吸是二氧化碳的主要来源之一。火山爆发时,碳酸类矿物(如碳酸钙)的岩层高温分解也会产生二氧化碳,写出碳酸钙分解的化学方程式:
(2)化石燃料的利用使大气中二氧化碳的浓度逐年上升。下列物质中,不属于化石燃料的是
a.煤b.氢气c.石油d.天然气
Ⅱ、二氧化碳的捕集
(3)自然界中消耗二氧化碳的主要途径有
(4)化学链燃烧技术有利于高效捕集CO2,流程如下图所示:

①写出“空气反应器”中Fe3O4在加热条件下与氧气反应的化学方程式:
②该流程中可循环利用的物质有
③与CO、H2直接在空气中燃烧相比,从燃料反应器排放出的CO2浓度更高的原因是
Ⅲ、二氧化碳的应用
2021年9月,中国科学家发表了利用CO2、H2人工合成淀粉的成果。合成步骤如下图所示:

(5)淀粉是由分子构成的有机物,从微观角度分析,直链淀粉和支链淀粉的性质不同,原因是
(6)步骤I中的反应为:
 ,现有6.6gCO2,最多能生成甲醇(CH3OH)的质量是多少?(写出计算过程)
,现有6.6gCO2,最多能生成甲醇(CH3OH)的质量是多少?(写出计算过程)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】化学和生活息息相关。在抗击新冠疫情的斗争中,医护人员常用84消毒液、次氯酸和医用酒精做消毒剂。
(1)84消毒液于1984年由北京第一传染病医院研制成功,故称之为“84消毒液”。84消毒液为无色或淡黄色液体,具有刺激性气味;具有强氧化性,见光或受热就迅速分解。84消毒液常用于地面、下水道、厕所等处的消毒。
以上描述中,属于84消毒液化学性质的是___________ (写出一条即可),84消毒液应___________ 保存。
(2)次氯酸(化学式为HClO)常用于门把手、快递包装盒、外套、鞋子等的消毒。次氯酸中氯元素的化合价为___________ 价。
(3)消毒酒精常用于个人护理和家庭清洁。酒精学名叫乙醇,化学式为C2H6O,在空气中燃烧生成二氧化碳和水。写出乙醇燃烧的化学符号表达式(或化学方程式)___________ ;假酒中常含有甲醇(CH4O),甲醇对人体有剧毒。从微观角度分析,甲醇与乙醇组成元素相同,但化学性质不同的原因是___________ 。
(1)84消毒液于1984年由北京第一传染病医院研制成功,故称之为“84消毒液”。84消毒液为无色或淡黄色液体,具有刺激性气味;具有强氧化性,见光或受热就迅速分解。84消毒液常用于地面、下水道、厕所等处的消毒。
以上描述中,属于84消毒液化学性质的是
(2)次氯酸(化学式为HClO)常用于门把手、快递包装盒、外套、鞋子等的消毒。次氯酸中氯元素的化合价为
(3)消毒酒精常用于个人护理和家庭清洁。酒精学名叫乙醇,化学式为C2H6O,在空气中燃烧生成二氧化碳和水。写出乙醇燃烧的化学符号表达式(或化学方程式)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】科技缔造生活,化学创新未来。
(1)2023年9月6日,中国自主研制全球首辆氢能源智轨电车成功发往马来西亚。氢气做能源有什么优点?_______ (答两点)。保持氢气化学性质的最小粒子是_______ 。
A.氢元素 B.氢原子 C.氢分子 D.氢离子
(2)2023年9月21日,在“天宫课堂”中神舟十六号航天员在太空点燃蜡烛,火焰呈球形与地面火焰不同,充分燃烧产物相同。实验小组利用如图装置探究蜡烛燃烧及组成。烧杯中的蜡烛燃烧熄灭后,注射器推入澄清的石灰水。请你描述观察到的现象,由此得出蜡烛中一定含有哪些元素:_______ 。
(3)2023年9月22日,央视报道,我国首次太空育种的大樱桃在陕西铜川移栽成功。为提高樱桃的产量可施加一定最的碳酸氢铵(NH4HCO3)。

计算:
①碳酸氢铵中氢、碳元素的质量比______ ;
②碳酸氢铵的相对分子质量______ ;
③100 g碳酸氢铵中含氮元素______ 克。
(②③要有计算过程,③的计算结果保留一位小数)
(1)2023年9月6日,中国自主研制全球首辆氢能源智轨电车成功发往马来西亚。氢气做能源有什么优点?
A.氢元素 B.氢原子 C.氢分子 D.氢离子
(2)2023年9月21日,在“天宫课堂”中神舟十六号航天员在太空点燃蜡烛,火焰呈球形与地面火焰不同,充分燃烧产物相同。实验小组利用如图装置探究蜡烛燃烧及组成。烧杯中的蜡烛燃烧熄灭后,注射器推入澄清的石灰水。请你描述观察到的现象,由此得出蜡烛中一定含有哪些元素:
(3)2023年9月22日,央视报道,我国首次太空育种的大樱桃在陕西铜川移栽成功。为提高樱桃的产量可施加一定最的碳酸氢铵(NH4HCO3)。

计算:
①碳酸氢铵中氢、碳元素的质量比
②碳酸氢铵的相对分子质量
③100 g碳酸氢铵中含氮元素
(②③要有计算过程,③的计算结果保留一位小数)
您最近一年使用:0次



