根据图示实验过程和所提供的数据进行计算:

(1)生成氢气的质量为______ g。
(2)Cu-Zn合金中铜的质量分数。

(1)生成氢气的质量为
(2)Cu-Zn合金中铜的质量分数。
更新时间:2023-02-09 21:41:06
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】取一定质量的KClO3和12.6gMnO2的混合物于试管中,加热一段时间后,冷却,称量剩余固体质量为52g,经测定剩余固体中钾元素的质量分数为30%。求:
(1)生成氧气的质量是多少?
(2)生成的氯化钾质量是多少?
(3)参加反应的氯酸钾的质量是多少?
(1)生成氧气的质量是多少?
(2)生成的氯化钾质量是多少?
(3)参加反应的氯酸钾的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】镁是一种活泼性较强的金属,在空气中易发生缓慢氧化,表面呈灰黑色。
(1)将2.4g未氧化的镁加入到97.8g的稀硫酸中,恰好完全反应。求反应后所得溶液的溶质质量分数(假设反应过程中水分未损失)。(写出计算过程)
(2)若30g镁条存放一段时间后,质量变为了34g,则参加反应的氧气为__ g(假设镁只与氧气反应)。若将上述氧化前和氧化后的镁条分别与足量稀硫酸反应,生成硫酸镁的质量关系是前者____ 后者(填“>”、“=”或“<”)。
(1)将2.4g未氧化的镁加入到97.8g的稀硫酸中,恰好完全反应。求反应后所得溶液的溶质质量分数(假设反应过程中水分未损失)。(写出计算过程)
(2)若30g镁条存放一段时间后,质量变为了34g,则参加反应的氧气为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】宜宾市某县有丰富的石灰石资源,某兴趣小组同学为了测定石灰石中碳酸钙的质量分数,将100g稀盐酸分五次加入盛有10g石灰石的烧杯中,充分反应后测得实验数据如下表(杂质不参加反应):
(1)表格中m的值为______ 。
(2)该县的石灰石中碳酸钙的质量分数。(写出计算过程)
(3)该县某工厂煅烧石灰石制生石灰,计算用100吨石灰石可生产出有杂质的生石灰的质量______ 。(杂质不反应)
实验次数 | 1 | 2 | 3 | 4 | 5 |
累计加入稀盐酸的质量/g | 20 | 40 | 60 | 80 | 100 |
烧杯中剩余物质的质量/g | 29 | 48 | m | 86.7 | 106.7 |
(2)该县的石灰石中碳酸钙的质量分数。(写出计算过程)
(3)该县某工厂煅烧石灰石制生石灰,计算用100吨石灰石可生产出有杂质的生石灰的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定样品中碳酸钙的含量,甲、乙两同学各取12g石灰石样品,用足量的浓度为10%的盐酸与其充分反应,测得数据如图所示。试回答下列问题:

(1)12g石灰石样品充分反应,产生的 的质量为
的质量为___________ g。
(2)由图像可知,化学反应的速率与反应物的接触面积的关系是___________ 。
(3)12g该样品中碳酸钙的质量是多少?(写出计算过程)
(4)在图中画出12g石灰石粉状样品与足量15%盐酸,充分反应的曲线c的大致位置及趋势。

(1)12g石灰石样品充分反应,产生的
 的质量为
的质量为(2)由图像可知,化学反应的速率与反应物的接触面积的关系是
(3)12g该样品中碳酸钙的质量是多少?(写出计算过程)
(4)在图中画出12g石灰石粉状样品与足量15%盐酸,充分反应的曲线c的大致位置及趋势。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组用一块表面已经被氧化的镁块做了如下实验:取一定质量的镁块样品于烧瓶中,逐滴滴加溶质质量分数为 9.8%的稀硫酸至固体恰好完全溶解,消耗了 300g 稀硫酸,共收集到0.4 g氢气。请回答下列问题∶
(1)MgO的相对分子质量是____,H2SO4中氢、硫、氧的原子个数比为
(2)MgSO4中镁元素的质量分数为____
(3)参加反应的镁单质的质量为____g
(4)计算该镁块样品中镁单质的质量分数。(写出简单的计算过程,计算结果精确至0.1)
(1)MgO的相对分子质量是____,H2SO4中氢、硫、氧的原子个数比为
(2)MgSO4中镁元素的质量分数为____
(3)参加反应的镁单质的质量为____g
(4)计算该镁块样品中镁单质的质量分数。(写出简单的计算过程,计算结果精确至0.1)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂质) ,请你参与他们的探究过程。称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应 后,测定生成氢气的质量,实验数据如下表所示:
试求:
(1)m的数值是______ ;
(2)此黄铜样品中铜的质量分数是________ ? (写出计算过程)
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(mL) | 15 | 15 | 15 |
| 生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:
(1)m的数值是
(2)此黄铜样品中铜的质量分数是
您最近一年使用:0次


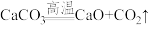 ,假设杂质不参与反应)。请计算:
,假设杂质不参与反应)。请计算:

