镁是一种活泼性较强的金属,在空气中易发生缓慢氧化,表面呈灰黑色。
(1)将2.4g未氧化的镁加入到97.8g的稀硫酸中,恰好完全反应。求反应后所得溶液的溶质质量分数(假设反应过程中水分未损失)。(写出计算过程)
(2)若30g镁条存放一段时间后,质量变为了34g,则参加反应的氧气为__ g(假设镁只与氧气反应)。若将上述氧化前和氧化后的镁条分别与足量稀硫酸反应,生成硫酸镁的质量关系是前者____ 后者(填“>”、“=”或“<”)。
(1)将2.4g未氧化的镁加入到97.8g的稀硫酸中,恰好完全反应。求反应后所得溶液的溶质质量分数(假设反应过程中水分未损失)。(写出计算过程)
(2)若30g镁条存放一段时间后,质量变为了34g,则参加反应的氧气为
更新时间:2016-11-28 13:59:14
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在CO和CO2的混合气体中,氧元素的质量分数是64%,将该气体5g通过足量的灼热的CuO粉末,完全反应后,气体通过足量的澄清石灰水得到白色沉淀的质量是__________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定锌铜合金中锌的含量,取该合金粉末放入如图所示盛有稀硫酸的锥形瓶中,发生反应。多次实验后,取平均值所得数据如下表:
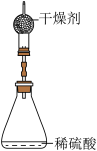
不考虑干燥剂吸收空气中的水蒸气。请分析计算:
(1)根据质量守恒定律可得生成氢气的质量为______ g。
(2)该合金中锌的质量分数。

| 反应前 | 充充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金粉末质量 | |
 |  |  |
(1)根据质量守恒定律可得生成氢气的质量为
(2)该合金中锌的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】H2在加热的条件下可以还原CuO(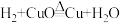 )。某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物,Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。
)。某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物,Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。
(1)该小组同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为_____________ 。
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。此红色固体中氧元素的质量为_____________ ,以此推得Cu2O的质量为_____________ 。
(3)将(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O + 2HCl═CuCl2+Cu+H2O ),充分搅拌,除有红色固体外,还发现溶液变成蓝绿。试计算此蓝色溶液中CuCl2的质量分数(精确到0.01 % )。__
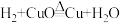 )。某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物,Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。
)。某兴趣小组同学在一份资料中了解到:铜有CuO和Cu2O(红色)两种常见的氧化物,Cu和Cu2O均为红色,故他们猜测,在H2还原CuO所得的红色产物中可能含有Cu2O。(1)该小组同学准确称取了8.0g黑色CuO粉末放入大试管中,不断通入足量的H2,在加热条件下进行还原,如果产物只有Cu,其质量应为
(2)该小组在H2还原CuO时,当发现8.0g黑色CuO粉末全部转变成红色时,停止加热,冷却后称得固体质量为6.8g。此红色固体中氧元素的质量为
(3)将(2)中所得的6.8g固体放入烧杯中,加入48.0g过量稀盐酸(Cu2O与稀盐酸的反应为:Cu2O + 2HCl═CuCl2+Cu+H2O ),充分搅拌,除有红色固体外,还发现溶液变成蓝绿。试计算此蓝色溶液中CuCl2的质量分数(精确到0.01 % )。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】镁铜合金常用作飞机天线等导电材料。现取10g该合金样品,加入足量的稀盐酸中,充分反应后,放出0.3g气体,样品中铜的质量分数是多少?(写出计算过程)_______
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】为测定生铁中铁的含量,现将14g生铁样品加入到100g稀硫酸中恰好完全反应(杂质不溶于水,也不与酸反应,杂质中不含铁元素),实验过程及测得的数据如下:
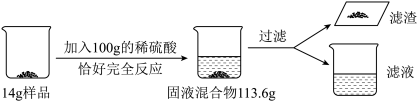
(1)写出上述反应的化学方程式_____ 。
(2)反应生成氢气的质量为_____ 。
(3)该生铁中铁的含量(质量分数)为_____ 。
(4)所得滤液的颜色为_____ ;质量为_____ 。

(1)写出上述反应的化学方程式
(2)反应生成氢气的质量为
(3)该生铁中铁的含量(质量分数)为
(4)所得滤液的颜色为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】铁是常用的金属材料。兴趣小组的同学对某铁制品中铁的质量分数进行了测定。 称取3 g铁屑,缓慢加入一定溶质质量分数的硫酸溶液,直到过量(假设除铁以外的物质都不与硫酸反应),实验数据如图所示。 请计算:
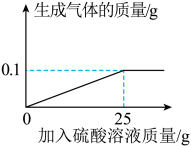
(1)该铁制品中铁的质量分数(最终结果保留到0.1%);
(2)所用硫酸溶液的溶质质量分数。(要求有计算的过程)
(3)恰好完全反应时所得溶液的质量为多少?

(1)该铁制品中铁的质量分数(最终结果保留到0.1%);
(2)所用硫酸溶液的溶质质量分数。(要求有计算的过程)
(3)恰好完全反应时所得溶液的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】现有一瓶硫酸铜和稀硫酸的混合溶液 49.0 g,小玉向该混合溶液中逐渐滴加 10%的氢氧化钠溶液至过量。测得所加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示:
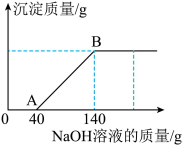
(1)与硫酸铜反应所消耗的氢氧化钠溶液的质量为____________g;
(2)请算出原混合溶液中稀硫酸的质量分数。(要求写出计算过程)

(1)与硫酸铜反应所消耗的氢氧化钠溶液的质量为____________g;
(2)请算出原混合溶液中稀硫酸的质量分数。(要求写出计算过程)
您最近一年使用:0次




