海水可用于制造纯碱。
(1)工业上采用氨碱法生产纯碱(Na2CO3),主要流程如下图1:
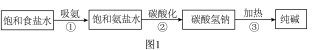
在①〜③三个过程中,发生分解反应的是______ (填序号),氨盐水比食盐水更容易吸收二氧化碳的原因是_________________ 。
(2)我国化学家侯德榜在氨碱法的基础上创立的侯氏制碱法,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图2所示:
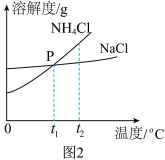
①写出一条P点表示的意义____________ 。
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会_____ (填“变大”“变小”“不变”之一)。当NH4Cl固体中含有少量NaCl时,可采用____ (填“蒸发结晶”或“降温结晶”)的方法提纯NH4Cl。
③将接近饱和NaCl溶液变为饱和溶液,可采用的方法有_____________ 、_____________ 。
(1)工业上采用氨碱法生产纯碱(Na2CO3),主要流程如下图1:

在①〜③三个过程中,发生分解反应的是
(2)我国化学家侯德榜在氨碱法的基础上创立的侯氏制碱法,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图2所示:

①写出一条P点表示的意义
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会
③将接近饱和NaCl溶液变为饱和溶液,可采用的方法有
更新时间:2023-02-18 14:44:42
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图分别表示A、B、C三种物质的溶解度曲线,试答:

(1)通过加溶质、蒸发溶剂、升高温度均可使接近饱和的溶液变为其饱和溶液的物质是______ 。
(2)等质量的三种饱和溶液从60℃降温至20℃时,其中析出晶体最多的是______ 。
(3)要从A、B、C的混合物中分离出A,最好用______ 法。

(1)通过加溶质、蒸发溶剂、升高温度均可使接近饱和的溶液变为其饱和溶液的物质是
(2)等质量的三种饱和溶液从60℃降温至20℃时,其中析出晶体最多的是
(3)要从A、B、C的混合物中分离出A,最好用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图为KNO3和NaCl的溶解度曲线,根据图示信息回答问题。___________ g;
(2)a点对应的是60℃时KNO3的___________ (填“饱和”或“不饱和”)溶液;
(3)若要实现a点到b点KNO3溶液的转化,以下操作可行的是___________;
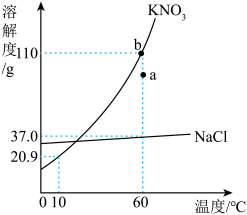
(2)a点对应的是60℃时KNO3的
(3)若要实现a点到b点KNO3溶液的转化,以下操作可行的是___________;
| A.加KNO3 | B.加入60℃的水 | C.恒温蒸发溶剂 | D.降温 |
您最近一年使用:0次
【推荐1】根据右图所示的溶解度曲线,回答下列问题。

(1)10℃时,将NaCl、KNO3各30g分别加入100g水中,充分搅拌后,固体全部溶解的是_____ ;
(2)将KNO3的饱和溶液转化为不饱和溶液,通常采用的方法有:加水和_____ 。

(1)10℃时,将NaCl、KNO3各30g分别加入100g水中,充分搅拌后,固体全部溶解的是
(2)将KNO3的饱和溶液转化为不饱和溶液,通常采用的方法有:加水和
您最近一年使用:0次
【推荐2】下图是是甲、乙两种固体物质的溶解度曲线,请你回答下列问题:

(1)__________ ℃时,甲、乙两种物质的溶解度相等;
(2)若固体甲中含有少量乙时,可用__________ 方法提纯甲(填“蒸发结晶”或“冷却结晶”);
(3)溶解度受温度影响比较大的物质是_______ ;
(4)t2℃时,用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量:甲______ 乙(填“>”“<”或“=”)

(1)
(2)若固体甲中含有少量乙时,可用
(3)溶解度受温度影响比较大的物质是
(4)t2℃时,用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量:甲
您最近一年使用:0次
【推荐3】回答下列问题。
(1)2018年5月6日晚,泉城济南筹备了近一年的“明湖灯光秀”首次公演,奇光异彩、如梦如幻的场景让济南备受关注。“明湖秀”作为泉城夜宴的精华,以大明湖为载体,讲述了泉城济南从历史走向未来的动人篇章。某化学兴趣小组为了解提升大明湖的水质方法,查阅了相关资料。

①该小组同学查阅资料得知二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂,其中氯元素的化合价为______________ 。
②工业上制备二氧化氧的方法是将氯气通入亚氯酸钠(NaClO2)制得二氧化氯,写出该反应的化学方程式______________ 。
(2)同学们又探究了温度对物质溶解性的影响(溶解度曲线如图所示),试回答下列问题:

①t1℃时,A、B、C三种物质中溶解度最大的是______________ 。
②t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为___________ g。
③t1℃时,C的饱和溶液的溶质质量分数为___________ 。
④将t1℃的A、B、C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是___________ 。
(1)2018年5月6日晚,泉城济南筹备了近一年的“明湖灯光秀”首次公演,奇光异彩、如梦如幻的场景让济南备受关注。“明湖秀”作为泉城夜宴的精华,以大明湖为载体,讲述了泉城济南从历史走向未来的动人篇章。某化学兴趣小组为了解提升大明湖的水质方法,查阅了相关资料。

①该小组同学查阅资料得知二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂,其中氯元素的化合价为
②工业上制备二氧化氧的方法是将氯气通入亚氯酸钠(NaClO2)制得二氧化氯,写出该反应的化学方程式
(2)同学们又探究了温度对物质溶解性的影响(溶解度曲线如图所示),试回答下列问题:

①t1℃时,A、B、C三种物质中溶解度最大的是
②t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为
③t1℃时,C的饱和溶液的溶质质量分数为
④将t1℃的A、B、C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】以碳酸钠溶液为例的反应关系(如下图)体现了盐类物质的化学性质,结合此图回答问题:

(1)碳酸钠俗称纯碱或_______ 。
(2)反应①的化学方程式为_______ 。
(3)为了验证性质②将碳酸钠溶液与酚酞溶液混合,溶液由无色变为___ ,证明碳酸钠溶液显____ (填“酸”或“碱”)性。
(4)反应③和④的基本反应类型为_______ 。
(5)反应⑤将二氧化碳通入碳酸钠溶液会生成碳酸氢钠,该反应的化学方程式为_______ 。

(1)碳酸钠俗称纯碱或
(2)反应①的化学方程式为
(3)为了验证性质②将碳酸钠溶液与酚酞溶液混合,溶液由无色变为
(4)反应③和④的基本反应类型为
(5)反应⑤将二氧化碳通入碳酸钠溶液会生成碳酸氢钠,该反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】超细碳酸钙可用于生产钙片、牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示意如下:
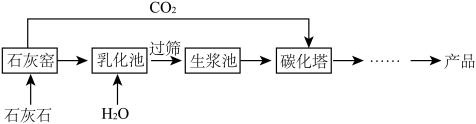
(1)石灰石主要成分是碳酸钙,在石灰窑中煅烧石灰石的化学方程式为_____________________ ;
(2)乳化池中,生石灰与水发生反应,这个反应过程中会_________ (填“吸收”或“放出”)热量, 这个反应的基本反应类型为_____________________________ ;
(3)碳化塔中反应的化学方程式为__________________________________ 。

(1)石灰石主要成分是碳酸钙,在石灰窑中煅烧石灰石的化学方程式为
(2)乳化池中,生石灰与水发生反应,这个反应过程中会
(3)碳化塔中反应的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】碳酸钠(Na2CO3)是重要的化工原料,有如下制取方法:
Ⅰ.吕布兰法的原理:①
②
(1)从环保角度考虑,你认为该方法的不足之处是______ 。
Ⅱ.经科学家不断的改进,碳酸钠的制取可用以下方法:

(2)该流程中可循环使用的物质是______ 。
(3)步骤①在加压条件下通入CO2,这样操作的目的是______ 。
(4)步骤②发生分解反应的化学方程式是______ 。
Ⅰ.吕布兰法的原理:①

②

(1)从环保角度考虑,你认为该方法的不足之处是
Ⅱ.经科学家不断的改进,碳酸钠的制取可用以下方法:

(2)该流程中可循环使用的物质是
(3)步骤①在加压条件下通入CO2,这样操作的目的是
(4)步骤②发生分解反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】我国有漫长的海岸线,蕴藏着丰富的海洋资源。

(1)海水晒盐:
①海水“晒盐”是利用_______ (填字母代号)的方法使氯化钠晶体析出。
A 升高温度,使氯化钠溶解度增大
B 风吹日晒,使溶剂蒸发
②海水“晒盐”后,所得的母液是氯化钠的_______ (填“饱和”或“不饱和”)溶液。
(2)粗盐提纯:除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42-等杂质离子,为得到较纯的氯化钠,进行如下的实验操作(顺序不定):
①加入过量的碳酸钠溶液 ②加入过量的氯化钡溶液 ③加入过量的氢氧化钠溶液 ④加入适量的盐酸调节溶液的pH等于7 ⑤过滤 ⑥蒸发。其中操作①加入过量的碳酸钠溶液,可除去的溶液中的离子是_______ (填离子符号),④加入适量的盐酸调节溶液的pH等于7的目的是_______ 。
(3)海水制镁:实际生产中,步骤Ⅲ反应的化学方程式_______ 。
(4)海水“制碱”:氨碱工业生产过程中,在加压并不断向饱和的氨盐水中通入二氧化碳气体,_______ (填化学式)先结晶析出。

(1)海水晒盐:
①海水“晒盐”是利用
A 升高温度,使氯化钠溶解度增大
B 风吹日晒,使溶剂蒸发
②海水“晒盐”后,所得的母液是氯化钠的
(2)粗盐提纯:除去难溶性杂质后的食盐水中还含有Ca2+、Mg2+、SO42-等杂质离子,为得到较纯的氯化钠,进行如下的实验操作(顺序不定):
①加入过量的碳酸钠溶液 ②加入过量的氯化钡溶液 ③加入过量的氢氧化钠溶液 ④加入适量的盐酸调节溶液的pH等于7 ⑤过滤 ⑥蒸发。其中操作①加入过量的碳酸钠溶液,可除去的溶液中的离子是
(3)海水制镁:实际生产中,步骤Ⅲ反应的化学方程式
(4)海水“制碱”:氨碱工业生产过程中,在加压并不断向饱和的氨盐水中通入二氧化碳气体,
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】海洋是一个巨大的资源宝库,但人类需根据物质的性质,采取适合的方法才能提出海水中的化学元素。回答以下问题:
(1)从海水中提取镁元素经过MgCl2→Mg(OH)2→MgCl2步骤,不直接对海水或卤水通电得到镁的原因是_____ 。
(2)我国制碱工业先驱﹣﹣侯德榜先生在“氨碱法”的基础上发明了“联合制碱法”。“氨碱法”的化学反应原理是_____ 、_____ ;“联合制碱法”除上述产物外还能得到一种化肥的名称是_____ 。
(3)碳酸钠是一种盐,由_____ 、_____ (填粒子符号)构成,属于碳酸盐。检验碳酸盐的方法是_____ 。
(1)从海水中提取镁元素经过MgCl2→Mg(OH)2→MgCl2步骤,不直接对海水或卤水通电得到镁的原因是
(2)我国制碱工业先驱﹣﹣侯德榜先生在“氨碱法”的基础上发明了“联合制碱法”。“氨碱法”的化学反应原理是
(3)碳酸钠是一种盐,由
您最近一年使用:0次