打开碳酸饮料瓶盖时会有大量气泡逸出。小组同学进行实验,探究影响CO2溶解能力的因素。
【活动一】探究温度和压强对CO2溶解能力的影响
实验1:标准大气压下,向试管中分别加入100mL某种无色碳酸饮料,大烧杯中加入不同温度的水,小烧杯中加入适量澄清石灰水。
实验2:室温下,向试管中分别加入100mL某种无色碳酸饮料。
(1)实验1,烧杯中澄清石灰水变浑浊的原因是____ (用化学方程式表示)。
(2)由实验1得到的结论是_____ 。
(3)由实验2可知,压强越大,CO2溶解的量越_____ (填“多”或“少”)。
【活动二】探究CO2在不同物质的溶解性
实验3:烧瓶中收集250mL的气体,分别加入50mL不同液体,通过压强传感器测定瓶中压强变化。(实验前烧瓶内压强为104.20kPa,实验过程中保持温度恒定)
(4)实验后瓶内的压强,实验⑧小于实验⑦的原因是_____ 。
(5)根据实验3分析可知,选用排_____ 液体收集CO2效果更好。
(6)从上述实验中可知,1体积水约能溶解1体积CO2的依据是:_____ 。
(7)化学学习是一个宏微结合的过程,根据实验3所给的数据,按照图1的方式画出图2中液体上方的微观示意图。

(8)请你利用二氧化碳溶解性知识,解释“打开碳酸饮料瓶盖时,会有大量气泡逸出”的原因____ 。
【活动一】探究温度和压强对CO2溶解能力的影响
实验1:标准大气压下,向试管中分别加入100mL某种无色碳酸饮料,大烧杯中加入不同温度的水,小烧杯中加入适量澄清石灰水。
| 实验装置 | 实验序号 | 大烧杯中水的温度 | 试管中产生气泡的速率 | 澄清石灰水的现象 |
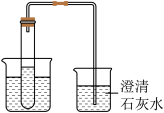 | 实验① | 0℃ | 缓慢 | 不浑浊 |
| 实验② | 20℃ | 适中 | 不浑浊 | |
| 实验③ | 90℃ | 很快 | 变浑浊 |
| 实验装置 | 实验序号 | 注射器活塞的位置 | 试管中的产生气泡的速率 |
 | 实验④ | 不拉动活塞 | 适中 |
| 实验⑤ | 向上拉活塞到25mL | 变快 | |
| 实验⑥ | 向上拉活塞到50mL | 变得更快 |
(1)实验1,烧杯中澄清石灰水变浑浊的原因是
(2)由实验1得到的结论是
(3)由实验2可知,压强越大,CO2溶解的量越
【活动二】探究CO2在不同物质的溶解性
实验3:烧瓶中收集250mL的气体,分别加入50mL不同液体,通过压强传感器测定瓶中压强变化。(实验前烧瓶内压强为104.20kPa,实验过程中保持温度恒定)
| 实验操作 | 实验序号 | 烧瓶中气体 | 注射器中物质 | 实验后瓶内压强 |
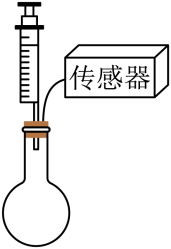 | 实验⑦ | 空气 | 水 | 130.25kPa |
| 实验⑧ | CO2 | 水 | 104.98kPa | |
| 实验⑨ | CO2 | 盐酸 | 106.67kPa | |
| 实验⑩ | CO2 | 小苏打的水溶液 | 103.40kPa |
(4)实验后瓶内的压强,实验⑧小于实验⑦的原因是
(5)根据实验3分析可知,选用排
(6)从上述实验中可知,1体积水约能溶解1体积CO2的依据是:
(7)化学学习是一个宏微结合的过程,根据实验3所给的数据,按照图1的方式画出图2中液体上方的微观示意图。

(8)请你利用二氧化碳溶解性知识,解释“打开碳酸饮料瓶盖时,会有大量气泡逸出”的原因
更新时间:2023-02-20 10:51:20
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】下列A~E是实验室制取气体的常用装置。
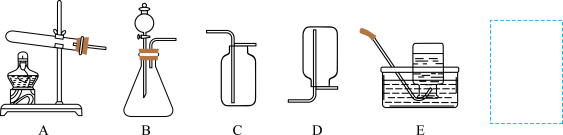
(1)实验室用锌粒和稀硫酸反应制氢气,请选择一套装置组合_________ 。
(2)写出一个用A装置制取氧气的化学方程式________ 。
(3)请在虚线框内画出用试管采用排空气法收集二氧化碳的装置图________ 。

(1)实验室用锌粒和稀硫酸反应制氢气,请选择一套装置组合
(2)写出一个用A装置制取氧气的化学方程式
(3)请在虚线框内画出用试管采用排空气法收集二氧化碳的装置图
您最近一年使用:0次
【推荐2】2023年5月28日,国产大飞机C919完成首次商业航班飞行。作为拥有完全知识产权的干线客机,C919中承载着许多科技元素。制造飞机最重要的金属材料是硬铝合金,下图是硬铝有关说明和相关实验。

(1)如图A所示,将未打磨过的硬铝放入足量稀硫酸中,初始未观察到气泡的原因是___________ 。
(2)如图B所示,将打磨过的硬铝丝放入硫酸铜溶液中,写出硬铝中镁与硫酸铜溶液反应的方程式___________ 。
(3)如图C所示,将一定量硝酸银溶液滴入盛有硬铝粉末的试管中,充分反应后,过滤,滤渣中有红色固体,则滤渣一定有___________ (填“Cu、Ag”或“Ag”)。

(1)如图A所示,将未打磨过的硬铝放入足量稀硫酸中,初始未观察到气泡的原因是
(2)如图B所示,将打磨过的硬铝丝放入硫酸铜溶液中,写出硬铝中镁与硫酸铜溶液反应的方程式
(3)如图C所示,将一定量硝酸银溶液滴入盛有硬铝粉末的试管中,充分反应后,过滤,滤渣中有红色固体,则滤渣一定有
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】同学们用下图所示装置进行实验,验证CO2与NaOH、Ca(OH)2都能发生反应。

分别向甲、乙两个瓶中注入少量、等体积的两种溶液,观察实验现象。
(1)甲中反应的化学方程式是____ 。说明CO2能与Ca(OH)2反应的实验现象是____ 。
(2)下列实验现象中,一定能说明“CO2与NaOH发生了化学反应”的是____ (填序号)。
a.U型管中红墨水左低右高
b.U型管中红墨水左高右低
c.U型管中红墨水液面没有发生改变

分别向甲、乙两个瓶中注入少量、等体积的两种溶液,观察实验现象。
(1)甲中反应的化学方程式是
(2)下列实验现象中,一定能说明“CO2与NaOH发生了化学反应”的是
a.U型管中红墨水左低右高
b.U型管中红墨水左高右低
c.U型管中红墨水液面没有发生改变
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】某实验小组同学设计了一款简易吸风机来“捉碳”,打开开关,风扇旋转产生内外压强差将空气自右向左吸进简易吸风机, 在沙布上被吸碳剂捕获。同学们通过实验探寻适宜的
在沙布上被吸碳剂捕获。同学们通过实验探寻适宜的 吸碳剂。
吸碳剂。 吸碳剂一振荡吸收法
吸碳剂一振荡吸收法
(1)在三只装有等量 的软塑料瓶中分别倒入水、澄清石灰水、石灰乳,旋紧瓶盖,振荡,瘪的最厉害的是
的软塑料瓶中分别倒入水、澄清石灰水、石灰乳,旋紧瓶盖,振荡,瘪的最厉害的是_______ 瓶(填序号);
(2)在吸风机纱布上涂抹一层石灰乳进行实验,一段时间后发现纱布变硬,吸风效果变差,原因可能是_________ (用化学方程式表示)。
Ⅱ.催化固碳
实验小组查阅资料,发现利用 和
和 在催化剂作用下反应,不仅可以解决固碳问题还可以生成可做燃料的甲醇
在催化剂作用下反应,不仅可以解决固碳问题还可以生成可做燃料的甲醇 。
。_____ K时甲醇产率最高;压强越大,甲醇产率越高。
(4)催化固碳条件较为苛刻,实验小组发现还可以利用电解法来固碳,写出电解法固碳的化学方程式________ 。
 在沙布上被吸碳剂捕获。同学们通过实验探寻适宜的
在沙布上被吸碳剂捕获。同学们通过实验探寻适宜的 吸碳剂。
吸碳剂。
 吸碳剂一振荡吸收法
吸碳剂一振荡吸收法| A瓶 | B瓶 | C瓶 |
| 水 | 澄清石灰水 | 石灰乳 |
 水 水 |  |  |
(1)在三只装有等量
 的软塑料瓶中分别倒入水、澄清石灰水、石灰乳,旋紧瓶盖,振荡,瘪的最厉害的是
的软塑料瓶中分别倒入水、澄清石灰水、石灰乳,旋紧瓶盖,振荡,瘪的最厉害的是(2)在吸风机纱布上涂抹一层石灰乳进行实验,一段时间后发现纱布变硬,吸风效果变差,原因可能是
Ⅱ.催化固碳
实验小组查阅资料,发现利用
 和
和 在催化剂作用下反应,不仅可以解决固碳问题还可以生成可做燃料的甲醇
在催化剂作用下反应,不仅可以解决固碳问题还可以生成可做燃料的甲醇 。
。
(4)催化固碳条件较为苛刻,实验小组发现还可以利用电解法来固碳,写出电解法固碳的化学方程式
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】海洋酸化对海洋生物带来了威胁。尤其如珊瑚和软体动物等长有坚硬外壳(主要成分是碳酸钙)生物,会出现外壳溶解而难以生存。如图是1990年2010年间某海域中二氧化碳浓度及海水pH变化趋势,请回答下列问题。

(1)该海域海水呈_____ (填“酸”或“碱”)性。
(2)珊瑚等动物难以生存的主要原因是碳酸钙与海水中的CO2和水反应生成了可溶的碳酸氢钙,该化学方程式为_____ 。
【校内拓展】为研究降低CO2的方法,小铭在实验室用传感器研究等量饱和澄清石灰水、饱和NaOH溶液分别吸收CO2的效果,装置及测定结果如图所示。

(3)实验开始前应先进行的操作是_____ 。
(4)表示石灰水吸收CO2结果的曲线是_____ (填“①”或“②”)。
(5)【小铭的实验结论】_____ 。

(1)该海域海水呈
(2)珊瑚等动物难以生存的主要原因是碳酸钙与海水中的CO2和水反应生成了可溶的碳酸氢钙,该化学方程式为
【校内拓展】为研究降低CO2的方法,小铭在实验室用传感器研究等量饱和澄清石灰水、饱和NaOH溶液分别吸收CO2的效果,装置及测定结果如图所示。

(3)实验开始前应先进行的操作是
(4)表示石灰水吸收CO2结果的曲线是
(5)【小铭的实验结论】
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】(1)(1)在溶液中较难制得纯净的Fe(OH)2,原因是Fe(OH)2不稳定,在水中只要有一点氧气就极易反应生成红褐色沉淀Fe(OH)3。写出其反应的化学方程式:
_________________________________________________ 。
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀。
(2)方法一:用不含氧气的蒸馏水配置FeSO4溶液与NaOH溶液,然后反应制备。
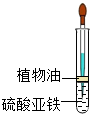
a.除去蒸馏水中溶解的氧气,常采用__________ 的方法。
b.如图所示,用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。试管中油层的作用是________________ 。
方法二:用如图装置来制备。
(3)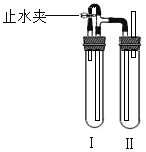
a在装置Ι中加入Fe和稀H2SO4,写出其反应的化学方程式__________________ ;在装置Ⅱ中加入NaOH浓溶液。
b为了制得白色Fe(OH)2沉淀,需要下列步骤,其顺序为__
①气密性检查 ②气体验纯
③加入试剂塞紧橡皮塞 ④打开止水夹 ⑤夹紧止水夹。
c.写出试管Ⅱ中发生的化学反应方程式
___________________ 、 ___________________ 。
这样生成的Fe(OH)2沉淀能较长时间保持白色。
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀。
(2)方法一:用不含氧气的蒸馏水配置FeSO4溶液与NaOH溶液,然后反应制备。

a.除去蒸馏水中溶解的氧气,常采用
b.如图所示,用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。试管中油层的作用是
方法二:用如图装置来制备。
(3)

a在装置Ι中加入Fe和稀H2SO4,写出其反应的化学方程式
b为了制得白色Fe(OH)2沉淀,需要下列步骤,其顺序为
①气密性检查 ②气体验纯
③加入试剂塞紧橡皮塞 ④打开止水夹 ⑤夹紧止水夹。
c.写出试管Ⅱ中发生的化学反应方程式
这样生成的Fe(OH)2沉淀能较长时间保持白色。
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】研究性学习小组利用如图1装置进行相关气体制取的探究,请你分析并填空。

(1)实验室制取二氧化碳的化学方程式是________ ,实验室制取二氧化碳应选择的制取装置是__________ 。(填字母)(在A-E装置中选)
(2)甲烷是一种无色、无味、难溶于水的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取甲烷应选择的发生装置是__________ (填字母)。若用F装置收集甲烷,应从导管__________ (填“①”或“②”)通入甲烷.
(3)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如图2所示.
①在干燥管内的铜网上应盛放__________ 。
②用该装置制取二氧化碳的优点是:__________ 。
③若将铜网换成铁网,可能产生的后果是_________ ,其原因是______ (用化学方程式表示)。
(4)制取二氧化碳时提供的原料药品只有37%的浓盐酸与石灰石,这样制取的二氧化碳中肯定混有水蒸气和氯化氢气体。为减少二氧化碳气体中混杂的氯化氢,倾倒盐酸之前,可预先在锥形瓶中加__________ 。
(5)下表是CO2在水中的溶解度(单位:ml)的几组数据:
①根据数据分析:CO2在水中的溶解度随温度的升高而________ (填“增大”或“减小”)。
②打开汽水瓶盖有气体逸出,说明原瓶内的气压________ (填“>”“<”或“=”)瓶外大气压。

(1)实验室制取二氧化碳的化学方程式是
(2)甲烷是一种无色、无味、难溶于水的气体,实验室常用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取甲烷应选择的发生装置是
(3)该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如图2所示.
①在干燥管内的铜网上应盛放
②用该装置制取二氧化碳的优点是:
③若将铜网换成铁网,可能产生的后果是
(4)制取二氧化碳时提供的原料药品只有37%的浓盐酸与石灰石,这样制取的二氧化碳中肯定混有水蒸气和氯化氢气体。为减少二氧化碳气体中混杂的氯化氢,倾倒盐酸之前,可预先在锥形瓶中加
(5)下表是CO2在水中的溶解度(单位:ml)的几组数据:
压强/101kPa 温度/℃ | 0 | 25 | 50 | 75 | 100 |
1 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
10 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
25 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
②打开汽水瓶盖有气体逸出,说明原瓶内的气压
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】下图是实验室常见的制取气体的装置,请结合下图回答问题:
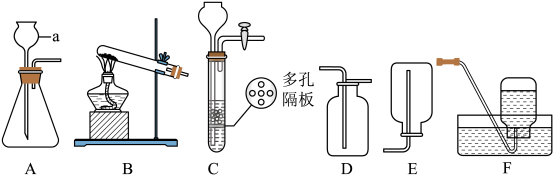
(1)写出编号仪器名称:a___________ 。
(2)用高锰酸钾制取氧气,选择B作发生装置,需要补充的实验用品是______ ,反应的化学方程式为_____ ,要收集较为纯净的氧气,应选择的收集装置是______ (选填字母)。
(3)实验室制取CO2的化学方程式为___________ ,用D装置收集二氧化碳,检验二氧化碳已集满的方法是___________ 。
(4)若用装置F收集CO2气体,要将水换成温水,其理由是___________ 。
(5)实验室用装置C制取氢气,打开止水夹,发现稀硫酸未能与多孔塑料板上锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是___________(填字母)。

(1)写出编号仪器名称:a
(2)用高锰酸钾制取氧气,选择B作发生装置,需要补充的实验用品是
(3)实验室制取CO2的化学方程式为
(4)若用装置F收集CO2气体,要将水换成温水,其理由是
(5)实验室用装置C制取氢气,打开止水夹,发现稀硫酸未能与多孔塑料板上锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是___________(填字母)。
| A.氢氧化钠溶液 | B.碳酸钠溶液 | C.硫酸钠溶液 | D.澄清石灰水 |
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为探究分子的运动情况,在课本实验图甲的基础上进行改进,如图乙进行实验一和实验二:
在T形管的粗玻璃管里,固定一根湿润的酚酞滤纸条,完成下列实验。
实验一:将浓氨水加入左侧试管中,3分钟后观察到ba段滤纸条先变红。
实验二:换一根湿润的酚酞滤纸条,微微加热试管,观察。
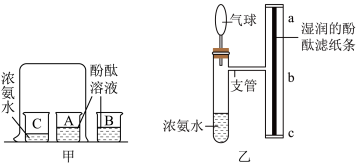
(1)图甲可观察到现象是________ 。
(2)实验一说明相同条件下氨气的密度比空气_______ (填“大”或“小”)。
(3)实验二现象为________ ,对比实验一和实验二可得出结论是_________ 。
(4)实验中使用气球目的是为了________ 。
(5)图甲实验与图乙实验对比,改进后的优点是________ 。
在T形管的粗玻璃管里,固定一根湿润的酚酞滤纸条,完成下列实验。
实验一:将浓氨水加入左侧试管中,3分钟后观察到ba段滤纸条先变红。
实验二:换一根湿润的酚酞滤纸条,微微加热试管,观察。

(1)图甲可观察到现象是
(2)实验一说明相同条件下氨气的密度比空气
(3)实验二现象为
(4)实验中使用气球目的是为了
(5)图甲实验与图乙实验对比,改进后的优点是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】为探究催化剂对过氧化氢溶液分解的催化效果,某研究小组做了如下实验。
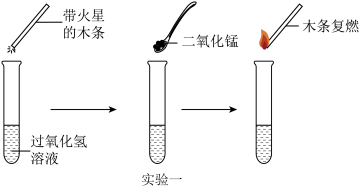
实验二:数据记录表
(1)实验一图中的实验能否证明二氧化锰是过氧化氢分解反应的催化剂?并说明理由:___________ 。
(2)实验二:从表格的设计可以看出,该实验的目的是__________ 。
(3)写出该反应的化学方程式:____________ 。
(4)造成实验二后面数据不变的原因可能是_________ (写一条)。

实验二:数据记录表
 的过氧化氢溶液 的过氧化氢溶液 |  |  |  |  |  |  |
加入二氧化锰的质量 | 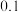 |  |  | 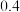 | 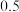 | 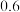 |
测量 末收集氧气的体积 末收集氧气的体积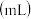 |  | 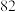 |  |  |  |  |
(1)实验一图中的实验能否证明二氧化锰是过氧化氢分解反应的催化剂?并说明理由:
(2)实验二:从表格的设计可以看出,该实验的目的是
(3)写出该反应的化学方程式:
(4)造成实验二后面数据不变的原因可能是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】为探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330℃或380℃,(其他实验条件见下表),并设计了以下实验。
请回答:
(1)通过比较待测值大小来判断反应的速率,则待测值指的是____________ 。
(2)进行实验②和③,并进行对比,其实验目的是____ ;实验③反应的文字表达式:___ 。
(3)用实验③和④探究温度对氯酸钾分解速率的影响,则二氧化锰的质量是_______ g,若实验③的待测值小于④,则得到的实验结论:_______ 。
【继续探究】氯酸钾(KClO3)和氧化铁(Fe2O3)的质量比会不会影响反应的快慢?
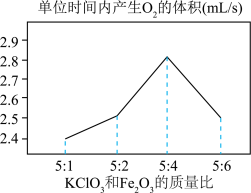
(4)调节氯酸钾和氧化铁的质量比制备氧气,整理数据绘制出如图,从图中得出氯酸钾(KClO3)和氧化铁(Fe2O3)反应的最佳质量比是________ 。
(5)测量气体体积时,可以将反应的发生装置和倒置量筒连接(如图所示),读数时慢慢上下移动量筒,使量筒内外液面高度相同,目的是:________ ;为了提高测量结果的准确率,则收集气体应选图中的______ (填A或B)。
(6)测量气体体积开始前,量筒内上方未排出的空气,使测量结果______ (填偏大、偏小或不变)。读数操作正确的情况下,测得的气体体积比理论上生成的氧气体积大,可能原因是_____ 。
(7)如图所示,在KClO3和Fe2O3质量比为5:4之前,氧化铁质量越多,反应越快的原因:__ 。

| 实验编号 | 氯酸钾的质量 | 催化剂及其质量/g | 温度/℃ | 反应的时间/s | 待测值 |
| ① | 2.0 | 无 | 330 | 100 | |
| ② | 2.0 | 氧化铁0.5 | 330 | 100 | |
| ③ | 2.0 | 二氧化锰0.5 | 330 | 100 | |
| ④ | 2.0 | 二氧化锰? | ? | 100 |
(1)通过比较待测值大小来判断反应的速率,则待测值指的是
(2)进行实验②和③,并进行对比,其实验目的是
(3)用实验③和④探究温度对氯酸钾分解速率的影响,则二氧化锰的质量是
【继续探究】氯酸钾(KClO3)和氧化铁(Fe2O3)的质量比会不会影响反应的快慢?
(4)调节氯酸钾和氧化铁的质量比制备氧气,整理数据绘制出如图,从图中得出氯酸钾(KClO3)和氧化铁(Fe2O3)反应的最佳质量比是

(5)测量气体体积时,可以将反应的发生装置和倒置量筒连接(如图所示),读数时慢慢上下移动量筒,使量筒内外液面高度相同,目的是:
(6)测量气体体积开始前,量筒内上方未排出的空气,使测量结果
(7)如图所示,在KClO3和Fe2O3质量比为5:4之前,氧化铁质量越多,反应越快的原因:

您最近一年使用:0次




