小李用右图气体发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶。
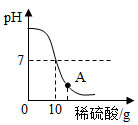
(1)小李要把稀盐酸选出,可选用下列的________来检验。
A硝酸银溶液 B.酚酞试液 C.pH试纸
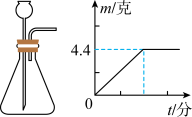
(2)小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如右图所示,最后还有少量石灰石剩余。根据图象可知,最终生成二氧化碳的质量为________克。所用稀盐酸的溶质质量分数是多少?_________写出计算过程(不计水蒸发和稀盐酸的挥发)。

(1)小李要把稀盐酸选出,可选用下列的________来检验。
A硝酸银溶液 B.酚酞试液 C.pH试纸
(2)小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如右图所示,最后还有少量石灰石剩余。根据图象可知,最终生成二氧化碳的质量为________克。所用稀盐酸的溶质质量分数是多少?_________写出计算过程(不计水蒸发和稀盐酸的挥发)。
2017九年级下·江苏·专题练习 查看更多[2]
更新时间:2016-11-27 16:33:15
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有188.8g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为205g。计算:
(1)生成二氧化碳的质量_____;
(2)反应后所得溶液中溶质的质量分数______。
(1)生成二氧化碳的质量_____;
(2)反应后所得溶液中溶质的质量分数______。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定石灰石中碳酸钙的纯度,取石灰石样品 克与一定量
克与一定量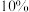 的稀盐酸在烧杯中恰好完全反应
的稀盐酸在烧杯中恰好完全反应 杂质不反应也不溶于水
杂质不反应也不溶于水 ,有关数据如表。
,有关数据如表。
请计算:
(1)根据质量守恒定律,反应生成 的质量为
的质量为_____
(2)该石灰石样品中碳酸钙的质量分数。
 克与一定量
克与一定量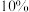 的稀盐酸在烧杯中恰好完全反应
的稀盐酸在烧杯中恰好完全反应 杂质不反应也不溶于水
杂质不反应也不溶于水 ,有关数据如表。
,有关数据如表。| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石的质量 | 烧杯和其中混合物的质量 |
 克 克 |  克 克 |  克 克 | |
(1)根据质量守恒定律,反应生成
 的质量为
的质量为(2)该石灰石样品中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】某课外小组,用大理石与盐酸反应制取二氧化碳(大理石中杂质不与盐酸反应).甲、乙、丙三同学分别进行实验,实验数据如下(烧杯的质量为25.0g).
| 烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 |
甲 | 75.0g | 13.2g | 83.8g |
乙 | 75.0g | 16.0g | 86.6g |
丙 | 95.0g | 13.2g | 103.8g |
若甲、乙、丙三同学中有一名同学所取的大理石和盐酸恰好完全反应,请回答下列问题.
(1)_____同学所取的盐酸与大理石恰好完全反应.
(2)计算大理石中碳酸钙的质量分数_________(计算结果精确到0.1%).
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品15g,加入90.4g水中配成溶液,并向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系如图所示:
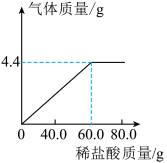
试计算:
(1)样品中Na2CO3的质量分数(计算结果精确到0.1%)
(2)恰好反应后所得溶液中溶质的质量分数。

试计算:
(1)样品中Na2CO3的质量分数(计算结果精确到0.1%)
(2)恰好反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】黄铜是铜锌合金,学校化学兴趣小组对某铜锌合金样品进行探究实验。称取样品100g,再用100.0g稀硫酸溶液逐滴滴入,实验情况如图所示,求:
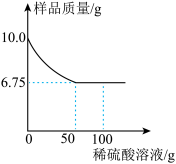
(1)样品中铜的质量为 g。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
(3)黄铜外观与黄金很相似,以假乱真。区分黄铜和黄金除了加入稀硫酸或稀盐酸以外,还有 (写一种)。

(1)样品中铜的质量为 g。
(2)所用稀硫酸溶液中溶质的质量分数是多少?
(3)黄铜外观与黄金很相似,以假乱真。区分黄铜和黄金除了加入稀硫酸或稀盐酸以外,还有 (写一种)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】碱式碳酸铜[Cu2(OH)2CO3]常用于烟花、农药等行业、将CuSO4溶液和Na2CO3溶液混合可制备碱式碳酸铜[Cu2(OH)2CO3],反应原理为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+CO2↑+2Na2SO4。某小组同学利用该原理制备碱式碳酸铜,并测定所用CuSO4溶液的质量分数。
(1)实验测得所取用的CuSO4溶液的pH=6,则该CuSO4溶液呈______ (填“酸性”“碱性”或“中性”)。
(2)已知碱性条件下有利于大颗粒碱式碳酸铜的生成,为了得到较大颗粒的碱式碳酸铜,混合碳酸钠和硫酸铜两溶液的操作方法是______ 。
(3)取100gCuSO4溶液和足量的碳酸钠溶液按(2)中正确方法混合后,过滤,将所得的沉淀过滤、洗涤、低温烘干后称量,质量为2.22g。
①计算所取CuSO4溶液的质量分数______ 。
②如没有对所得沉淀进行洗涤,则CuSO4溶液的质量分数将______ (填“偏大”“偏小”或“无影响”)。
(1)实验测得所取用的CuSO4溶液的pH=6,则该CuSO4溶液呈
(2)已知碱性条件下有利于大颗粒碱式碳酸铜的生成,为了得到较大颗粒的碱式碳酸铜,混合碳酸钠和硫酸铜两溶液的操作方法是
(3)取100gCuSO4溶液和足量的碳酸钠溶液按(2)中正确方法混合后,过滤,将所得的沉淀过滤、洗涤、低温烘干后称量,质量为2.22g。
①计算所取CuSO4溶液的质量分数
②如没有对所得沉淀进行洗涤,则CuSO4溶液的质量分数将
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室欲测定一瓶标签破损的稀盐酸的溶质质量分数,现取10g稀盐酸样品,将5%的氢氧化钠溶液逐滴加入到样品中,边加边搅拌,随着氢氧化钠溶液的加入,溶液pH的变化情况如图所示。请回答:
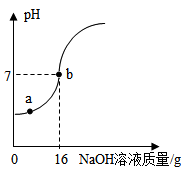
(1)a点溶液中含有的离子是_____________ (填写化学符号)。
(2)pH=7时,消耗氢氧化钠的质量为_____________ g。
(3)计算稀盐酸的溶质质量分数。(计算结果精确至0.1%)。

(1)a点溶液中含有的离子是
(2)pH=7时,消耗氢氧化钠的质量为
(3)计算稀盐酸的溶质质量分数。(计算结果精确至0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在盛有40g溶质质量分数为20%氢氧化钠溶液的烧杯中,用滴管吸取盐酸逐滴向其中加入,以此验证 “中和反应会放热”,同时用pH计记录溶液pH的变化,绘制成如图所示的函数图象.
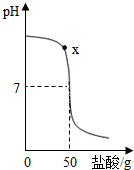
(1)用玻璃棒蘸取x点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有_____ (填化学式)
(2)为什么不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”?______________ 。
(3)当pH=7时,溶液中溶质的质量分数是___________ 。

(1)用玻璃棒蘸取x点溶液,在酒精灯火焰上加热至蒸干,玻璃棒上留下的固体中一定含有
(2)为什么不能用氢氧化钠固体和稀盐酸反应验证“中和反应会放热”?
(3)当pH=7时,溶液中溶质的质量分数是
您最近一年使用:0次