一次用餐中,小丽同学对“固体酒精”产生好奇,于是她对其进行研究。
【收集资料】①固体酒精中含有酒精、氢氧化钠、氯化钙等物质 ②酒精的化学式为C2H5OH
【提出问题】(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是否显碱性?从下面试剂中选择合适试剂进行鉴别_____ (填字母)
A硫酸铜 B氯化钠 C硝酸钾 D酚酞
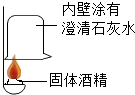
(2)酒精中是否含有碳元素?按如图实验,发现澄清石灰水_____ 。可得出酒精中含有碳元素的结论。
(3)氢氧化钠是否变质?取少量固体酒精于烧杯中,加足量的蒸馏水溶解,发现烧杯底部有白色沉淀,分析实验并结合资料得出氢氧化钠已变质。进一步探究氢氧化钠是否完全变质。
限选试剂:氢氧化钡溶液、硝酸钙溶液、硝酸钡溶液、稀硫酸、稀盐酸、稀硝酸、酚酞溶液
【收集资料】①固体酒精中含有酒精、氢氧化钠、氯化钙等物质 ②酒精的化学式为C2H5OH
【提出问题】(1)酒精的化学式与NaOH相比,都有“OH”,那么酒精的水溶液是否显碱性?从下面试剂中选择合适试剂进行鉴别
A硫酸铜 B氯化钠 C硝酸钾 D酚酞
(2)酒精中是否含有碳元素?按如图实验,发现澄清石灰水

(3)氢氧化钠是否变质?取少量固体酒精于烧杯中,加足量的蒸馏水溶解,发现烧杯底部有白色沉淀,分析实验并结合资料得出氢氧化钠已变质。进一步探究氢氧化钠是否完全变质。
限选试剂:氢氧化钡溶液、硝酸钙溶液、硝酸钡溶液、稀硫酸、稀盐酸、稀硝酸、酚酞溶液
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取上述实验步骤烧杯中的上层清液于试管中,滴入 | 证明固体酒精中有碳酸钠和氢氧化钠,固体酒精部分变质 | |
| 2. |
更新时间:2019-09-26 23:15:41
|
相似题推荐
科学探究题
|
较难
(0.4)
【推荐1】生石灰(CaO)是一种传统的建筑材料,工业上通过在石灰窑中煅烧石灰石(CaCO3)制得二氧化碳和生石灰,其反应原理是: ,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
【提出问题】刚出窑的“生石灰”有哪些成分?
【作出猜想】1.只有氧化钙Ⅱ.只有碳酸钙 Ⅲ.既有氧化钙也有碳酸钙
【查阅资料】石灰石不溶于水,生石灰能和水发生化合反应,放出大量的热,生成熟石灰[Ca(OH)2],其反应原理是:CaO+H2O=Ca(OH)2,熟石灰微溶于水(即:不能全部溶解)。
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立。乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是______ 。
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是______ 。
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告。
【拓展反思】使用“生石灰”的建筑工地上常有一个大的石灰池,使用“生石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用。长期使用的石灰池内壁会逐渐增厚,其主要原因是(用化学方程式表示)______ 。
 ,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。【提出问题】刚出窑的“生石灰”有哪些成分?
【作出猜想】1.只有氧化钙Ⅱ.只有碳酸钙 Ⅲ.既有氧化钙也有碳酸钙
【查阅资料】石灰石不溶于水,生石灰能和水发生化合反应,放出大量的热,生成熟石灰[Ca(OH)2],其反应原理是:CaO+H2O=Ca(OH)2,熟石灰微溶于水(即:不能全部溶解)。
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立。乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| ① ② | 猜想Ⅲ成立 |
【拓展反思】使用“生石灰”的建筑工地上常有一个大的石灰池,使用“生石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用。长期使用的石灰池内壁会逐渐增厚,其主要原因是(用化学方程式表示)
您最近一年使用:0次
【推荐2】探究氢氧化钠的变质
实验室有一瓶敞口放置的氢氧化钠固体,同学们想探究这瓶固体的成分。
请写出氢氧化钠在空气中变质的化学方程式________________________ 。
【提出猜想】猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分只有(填化学式)________________________ 。
猜想3:这瓶固体的成分是(填化学式)________________________ 。
【收集证据】
(1)取少量样品于试管中,加入适量蒸馏水振荡,样品全部溶解,向其中加入无色酚酞试液,溶液由无色变成红色。甲同学认为这瓶固体中含有氢氧化钠,乙同学认为甲同学的结论不正确,其理由是________________________ 。
【反思交流】
(2)若利用沉淀法测定该固体中碳酸钠的质量分数,你确定的反应原理是(用化学方程式表示)________________________ 。
(3)假设你取样的质量为m1,测得的沉淀的质量为m2.。
请你设计实验方案,获得数据m1、m2,把方案填在下表中。
【数据处理】
(4)请用含m1、m2的计算式表示样品中碳酸钠的质量分数_____________________ 。
实验室有一瓶敞口放置的氢氧化钠固体,同学们想探究这瓶固体的成分。
请写出氢氧化钠在空气中变质的化学方程式
【提出猜想】猜想1:这瓶固体的成分是NaOH;
猜想2:这瓶固体的成分只有(填化学式)
猜想3:这瓶固体的成分是(填化学式)
【收集证据】
(1)取少量样品于试管中,加入适量蒸馏水振荡,样品全部溶解,向其中加入无色酚酞试液,溶液由无色变成红色。甲同学认为这瓶固体中含有氢氧化钠,乙同学认为甲同学的结论不正确,其理由是
【反思交流】
(2)若利用沉淀法测定该固体中碳酸钠的质量分数,你确定的反应原理是(用化学方程式表示)
(3)假设你取样的质量为m1,测得的沉淀的质量为m2.。
请你设计实验方案,获得数据m1、m2,把方案填在下表中。
| 选用的仪器名称 | 实验步骤 |
【数据处理】
(4)请用含m1、m2的计算式表示样品中碳酸钠的质量分数
您最近一年使用:0次
【推荐3】下面是兴趣小组同学对暴露在空气的氢氧化钠固体的探究。请回答下列问题:
[提出问题1]:该氢氧化钠固体有没有变质呢?
[进行实验1]:甲同学取少量固体于试管中用足量的水溶解,后加入过量的 BaCl2溶液,观察到______ ,证明氢氧化钠固体已经含有 Na2CO3。
[提出问题2]:如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
[进行实验2]:乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验。

[实验分析]:
(1)步骤②反应的化学方程式是______ ,步骤②的操作有搅拌和过滤,搅拌的作用是______ 。
(2)证明步骤②中已达到 Ca(OH)2溶液过量的目的,下列方案中可行的是______ 。
a、取少量滤液 B,向其中通二氧化碳气体,溶液变浑浊
b、取少量溶液 B,向其中再加少量石灰水,无白色浑浊
c、取少量溶液 B,向其中再加少量浓碳酸钠溶液,有白色浑浊
(3)为获得纯净的氢氧化钠步骤③所包含的具体操作是蒸发浓缩、______ 、过滤。(A.蒸发结晶 B.降温结晶)
(4)丙同学认为乙同学流程中的 Ca(OH)2溶液可以用稍过量的CaCl2溶液代替,乙同学认为不可以,你认为他的理由是______ 。
[实验拓展]:如何测定久置的烧碱样品中氢氧化钠的质量分数呢?
从一瓶久置的烧碱中称取了20g,干燥后剩余固体质量为 19g,完全溶于蒸馏水中配成 100g 样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反 应后得到如表所示的数据。
(5)表中第______ 次恰好完全反应。
(6)请计算干燥后剩余固体样品中氢氧化钠的质量分数?______ (请写具体解题过程)
[提出问题1]:该氢氧化钠固体有没有变质呢?
[进行实验1]:甲同学取少量固体于试管中用足量的水溶解,后加入过量的 BaCl2溶液,观察到
[提出问题2]:如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
[进行实验2]:乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验。

[实验分析]:
(1)步骤②反应的化学方程式是
(2)证明步骤②中已达到 Ca(OH)2溶液过量的目的,下列方案中可行的是
a、取少量滤液 B,向其中通二氧化碳气体,溶液变浑浊
b、取少量溶液 B,向其中再加少量石灰水,无白色浑浊
c、取少量溶液 B,向其中再加少量浓碳酸钠溶液,有白色浑浊
(3)为获得纯净的氢氧化钠步骤③所包含的具体操作是蒸发浓缩、
(4)丙同学认为乙同学流程中的 Ca(OH)2溶液可以用稍过量的CaCl2溶液代替,乙同学认为不可以,你认为他的理由是
[实验拓展]:如何测定久置的烧碱样品中氢氧化钠的质量分数呢?
从一瓶久置的烧碱中称取了20g,干燥后剩余固体质量为 19g,完全溶于蒸馏水中配成 100g 样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反 应后得到如表所示的数据。
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 样品溶液质量(g) | 10 | 20 | 30 | 40 |
| 氯化钡溶液质量(g) | 10 | 15 | 15 | 30 |
| 产生沉淀的质量(g) | 1.97 | 3.94 | 3.94 | X |
(5)表中第
(6)请计算干燥后剩余固体样品中氢氧化钠的质量分数?
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重。醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用。交警对呼气酒精检验的原理是:橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:__________
【实验探究】
【实验反思】操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?________ ,理由是__________ 。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | 猜想3成立 | |
| ② |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组在进行酸碱中和反应的实验时,先向烧杯中加入适量稀盐酸,并滴加几滴酚酞溶液,然后用滴管慢慢滴入稀氢氧化钠溶液,并不断搅拌,一会儿后停止滴加氢氧化钠溶液,观察到烧杯中溶液为无色。同学们对反应后的溶液M的成分进行如下探究:
【猜想假设】
猜想Ⅰ:氢氧化钠过量,溶液M呈碱性。
猜想Ⅱ:氢氧化钠与盐酸恰好完全中和,溶液M呈中性
猜想Ⅲ:________ 。
同学们经过讨论后认为猜想Ⅰ不正确,其理由是_______ 。
【实验探究】
(1)为了验证自己的猜想,小明设计了实验方案一:
(2)小强设计了实验方案二:
【分析评价】
同学们对小强的实验方案进行了分析,认为他的实验结论不正确。如果猜想Ⅱ正确,按照方案二的实验操作,也会生成白色沉淀,此时发生反应的化学方程式为________ 。
【再次探究】
如果要验证猜想Ⅲ正确,可以设计实验方案三:取少量溶液M于试管中,然后分别加入下列物质进行实验,能观察到明显现象并得出正确结论的是________ (填序号)。
①锌粒 ②铜丝 ③二氧化碳 ④氧化铁 ⑤氢氧化钾 ⑥硫酸铜 ⑦碳酸钙 ⑧硝酸铵
【猜想假设】
猜想Ⅰ:氢氧化钠过量,溶液M呈碱性。
猜想Ⅱ:氢氧化钠与盐酸恰好完全中和,溶液M呈中性

猜想Ⅲ:
同学们经过讨论后认为猜想Ⅰ不正确,其理由是
【实验探究】
(1)为了验证自己的猜想,小明设计了实验方案一:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液M于试管中,滴加紫色石蕊溶液 | 溶液显 | 猜想Ⅱ正确 |
(2)小强设计了实验方案二:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液M于试管中,滴加硝酸银溶液和稀硝酸 | 产生白色沉淀 | 猜想Ⅲ正确 |
【分析评价】
同学们对小强的实验方案进行了分析,认为他的实验结论不正确。如果猜想Ⅱ正确,按照方案二的实验操作,也会生成白色沉淀,此时发生反应的化学方程式为
【再次探究】
如果要验证猜想Ⅲ正确,可以设计实验方案三:取少量溶液M于试管中,然后分别加入下列物质进行实验,能观察到明显现象并得出正确结论的是
①锌粒 ②铜丝 ③二氧化碳 ④氧化铁 ⑤氢氧化钾 ⑥硫酸铜 ⑦碳酸钙 ⑧硝酸铵
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
【推荐3】某化学兴趣小组对“制镁企业不能使用CO2灭火器作为消防器材”的问题进行探究,请你参与他们的活动。
(1)二氧化碳的制备
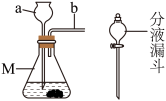
用如图所示实验装置制备CO2,写出仪器M的名称:______ ;组装时,仪器a、b插入双孔橡皮塞的先后顺序是 _____ (填序号);若将长颈漏斗换为分液漏斗,其优点是 ___________________ 。该反应选用CaCO3与稀盐酸制取CO2,请写出反应的化学方程式: _______________________ 。
(2)探究镁与二氧化碳的反应
兴趣小组同学将点燃的镁条插入盛满CO2的集气瓶内,镁条继续剧烈燃烧,生成白色固体并有黑色物质附着于集气瓶内壁。同学们对镁与CO2反应的产物继续进行探究。
【提出猜想】
猜想Ⅰ:产物是MgO和C;
猜想Ⅱ:产物是MgO、MgC2和C。
提出以上猜想的依据是_______________________ 。
【查阅资料】MgO+H2O=Mg(OH)2,Mg(OH)2在热水中的溶解度增大;
MgC2+2H2O=Mg(OH)2+C2H2↑。
【实验分析】为探究白色固体的成分,兴趣小组同学进行了如下实验:
①取少量反应后的固体混合物放入试管,加入足量热水,无气体放出,说明猜想_______ 不正确;
②为了验证另一种猜想中白色固体成分,请设计一个简单实验。
实验操作_______________ ;
实验现象_______________ 。
若该猜想正确,此时Mg与CO2反应的类型属于_______________ 。
【实验反思】通过本实验,对“CO2不助燃”,你有什么新的认识:______________ 。
(1)二氧化碳的制备
用如图所示实验装置制备CO2,写出仪器M的名称:

(2)探究镁与二氧化碳的反应
兴趣小组同学将点燃的镁条插入盛满CO2的集气瓶内,镁条继续剧烈燃烧,生成白色固体并有黑色物质附着于集气瓶内壁。同学们对镁与CO2反应的产物继续进行探究。
【提出猜想】
猜想Ⅰ:产物是MgO和C;
猜想Ⅱ:产物是MgO、MgC2和C。
提出以上猜想的依据是
【查阅资料】MgO+H2O=Mg(OH)2,Mg(OH)2在热水中的溶解度增大;
MgC2+2H2O=Mg(OH)2+C2H2↑。
【实验分析】为探究白色固体的成分,兴趣小组同学进行了如下实验:
①取少量反应后的固体混合物放入试管,加入足量热水,无气体放出,说明猜想
②为了验证另一种猜想中白色固体成分,请设计一个简单实验。
实验操作
实验现象
若该猜想正确,此时Mg与CO2反应的类型属于
【实验反思】通过本实验,对“CO2不助燃”,你有什么新的认识:
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组的同学做完“大理石和稀盐酸制取二氧化碳的实验”后,将反应后锥形瓶中残留的废液过滤,并对滤液进行探究(已知大理石中所含杂质既不溶于水,也不与酸反应)。
【提出问题】滤液中所含溶质是什么?
【查阅资料】氯化钙溶液呈中性
【猜想与假设】
猜想1:滤液中的溶质可能是CaCl2和CaCO3
猜想2:滤液中的溶质只有CaCl2
猜想3:滤液中的溶质是_________
【讨论与交流】
小明认为猜想1无需验证就知道是错误的,他的理由是_________ 。
【实验与结论】
(1)小亮同学为验证猜想2,取少量滤液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮认为猜想2正确。你认为他的结论_________ (填“正确”或“错误”),理由是 _____________ 。
(2)小美为验证猜想3,用洁净干燥的玻璃棒蘸取该滤液滴到湿润的pH试纸上,测得pH=4,她认为猜想3正确。对她的操作方法、测量结果及结论的评价,正确的是__________ 。
A 方法不正确,结果偏小,结论正确
B 方法正确,结果偏大,结论不正确
C 方法不正确,结果偏大,结论正确
D 方法正确,结果偏小,结论不正确
(3)小丽选择了其他几种不同类别的物质来验证猜想3,也得出了结论,可供选择的试剂有:石蕊溶液、铜片、镁条、氧化钙、氧化铁、氢氧化钠、氢氧化铜、碳酸钠溶液、硝酸银溶液
请完成下表:
【反思与评价】上述方案有错误及错误的原因是 ______________ (填写错误方案的序号,并解释其错误的原因)。
【拓展与延伸】
若猜想3成立,小丽认为无需另加试剂,只要对滤液进行________________ 操作即可除去杂质,从滤液中得到CaCl2固体。
(4)小丽同学取了100g 滤液,逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与溶液pH的关系如下图所示。

试回答下列问题:
① 写出首先发生的反应的化学方程式________________ ;
② a点对应的溶液中溶质为_________ ;
③ 恰好完全反应时所得溶液中溶质的质量分数为____________ 。(写出计算过程,结果精确到0.1%)
【提出问题】滤液中所含溶质是什么?
【查阅资料】氯化钙溶液呈中性
【猜想与假设】
猜想1:滤液中的溶质可能是CaCl2和CaCO3
猜想2:滤液中的溶质只有CaCl2
猜想3:滤液中的溶质是
【讨论与交流】
小明认为猜想1无需验证就知道是错误的,他的理由是
【实验与结论】
(1)小亮同学为验证猜想2,取少量滤液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮认为猜想2正确。你认为他的结论
(2)小美为验证猜想3,用洁净干燥的玻璃棒蘸取该滤液滴到湿润的pH试纸上,测得pH=4,她认为猜想3正确。对她的操作方法、测量结果及结论的评价,正确的是
A 方法不正确,结果偏小,结论正确
B 方法正确,结果偏大,结论不正确
C 方法不正确,结果偏大,结论正确
D 方法正确,结果偏小,结论不正确
(3)小丽选择了其他几种不同类别的物质来验证猜想3,也得出了结论,可供选择的试剂有:石蕊溶液、铜片、镁条、氧化钙、氧化铁、氢氧化钠、氢氧化铜、碳酸钠溶液、硝酸银溶液
请完成下表:
| 方案 | 试剂类别 | 选用试剂 | 实验现象 | 结论 |
| A | 指示剂 | 石蕊溶液 | 溶液变红 | 猜想3 正确 |
| B | 金属单质 | 固体表面产生气泡 | ||
| C | 金属氧化物 | 氧化铁 | ||
| D | 氢氧化铜 | 固体溶解,溶液变成蓝色 | ||
| E | 盐 | 硝酸银溶液 | 产生白色沉淀 |
【拓展与延伸】
若猜想3成立,小丽认为无需另加试剂,只要对滤液进行
(4)小丽同学取了100g 滤液,逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与溶液pH的关系如下图所示。

试回答下列问题:
① 写出首先发生的反应的化学方程式
② a点对应的溶液中溶质为
③ 恰好完全反应时所得溶液中溶质的质量分数为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】松花蛋,又称皮蛋、变蛋。其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg。加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍。
请回答下列问题:
(1)鸭蛋中富含的营养素有水和_________ 。
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是_________ 。
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为________ 色。
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动。
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质: 甲同学推断有Ca(OH)2;乙同学推断有Na2CO3;丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是_______ 。
【实验探究】
【探究结论】_____ 同学的推断是正确的。
【知识应用】皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是______ 。
(5)某同学在实验室做实验时,要中和质量分数为10%的烧碱溶液16克,则他需要溶质质量分数为9.8%的稀硫酸是___ 克。
请回答下列问题:
(1)鸭蛋中富含的营养素有水和
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动。
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质: 甲同学推断有Ca(OH)2;乙同学推断有Na2CO3;丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液, | 产生白色沉淀 |
【知识应用】皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是
(5)某同学在实验室做实验时,要中和质量分数为10%的烧碱溶液16克,则他需要溶质质量分数为9.8%的稀硫酸是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱。某小组同学按题下图所示流程进行实验,请你参与探究并回答相关问题。

(1)贝壳高温锻烧时,发生反应的化学方程式是___________ 。
(2)操作I中用到的玻璃仪器有烧杯、_____________ 、玻璃棒;
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是______________ ;
(4)【问题与发现】该小组同学所得固体C一定是纯净的NaOH吗?
[猜想与假设]根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH
乙:NaOH和Na2CO3的混合物
丙:NaOH和_______ 的混合物
(5)【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证。实验操作、现象和结论如下表,请参与他们的探究并完成所缺内容。
(6)【反思与评价】 同学们认真研究实验流程,讨论后一致认为______ 同学的实验方案不正确,理由是 ____________________________ 。
(7)【拓展】请设计实验方案验证实验室久置的氢氧化钠溶液已经部分变质:___________ 。

(1)贝壳高温锻烧时,发生反应的化学方程式是
(2)操作I中用到的玻璃仪器有烧杯、
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是
(4)【问题与发现】该小组同学所得固体C一定是纯净的NaOH吗?
[猜想与假设]根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH
乙:NaOH和Na2CO3的混合物
丙:NaOH和
(5)【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证。实验操作、现象和结论如下表,请参与他们的探究并完成所缺内容。
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量的 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和Na2CO3溶液 | 猜想成立 |
(6)【反思与评价】 同学们认真研究实验流程,讨论后一致认为
(7)【拓展】请设计实验方案验证实验室久置的氢氧化钠溶液已经部分变质:
您最近一年使用:0次



