生石灰(CaO)是一种传统的建筑材料,工业上通过在石灰窑中煅烧石灰石(CaCO3)制得二氧化碳和生石灰,其反应原理是: ,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
【提出问题】刚出窑的“生石灰”有哪些成分?
【作出猜想】1.只有氧化钙Ⅱ.只有碳酸钙 Ⅲ.既有氧化钙也有碳酸钙
【查阅资料】石灰石不溶于水,生石灰能和水发生化合反应,放出大量的热,生成熟石灰[Ca(OH)2],其反应原理是:CaO+H2O=Ca(OH)2,熟石灰微溶于水(即:不能全部溶解)。
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立。乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是______ 。
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是______ 。
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告。
【拓展反思】使用“生石灰”的建筑工地上常有一个大的石灰池,使用“生石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用。长期使用的石灰池内壁会逐渐增厚,其主要原因是(用化学方程式表示)______ 。
 ,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。
,兴趣小组的同学,对某地刚出窑的生石灰的成分进行探究。【提出问题】刚出窑的“生石灰”有哪些成分?
【作出猜想】1.只有氧化钙Ⅱ.只有碳酸钙 Ⅲ.既有氧化钙也有碳酸钙
【查阅资料】石灰石不溶于水,生石灰能和水发生化合反应,放出大量的热,生成熟石灰[Ca(OH)2],其反应原理是:CaO+H2O=Ca(OH)2,熟石灰微溶于水(即:不能全部溶解)。
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立。乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
| ① ② | 猜想Ⅲ成立 |
【拓展反思】使用“生石灰”的建筑工地上常有一个大的石灰池,使用“生石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用。长期使用的石灰池内壁会逐渐增厚,其主要原因是(用化学方程式表示)
更新时间:2019-03-16 08:56:09
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】化学兴趣小组的同学进行了以下实验:向烧杯中加入变质的氢氧化钙固体和一定量的稀盐酸,一段时间后固体全部溶解.他们对所得溶液中的溶质成分进行了探究.
探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:_____ ; 猜想二:CaCl2和HCl;
猜想三:CaCl2和Ca(OH)2; 猜想四:CaCl2、Ca(OH)2和HCl
根据所学知识判断,_____ 一定不成立.
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性.
【进行实验】
实验步骤:取少量烧杯内溶液加入试管中,滴入几滴酚酞溶液,振荡.
实验现象1:_____ .结论:猜想三不成立.
实验步骤:取少量烧杯内溶液加入另一支试管中,逐滴加入碳酸钠溶液至过量.
实验现象2:_____ .结论:猜想一不成立,猜想二成立.
【反思与拓展】
(1)碱性较强的液体直接进入下水道,会污染环境.要处理上述烧杯内的溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的_____ .
A CaO B CaCO3 C Ca(OH)2
(2)氢氧化钠在空气中变质的化学方程式_____ .
探究烧杯内溶液中溶质的成分.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:
猜想三:CaCl2和Ca(OH)2; 猜想四:CaCl2、Ca(OH)2和HCl
根据所学知识判断,
【查阅资料】氯化钙溶液呈中性,碳酸钠溶液呈碱性.
【进行实验】
实验步骤:取少量烧杯内溶液加入试管中,滴入几滴酚酞溶液,振荡.
实验现象1:
实验步骤:取少量烧杯内溶液加入另一支试管中,逐滴加入碳酸钠溶液至过量.
实验现象2:
【反思与拓展】
(1)碱性较强的液体直接进入下水道,会污染环境.要处理上述烧杯内的溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的
A CaO B CaCO3 C Ca(OH)2
(2)氢氧化钠在空气中变质的化学方程式
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组的同学在进行专题复习时,围绕酸、碱中和反应这一主题展开了深度学习。请你参与其中,按要求回答问题和开展探究。
(1)下列选项的应用与中和反应的原理无关的是_______ 。
A使用浓硫酸干燥CO2气体
B使用熟石灰改良酸性土壤
C服用含有A1(OH)3的药物治疗胃酸过多症
D利用氢氧化钠溶液洗涤石油产品中的残余硫酸
(2)做酸碱中和反应实验时,向烧杯内的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂。因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究。
(提出问题)该烧杯中溶液的溶质是什么?
(猜想假设)猜想一:只含有CaCl2猜想二:含有CaCl2、HCl和Ca(OH)2
猜想三:含有CaCl2和Ca(OH)2猜想四:含有CaCl2、HCl
同学们讨论后一致认为猜想二不合理,理由是________ 。
(查阅资料)氯化钙溶液呈中性。
(设计实验)同学们设计了不同的实验方案,证明猜想四是成立的。
其中一种方法是将一颗生锈铁钉放入试管中,取一定量烧杯中的溶液加入其中,观察到的实验现象是______ (答出两点)。
(反思评价)要使烧杯内溶液的溶质只含有CaCl2,选择的一种除杂方法是向烧杯中加入过量的碳酸钙,然后过滤,有关反应的化学方程式为_________ 。
(拓展延伸)(1)同学们想用氢氧化钠和稀盐酸重新做中和反应实验,发现所用的氢氧化钠溶液已完全变质,原因是_________ (用语言叙述)。
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有________ 。
(1)下列选项的应用与中和反应的原理无关的是
A使用浓硫酸干燥CO2气体
B使用熟石灰改良酸性土壤
C服用含有A1(OH)3的药物治疗胃酸过多症
D利用氢氧化钠溶液洗涤石油产品中的残余硫酸
(2)做酸碱中和反应实验时,向烧杯内的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂。因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究。
(提出问题)该烧杯中溶液的溶质是什么?
(猜想假设)猜想一:只含有CaCl2猜想二:含有CaCl2、HCl和Ca(OH)2
猜想三:含有CaCl2和Ca(OH)2猜想四:含有CaCl2、HCl
同学们讨论后一致认为猜想二不合理,理由是
(查阅资料)氯化钙溶液呈中性。
(设计实验)同学们设计了不同的实验方案,证明猜想四是成立的。
其中一种方法是将一颗生锈铁钉放入试管中,取一定量烧杯中的溶液加入其中,观察到的实验现象是
(反思评价)要使烧杯内溶液的溶质只含有CaCl2,选择的一种除杂方法是向烧杯中加入过量的碳酸钙,然后过滤,有关反应的化学方程式为
(拓展延伸)(1)同学们想用氢氧化钠和稀盐酸重新做中和反应实验,发现所用的氢氧化钠溶液已完全变质,原因是
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有

您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐3】某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,请你一起参与.
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】
猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙.
猜想②:氢氧化钙溶液可能部分变质,其成分是________ .
【实验探究】
【反思拓展】
(1)氢氧化钙露置于空气中容易变质,原因是___________ (用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是__________ .
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】
猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙.
猜想②:氢氧化钙溶液可能部分变质,其成分是
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸 | 有 | 原溶液里一定有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液成红色 | 原溶液一定有 |
【反思拓展】
(1)氢氧化钙露置于空气中容易变质,原因是
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是
您最近一年使用:0次
【推荐1】化学兴趣小组的同学将一小块生石灰投入盛有Na₂CO₃溶液的烧杯中,感觉到烧杯外壁发烫,经搅拌、静置后发现烧杯底部有白色不溶物。再过滤、洗涤、干燥后,得到固体A和澄清溶液B。
【分析问题】烧杯外壁发烫,是因为生石灰与水反应时会______ (填“放出”或“吸收”)热量,同时生成(Ca(OH)₂。
【实验探究】针对固体A和溶液B的成分,同学们分为两组展开了如下探究。
【表达交流】有同学指出,根据甲组实验的结论,可知固体A中含有Ca(OH)₂,则溶液B也一定是 Ca(OH)₂的饱和溶液,由此可得乙组的猜想二不成立,理由是(用化学方程式解释)______ 。
【分析问题】烧杯外壁发烫,是因为生石灰与水反应时会
【实验探究】针对固体A和溶液B的成分,同学们分为两组展开了如下探究。
| 甲组 | 乙组 | |
| 提出问题 | 固体A的成分是什么? | 溶液B的溶质是什么? |
| 理论依据 | 根据质量守恒定律可知,化学反应前后,元素的种类不发生改变 | |
| 猜想假设 | 猜想一:只有CaCO₃ 猜想二:含有CaCO₃和Ca(OH)₂ | 猜想一:只有NaOH 猜想二:含有NaOH和Na2CO₃ 猜想三:含有NaOH和Ca(OH)₂ |
| 讨论交流 | 固体A中可能含有Ca(OH)₂,理由是 | 溶液B一定呈 |
| 方案设计 | 取少量固体A于试管中,加入足量水,振荡、静置,滴加几滴 | 取少量溶液B于试管中,通入 |
| 实验现象 | 溶液变为红色 | 溶液变浑浊 |
| 得出结论 | 猜想二成立 | 猜想三成立 |
【表达交流】有同学指出,根据甲组实验的结论,可知固体A中含有Ca(OH)₂,则溶液B也一定是 Ca(OH)₂的饱和溶液,由此可得乙组的猜想二不成立,理由是(用化学方程式解释)
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐2】I、某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成。实验小组欲探究该水垢的主要成分:
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是:
①CaO ②Ca(OH)2 ③CaCO3 ④Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是___
【实验与事实】
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理:
(1)____ ,(2)________ 。
II、在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个“意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式____ .
【提出问题】该气体是什么呢?
【猜想与假设】猜想一:O2 猜想二:H2 猜想三:CO2 猜想四:SO2
同学们经过讨论,一致认为猜想三不成立,理由是___ .
【实验验证】⑴有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是___ .
⑵将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰.
【实验结论】____ .
【反思与交流】CuSO4溶液可能显____ 性(填“酸”或“碱”或“中”).
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是:
①CaO ②Ca(OH)2 ③CaCO3 ④Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是
【实验与事实】
| 实验一 | 实验现象 | 解释或结论 |
| 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 不变色说明水垢中一定没有 |
| 实验二 | 实验现象 | 解释或结论 |
 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成。则水垢中一定含有 |
(1)
II、在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个“意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式
【提出问题】该气体是什么呢?
【猜想与假设】猜想一:O2 猜想二:H2 猜想三:CO2 猜想四:SO2
同学们经过讨论,一致认为猜想三不成立,理由是
【实验验证】⑴有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是
⑵将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰.
【实验结论】
【反思与交流】CuSO4溶液可能显
您最近一年使用:0次
【推荐3】碱石灰是CaO和NaOH的混合物,实验室常用作干燥剂,久置在空气中会变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。
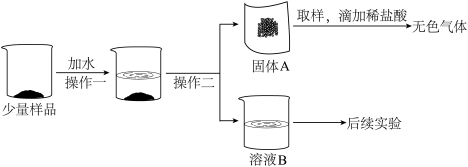
【查阅资料】①氢氧化钙、碳酸钠溶于水无明显的温度变化;
②氯化钙溶液呈中性。
(1)氢氧化钠久置在空气中会发生变质的原因是___________ (用化学方程式表示)。
(2)在操作一实验过程中,同学们发现向样品中加水时放出大量的热。据此实验,下列对样品成分分析正确的是___________(填字母)。
(3)在操作二之后所得的固体A中一定含有___________ 。
(4)实验小组的同学继续对溶液B的溶质成分进行了探究。
【猜想假设】猜想一:NaOH
猜想二:
猜想三:NaOH和
猜想四: 和
和___________
【实验验证】
【交流反思】①下列试剂中,能够替代实验中CaCl2溶液的试剂有___________ (填字母)。
A.稀盐酸 B.Ca(OH)2溶液 C.BaCl2溶液 D.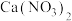 溶液
溶液
②像碱石灰这种容易变质的物质,需要注意密封保存。

【查阅资料】①氢氧化钙、碳酸钠溶于水无明显的温度变化;
②氯化钙溶液呈中性。
(1)氢氧化钠久置在空气中会发生变质的原因是
(2)在操作一实验过程中,同学们发现向样品中加水时放出大量的热。据此实验,下列对样品成分分析正确的是___________(填字母)。
| A.一定有CaO | B.一定有NaOH |
| C.至少有CaO和NaOH中的一种 | D.一定有CaO和NaOH |
(4)实验小组的同学继续对溶液B的溶质成分进行了探究。
【猜想假设】猜想一:NaOH
猜想二:

猜想三:NaOH和

猜想四:
 和
和【实验验证】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液B于试管中,加入足量的氯化钙溶液 过滤,再向滤液中加入无色酚酞溶液 | 猜想三成立 | |
A.稀盐酸 B.Ca(OH)2溶液 C.BaCl2溶液 D.
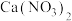 溶液
溶液②像碱石灰这种容易变质的物质,需要注意密封保存。
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】松花蛋是我国一种传统风味蛋制品。某化学课外小组的同学查阅资料后得知,腌制松花蛋的主要原料有:生石灰、纯碱和食盐。同学们向这三种物质中加入足量水,充分搅拌,过滤,对滤液中溶质的成分进行探究。
(1)小组同学讨论后一致认为,滤液中的溶质一定含有NaOH和______ (填化学式)。一定含有NaOH的原因是:①CaO+H2O=Ca(OH)2 ②______ (用化学方程式表示)。
【提出问题】滤液中还可能含有哪些溶质?
【作出猜想】猜想1:还可能有Ca(OH)2 猜想2:还可能有Na2CO3
【实验探究】同学们分别设计了如下两种方案并进行实验:
(2)方案一:甲同学取少量滤液于试管中,通入二氧化碳气体,没有观察到明显现象。从而得出猜想2成立。同学们一致认为,通过该实验不足以得出其结论,原因是______ 。
(3)方案二:乙和丙同学分别取少量滤液于试管中,滴加稀盐酸。乙同学观察到______ ,证明猜想2正确。丙同学却没有观察到明显现象,你认为原因可能是______ 。
【拓展延伸】证明猜想2正确后,同学们想进一步通过实验证明滤液中存在NaOH。于是,继续进行如下探究:
【查阅资料】氯化钡、硝酸钡、氯化钙、氯化钠溶液均显中性。
【实验探究】
【拓展提升】(5)丁同学将步骤Ⅰ中的BaCl2溶液换为其他试剂,进行以上实验,最终也得出了相同的实验结论。你认为合理试剂的是______ (填写化学式)。
(6)小芳同学认为向滤液中先加入酚酞溶液,后加入过量的BaCl2溶液,也能得出滤液中的溶质含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由______ 。
(1)小组同学讨论后一致认为,滤液中的溶质一定含有NaOH和
【提出问题】滤液中还可能含有哪些溶质?
【作出猜想】猜想1:还可能有Ca(OH)2 猜想2:还可能有Na2CO3
【实验探究】同学们分别设计了如下两种方案并进行实验:
(2)方案一:甲同学取少量滤液于试管中,通入二氧化碳气体,没有观察到明显现象。从而得出猜想2成立。同学们一致认为,通过该实验不足以得出其结论,原因是
(3)方案二:乙和丙同学分别取少量滤液于试管中,滴加稀盐酸。乙同学观察到
【拓展延伸】证明猜想2正确后,同学们想进一步通过实验证明滤液中存在NaOH。于是,继续进行如下探究:
【查阅资料】氯化钡、硝酸钡、氯化钙、氯化钠溶液均显中性。
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤Ⅰ:取少量滤液于试管中,滴加过量氯化钡溶液,静置。 | 有白色沉淀产生 | 滤液中含有NaOH |
| 步骤Ⅱ:取步骤Ⅰ中的上层清液少量于试管中,滴加酚酞溶液 | (4) |
【拓展提升】(5)丁同学将步骤Ⅰ中的BaCl2溶液换为其他试剂,进行以上实验,最终也得出了相同的实验结论。你认为合理试剂的是
(6)小芳同学认为向滤液中先加入酚酞溶液,后加入过量的BaCl2溶液,也能得出滤液中的溶质含有Na2CO3和NaOH的结论,你是否同意他的观点并说明理由
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】实验室中的药品一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组的同学对实验室里久置于空气中变质的过氧化钠(Na2O2)固体的成分进行探究。
【查阅资料】(1)Na2O2的化学性质很活泼,能与水、二氧化碳反应,相关反应的化学方程式为:
2Na2O2+2H2O=4NaOH+O2↑;
2Na2O2+2CO2=2Na2CO3+O2↑
(2)CaCl2溶液为中性
【猜想】
I:固体为Na2O2、NaOH、Na2CO3的混合物
Ⅱ:固体为NaOH和Na2CO3的混合物
Ⅲ:固体为NaOH
Ⅳ:____________ 。
【实验探究】
【反思评价】
(1)实验操作②中反应的化学方程式为________________________________________ ;
(2)实验操作②中“滴加CaCl2溶液至过量的目的是____________________________________ ;
(3)表格中实验操作③还可以采用_____ 方法得到相同结论。
【查阅资料】(1)Na2O2的化学性质很活泼,能与水、二氧化碳反应,相关反应的化学方程式为:
2Na2O2+2H2O=4NaOH+O2↑;
2Na2O2+2CO2=2Na2CO3+O2↑
(2)CaCl2溶液为中性
【猜想】
I:固体为Na2O2、NaOH、Na2CO3的混合物
Ⅱ:固体为NaOH和Na2CO3的混合物
Ⅲ:固体为NaOH
Ⅳ:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡,直至完全溶解 | 猜想I不成立 | |
| ②取少量①的溶液于试管中,滴加CaCl2溶液至过量 | 证明有Na2CO3存在 | |
| ③取少量②的溶液于试管中,加入 | 证明有NaOH存在 | |
| 综合以上实验现象,说明猜想II是成立的。 | ||
(1)实验操作②中反应的化学方程式为
(2)实验操作②中“滴加CaCl2溶液至过量的目的是
(3)表格中实验操作③还可以采用
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】实验是学习化学的重要方法。根据如图实验,回答问题。
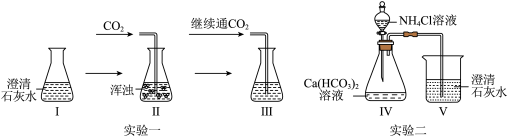
【实验一】
(1)Ⅲ中为 澄清溶液,则浑浊消失所发生反应的化学方程式为
澄清溶液,则浑浊消失所发生反应的化学方程式为__________ 。
(2)取少量 溶液缓缓加热,发现其很快变浑浊,说明
溶液缓缓加热,发现其很快变浑浊,说明 的热稳定性比
的热稳定性比
__________  填“强”或“弱”
填“强”或“弱” 。
。
【实验二】加入一定量 溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。
溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。
(1) 中石灰水变浑浊说明Ⅳ中产生的气体是
中石灰水变浑浊说明Ⅳ中产生的气体是__________ ,在 中烧杯口放湿润的红色石蕊试纸,试纸
中烧杯口放湿润的红色石蕊试纸,试纸__________ ,说明还生成了 。
。
【拓展】如实验二改加入过量 溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为
溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为__________ 。

【实验一】
(1)Ⅲ中为
 澄清溶液,则浑浊消失所发生反应的化学方程式为
澄清溶液,则浑浊消失所发生反应的化学方程式为(2)取少量
 溶液缓缓加热,发现其很快变浑浊,说明
溶液缓缓加热,发现其很快变浑浊,说明 的热稳定性比
的热稳定性比
 填“强”或“弱”
填“强”或“弱” 。
。【实验二】加入一定量
 溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。
溶液后加热锥形瓶,完全反应,瓶内出现浑浊且有气泡放出。(1)
 中石灰水变浑浊说明Ⅳ中产生的气体是
中石灰水变浑浊说明Ⅳ中产生的气体是 中烧杯口放湿润的红色石蕊试纸,试纸
中烧杯口放湿润的红色石蕊试纸,试纸 。
。【拓展】如实验二改加入过量
 溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为
溶液加热,则锥形瓶中有气泡放出且不变浑浊,其余现象与实验二相同,此时Ⅳ中反应的化学方程式为
您最近一年使用:0次



