铜与氧化铜残留物共20g,向其中加入稀硫酸,剩余固体质量与加入稀硫酸质量关系如图所示,请回答下列问题。
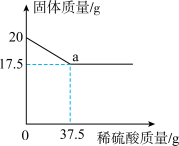
(1)所取固体残留物中铜的质量为__________ g。
(2)求a点处溶液中溶质的质量分数(写出计算过程)。

(1)所取固体残留物中铜的质量为
(2)求a点处溶液中溶质的质量分数(写出计算过程)。
2023·广西南宁·一模 查看更多[3]
更新时间:2023-03-21 11:44:44
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】2022年春晚节目《只此青绿》中“绿”指的是石绿,是古代对孔雀石的称谓,其主要成分为Cu2(OH)2CO3,也是铜锈的主要成分。实验室中有20g部分生锈的铜块,将其投入到98.22g硫酸溶液中(杂质不溶于水也不与硫酸发生反应),反应的方程式为: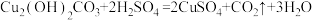 ,恰好将铜锈全部去除,反应完全后溶液和剩余固体总质量为117.78g。
,恰好将铜锈全部去除,反应完全后溶液和剩余固体总质量为117.78g。
已知:Cu2(OH)2CO3的相对分子质量为222。
请计算:
(1)生成的二氧化碳的质量为_______ g;
(2)求反应完全后剩余固体的质量?(写出计算过程,下同)
(3)反应后所得溶液中的溶质的质量分数?
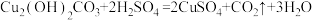 ,恰好将铜锈全部去除,反应完全后溶液和剩余固体总质量为117.78g。
,恰好将铜锈全部去除,反应完全后溶液和剩余固体总质量为117.78g。已知:Cu2(OH)2CO3的相对分子质量为222。
请计算:
(1)生成的二氧化碳的质量为
(2)求反应完全后剩余固体的质量?(写出计算过程,下同)
(3)反应后所得溶液中的溶质的质量分数?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】NaOH潮解后极易与空气中的CO2反应生成Na2CO3而变质。为测定实验室一瓶放置已久的烧碱中Na2CO3含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。
(1)反应产生的CO2的质量为 g。
(2)若所取烧碱样品为50.0g,则样品中Na2CO3的质量分数是多少?
(1)反应产生的CO2的质量为 g。
(2)若所取烧碱样品为50.0g,则样品中Na2CO3的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】课外活动小组为测定氢氧化钾的变质程度,取一定量该固体样品配制成104.4g溶液,向其中逐滴加入溶质质量分数为3.65%的稀盐酸,产生的二氧化碳与加入稀盐酸的质量关系如图所示。请回答下列问题:_______ (用化学方程式表示)。
(2)稀盐酸质量a=_______ 。
(3)求样品恰好完全反应时,所得溶液中溶质的质量分数(结果保留一位小数)。

(2)稀盐酸质量a=
(3)求样品恰好完全反应时,所得溶液中溶质的质量分数(结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定某未知浓度的氢氧化钠溶液的溶质质量分数,取19.6%的稀硫酸溶液20 g,逐滴加入氢氧化钠溶液30 g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示)。请回答下列问题。

(1)a点溶液中的溶质的化学式是__________ 。
(2)恰好完全反应时消耗的氢氧化钠溶液的质量为_____ 。
(3)通过计算求出氢氧化钠溶液的溶质质量分数。

(1)a点溶液中的溶质的化学式是
(2)恰好完全反应时消耗的氢氧化钠溶液的质量为
(3)通过计算求出氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
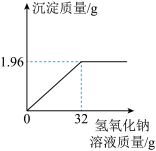
【推荐3】某化学兴趣小组欲测定一瓶失去标签的硫酸铜溶液的溶质质量分数,取该溶液20g,逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液质量的关系如图所示。___________ g;
(2)计算硫酸铜溶液的溶质质量分数(请写出计算步骤)。
(2)计算硫酸铜溶液的溶质质量分数(请写出计算步骤)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如右表:根据实验及有关数据进行分析与计算:
(1)20g样品中含氧化铜的质量为______g。
(2)根据第I组数据计算所用稀硫酸的溶质质量分数是多少?(写出计算过程)
(3)求第I组实验所得溶液中溶质的质量分数______(精确到0.1%)。
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,在图中画出滤液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。

| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀硫酸的质量/g | 50 | 100 | 150 |
| 溶解固体的质量/g | 10 | 16 | 16 |
(1)20g样品中含氧化铜的质量为______g。
(2)根据第I组数据计算所用稀硫酸的溶质质量分数是多少?(写出计算过程)
(3)求第I组实验所得溶液中溶质的质量分数______(精确到0.1%)。
(4)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,在图中画出滤液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图。

您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】为了测定某赤铁矿样品中氧化铁的含量(杂质中不含铁元素,杂质不溶于水,也不与其他物质反应),某化学小组进行了如下实验:

(1)配制上述质量分数为9.8%的稀硫酸300g,需要质量分数为98%的浓硫酸的质量是______ 。
(2)发生反应的化学方程式为___________ 。
(3)根据已知条件列出求解20g该赤铁矿样品中氧化铁的质量(x)的比例式为___________ 。
(4)该赤铁矿样品中氧化铁的含量为___________ 。
(5)向过滤后所得滤液中加入184g水,则最终所得溶液(不饱和)中溶质的质量分数________ 。
(6)现用250t此种赤铁矿炼制生铁,最终可炼得含铁90%的生铁样品的质量为140t,则炼制过程中铁元素的损失率为______ 。

(1)配制上述质量分数为9.8%的稀硫酸300g,需要质量分数为98%的浓硫酸的质量是
(2)发生反应的化学方程式为
(3)根据已知条件列出求解20g该赤铁矿样品中氧化铁的质量(x)的比例式为
(4)该赤铁矿样品中氧化铁的含量为
(5)向过滤后所得滤液中加入184g水,则最终所得溶液(不饱和)中溶质的质量分数
(6)现用250t此种赤铁矿炼制生铁,最终可炼得含铁90%的生铁样品的质量为140t,则炼制过程中铁元素的损失率为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室开放日,老师给化学兴趣小组一包氧化铜和铜的混合物样品,要求兴趣小组测定样品中氧化铜的质量分数。同学们称取5g样品于烧杯中,再把20g稀硫酸平均四次加入烧杯中并进行搅拌,让其充分反应。有关实验数据记录如下:
求:(1)样品中铜的质量为 g。
(2)样品中氧化铜的质量分数。
(3)所用稀硫酸的溶质质量分数。
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入的稀硫酸的质量/g | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体的质量/g | 4.2 | 3.4 | 3.0 | 3.0 |
求:(1)样品中铜的质量为 g。
(2)样品中氧化铜的质量分数。
(3)所用稀硫酸的溶质质量分数。
您最近一年使用:0次




