金属在日常生活的使用越来越广泛,清回答下列问题:
(1)下图中有标号的材料中,属于金属材料的是___________ 。(填标号)

(2)上图为利用数字化仪器测得的形状、大小均相同的足量的铝片、铁片分别与等质量、等浓度的稀盐酸反应时气体压强的变化。
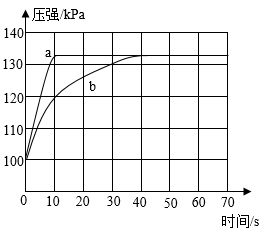
①图中表示铁片与稀盐酸反应的曲线是___________ (填“a”或“b”)。
②生活中铝制品不易被腐蚀,用化学方程式表示其原因___________ 。
③铁制品容易生锈,盐酸去铁锈的化学方程式为___________ 。
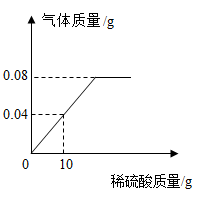
(3)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:原稀硫酸中溶质的质量分数(写出计算过程)。___________ 。
(1)下图中有标号的材料中,属于金属材料的是

(2)上图为利用数字化仪器测得的形状、大小均相同的足量的铝片、铁片分别与等质量、等浓度的稀盐酸反应时气体压强的变化。

①图中表示铁片与稀盐酸反应的曲线是
②生活中铝制品不易被腐蚀,用化学方程式表示其原因
③铁制品容易生锈,盐酸去铁锈的化学方程式为
(3)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:原稀硫酸中溶质的质量分数(写出计算过程)。

更新时间:2023-03-21 14:35:45
|
相似题推荐
【推荐1】宏观和微观相结合是认识物质结构与性质的重要方法。
(1)如图2为向铁和氧化铜的混合物中加入稀硫酸发生反应的微观过程示意图(反应容器中部分水分子没有画出)。_______ ,如图中A微粒符号为_______ 。
②反应中实际生成的微粒有Fen+、A、_______ 。
(2)为了探究Fe、Cu、Ag、R(R为未知金属)四种金属的金属活动性顺序,进行如下实验:如图甲所示,将四根金属丝同时插入烧杯中的溶液里,只观察到①中铁丝表面出现气泡,②中铁丝表面有紫红色物质;如图乙所示,一段时间后,将烧杯中铁丝替换为R丝进行实验,观察到①中R丝表面出现气泡,②中R丝表面无明显现象。“ ”“
”“ ””
”” ”为相应金属丝插入烧杯前,烧杯中溶液里存在的阳离子。
”为相应金属丝插入烧杯前,烧杯中溶液里存在的阳离子。_______ 。
(1)如图2为向铁和氧化铜的混合物中加入稀硫酸发生反应的微观过程示意图(反应容器中部分水分子没有画出)。

②反应中实际生成的微粒有Fen+、A、
(2)为了探究Fe、Cu、Ag、R(R为未知金属)四种金属的金属活动性顺序,进行如下实验:如图甲所示,将四根金属丝同时插入烧杯中的溶液里,只观察到①中铁丝表面出现气泡,②中铁丝表面有紫红色物质;如图乙所示,一段时间后,将烧杯中铁丝替换为R丝进行实验,观察到①中R丝表面出现气泡,②中R丝表面无明显现象。“
 ”“
”“ ””
”” ”为相应金属丝插入烧杯前,烧杯中溶液里存在的阳离子。
”为相应金属丝插入烧杯前,烧杯中溶液里存在的阳离子。
①图乙所示的②中存在的阳离子是 ”“
”“ ”“
”“ ”中选填)。
”中选填)。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】NiSO4·6H2O是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生产电池等行业、以一种废渣(主要成分是铁镍合金,还含有少量氧化铜等)为原料制取NiSO4·6H2O的步骤如下:
(1)为了提高“酸浸”效率,可采取的措施有______ (任写一种),该过程中产生气体的反应属于基本反应类型中的______ 反应。
(2)写出“除铜”时发生复分解反应的化学方程式:______ 。
(3)“除铁”加入H2O2溶液的目的是______ ,该过程中保持一定的温度可以更好的反应,但温度不宜过高,其原因是______ 。
(4)检验“沉镍”过程中Ni2+已完全沉淀的方法是(含实验操作及实验现象):______ 。
(5)“系列操作”主要包括硫酸溶解、______ 、冷却结晶、过滤、洗涤等。

(1)为了提高“酸浸”效率,可采取的措施有
(2)写出“除铜”时发生复分解反应的化学方程式:
(3)“除铁”加入H2O2溶液的目的是
(4)检验“沉镍”过程中Ni2+已完全沉淀的方法是(含实验操作及实验现象):
(5)“系列操作”主要包括硫酸溶解、
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】酸、碱、盐是重要的物质,在生产和生活中有广泛的用途。
(1)分别将装有相同质量的浓盐酸和浓硫酸烧杯在空气中放置一段时间后,溶液发生的变化是_______ (填序号)。
a.质量均增大 b.质量均减小
c.溶质质量分数均变大 d.溶质质量分数均变小
(2)实验室用氢氧化钙溶液、稀盐酸和碳酸钠溶液进行实验探究。

①甲实验中,事先要在氢氧化钙溶液中加几滴酚酞溶液,目的是什么_______ ?
②测得乙实验过程中溶液pH的变化如图丙所示。曲线ab段说明实验甲中过量的物质是_______ ;曲线bc段反应的化学方程式为_______ ;cd段pH增大的原因是什么_______ ?
(3)硫酸铜是化学实验中常用的试剂。
①将硫酸铜固体加热到650℃时,硫酸铜固体开始发生分解反应,生成氧化铜和另一种氧化物X,则X的化学式为_______ 。
②探究铁、铜的金属活动性顺序时,可将铁钉浸入到硫酸铜溶液中,观察到_______ ,说明铜的金属活动性比铁弱。
③向20g硫酸铜溶液中加入足量氯化钡溶液,将反应产生的沉淀过滤、洗涤、干燥后称量,沉淀的质量为4.66g,试计算该硫酸铜溶液的溶质质量分数_______ 。
(1)分别将装有相同质量的浓盐酸和浓硫酸烧杯在空气中放置一段时间后,溶液发生的变化是
a.质量均增大 b.质量均减小
c.溶质质量分数均变大 d.溶质质量分数均变小
(2)实验室用氢氧化钙溶液、稀盐酸和碳酸钠溶液进行实验探究。

①甲实验中,事先要在氢氧化钙溶液中加几滴酚酞溶液,目的是什么
②测得乙实验过程中溶液pH的变化如图丙所示。曲线ab段说明实验甲中过量的物质是
(3)硫酸铜是化学实验中常用的试剂。
①将硫酸铜固体加热到650℃时,硫酸铜固体开始发生分解反应,生成氧化铜和另一种氧化物X,则X的化学式为
②探究铁、铜的金属活动性顺序时,可将铁钉浸入到硫酸铜溶液中,观察到
③向20g硫酸铜溶液中加入足量氯化钡溶液,将反应产生的沉淀过滤、洗涤、干燥后称量,沉淀的质量为4.66g,试计算该硫酸铜溶液的溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】氯化铁(FeCl3)溶液对过氧化氢的分解有催化作用。取如图所示的过氧化氢溶液34g倒入小烧杯中,向其中加入10%的氯化铁溶液6.8g,使过氯化氢完全分解。完成下列分析及计算:

(1)东东根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为: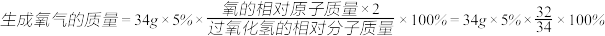 ,老师指出东东的计算是错误的,你认为错误的原因是
,老师指出东东的计算是错误的,你认为错误的原因是_________________ (填字母序号)。
A过氧化氢的相对分子质量计算有误
B过氧化氢中的氧元素没有全部转移到氧气中
(2)请你根据化学方程式计算制取氧气的质量________。
(3)反应后所得氯化铁溶液中溶质的质量分数________。(写出计算过程)

(1)东东根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为:
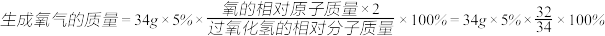 ,老师指出东东的计算是错误的,你认为错误的原因是
,老师指出东东的计算是错误的,你认为错误的原因是A过氧化氢的相对分子质量计算有误
B过氧化氢中的氧元素没有全部转移到氧气中
(2)请你根据化学方程式计算制取氧气的质量________。
(3)反应后所得氯化铁溶液中溶质的质量分数________。(写出计算过程)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】碱是初中化学学习的一类重要物质,氢氧化钠和氢氧化钙是两种常见的碱。
Ⅰ、碱的结构
(1)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在水溶液中都能解离出______(填字母)。
Ⅱ、碱的性质______ (填“氢氧化钠溶液”或“稀盐酸”)滴加到另一种溶液中;a点溶液中所含的溶质为______ 。
(3)如图2分别将二氧化碳气体通入氢氧化钙溶液和氢氧化钠溶液中。
①观察到试管 A 中溶液变浑浊,证明二氧化碳能与氢氧化钙溶液反应,写出反应的化学方程式;______ 。
②试管B 中未观察到明显现象,甲同学提出向反应后的溶液中滴加无色酚酞溶液,观察到溶液由无色变为______ 色,则证明二氧化碳能与氢氧化钠溶液反应,乙同学认为上述实验方案不合理。请设计实验方案证明两者能发生反应______ 。(简述实验操作和现象)
Ⅲ、碱的用途
(4)请简述氢氧化钙在生产或生活中的一种用途______ 。
(5)某工厂化验室用稀硫酸处理含氢氧化钠的废水。现取废水样品100g倒入烧杯中,然后逐滴加入9.8%的稀硫酸,恰好完全反应时,共消耗稀硫酸的质量为20g,求废水中氢氧化钠的质量分数。
Ⅰ、碱的结构
(1)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在水溶液中都能解离出______(填字母)。
| A.氢原子 | B.氢离子 | C.氢氧根离子 | D.水分子 |
Ⅱ、碱的性质

(3)如图2分别将二氧化碳气体通入氢氧化钙溶液和氢氧化钠溶液中。
①观察到试管 A 中溶液变浑浊,证明二氧化碳能与氢氧化钙溶液反应,写出反应的化学方程式;
②试管B 中未观察到明显现象,甲同学提出向反应后的溶液中滴加无色酚酞溶液,观察到溶液由无色变为
Ⅲ、碱的用途
(4)请简述氢氧化钙在生产或生活中的一种用途
(5)某工厂化验室用稀硫酸处理含氢氧化钠的废水。现取废水样品100g倒入烧杯中,然后逐滴加入9.8%的稀硫酸,恰好完全反应时,共消耗稀硫酸的质量为20g,求废水中氢氧化钠的质量分数。
您最近一年使用:0次
【推荐1】某校同学就九年级化学课本上的相关实验开展研究性学习。
I、实验活动:溶液酸碱性的检验。
(1)同学们在校园里取少量土壤样品,将土壤样品与蒸馏水按1:5的质量比在烧杯中混合,充分搅拌后静置,用pH试纸测澄清液体的酸碱度。具体操作是______ ,由此得出,该土样pH>7,呈______ (填“酸性”或“碱性”)。
(2)同学们经查阅资料获知:校园内土壤的酸碱度可能受城市建筑石灰性充填物的影响。据《本草图经》中记载:“石灰,今所在近山处皆有之,①此烧青石为灰也。…②以水沃之,则热蒸而解,力差劣。”文中的“青石”又名石灰石。请分别写出文中所述转化①和转化②的化学方程式:①______ ②______ 。
II、课外实验:自制汽水。
下图是家庭自制汽水的操作,请回答下列问题:

(3)从气体溶解度的角度解释:步骤②中使用凉开水制汽水的原因:______ 。
(4)为证明柠檬酸溶液中有H+,可选用下列物质中的______(填字母)进行验证。
I、实验活动:溶液酸碱性的检验。
(1)同学们在校园里取少量土壤样品,将土壤样品与蒸馏水按1:5的质量比在烧杯中混合,充分搅拌后静置,用pH试纸测澄清液体的酸碱度。具体操作是
(2)同学们经查阅资料获知:校园内土壤的酸碱度可能受城市建筑石灰性充填物的影响。据《本草图经》中记载:“石灰,今所在近山处皆有之,①此烧青石为灰也。…②以水沃之,则热蒸而解,力差劣。”文中的“青石”又名石灰石。请分别写出文中所述转化①和转化②的化学方程式:①
II、课外实验:自制汽水。
下图是家庭自制汽水的操作,请回答下列问题:

(3)从气体溶解度的角度解释:步骤②中使用凉开水制汽水的原因:
(4)为证明柠檬酸溶液中有H+,可选用下列物质中的______(填字母)进行验证。
| A.酚酞溶液 |
| B.镁条 |
| C.铜片 |
| D.鸡蛋壳 |
| E.二氧化碳 |
| F.食盐 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】构建思维导图是一种重要的学习方法。请根据酸和碱的化学性质思维导图,回答下列问题。(“—”表示相连的两类物质之间可以发生反应)

(1)图中甲表示的物质类别是________ ,写出关系“甲—酸”对应的一条用途_________ 。
(2)酸与碱作用生成盐和水叫做中和反应,可溶性碱溶液与酸反应时无明显现象,需要加入__________ 溶液证明酸和碱之间发生了化学反应或反应完成。
(3)利用图中“碱—非金属氧化物”反应可用氢氧化钠溶液吸收废气中的 。
(4)工业上用纯碱制取烧碱的反应应用的是图中盐和_______ (填物质类别)的反应关系。
(5)农业上用波尔多液杀虫,波尔多液配置过程是将熟石灰和硫酸铜溶液混合,制得悬浊液附着在叶片背面杀死虫卵,用化学方程式解释反应过程:________ 。
(6)图中涉及到的复分解反应有______ 种。

(1)图中甲表示的物质类别是
(2)酸与碱作用生成盐和水叫做中和反应,可溶性碱溶液与酸反应时无明显现象,需要加入
(3)利用图中“碱—非金属氧化物”反应可用氢氧化钠溶液吸收废气中的 。
| A.CO | B.CO2 | C.SO2 | D.N2 |
(5)农业上用波尔多液杀虫,波尔多液配置过程是将熟石灰和硫酸铜溶液混合,制得悬浊液附着在叶片背面杀死虫卵,用化学方程式解释反应过程:
(6)图中涉及到的复分解反应有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】盐酸是一-种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强, HCl由气态变为液态,从微观的角度分析该变化过程中改变的是_____ 。
(2)金属钴(Co)在国防工业中有重要应用。钴的化学性质与铁相似,与酸反应生成+2价的钻盐,CoCl2 溶液为红色。在盐酸中加入过量的钴粉充分反应。
①预测上述反应发生的现象:_____ 。
②如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):


_____ 、
_____ 、
_____ 。
(3)乙醇易燃烧,如图为乙醇(C2H5OH)在空气中完全燃烧时的微观示意图:

①乙框中含有_____ 种分子,其中属于氧化物的是 _____ 。(填化学式)
②甲、乙两个方框中的微观粒子均不完整,请将图中甲、乙两个方框中微观粒子的种类和数目补充完整_____ 。
(1)增大压强, HCl由气态变为液态,从微观的角度分析该变化过程中改变的是
(2)金属钴(Co)在国防工业中有重要应用。钴的化学性质与铁相似,与酸反应生成+2价的钻盐,CoCl2 溶液为红色。在盐酸中加入过量的钴粉充分反应。
①预测上述反应发生的现象:
②如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):




(3)乙醇易燃烧,如图为乙醇(C2H5OH)在空气中完全燃烧时的微观示意图:

①乙框中含有
②甲、乙两个方框中的微观粒子均不完整,请将图中甲、乙两个方框中微观粒子的种类和数目补充完整
您最近一年使用:0次
【推荐1】2022年北京冬奥会是一届绿色奥运、科技奥运、人文奥运,北京冬奥惊艳世界!_______ 。
(2)吉祥物“冰墩墩”表面材料为羊毛,内充PET(聚酯塑料)。羊毛属于_______ (填“天然纤维”或“合成材料”)。
(3)奥运场馆建设中使用国产高钒密闭索,钒可提高钢材的机械性能。有关钒元素的信息如图:x=_______ ,钒原子失去2个电子后形成的钒离子为_______ (填离子符号)。
火炬采用氢气作燃料,体现绿色办奥的理念,氢气燃料实现“零排放”的原因是_______ (用化学方程式表示),关闭火炬的燃气开关,使火炬熄灭,采用的灭火原理是_______ 。
(5)北京冬奥会恰逢中国农历春节,菜单突出“中国年味”
早餐中的清水牛肉,清淡而富有营养,牛肉为运动员提供的营养素主要是_______ 。

(2)吉祥物“冰墩墩”表面材料为羊毛,内充PET(聚酯塑料)。羊毛属于
(3)奥运场馆建设中使用国产高钒密闭索,钒可提高钢材的机械性能。有关钒元素的信息如图:x=


火炬采用氢气作燃料,体现绿色办奥的理念,氢气燃料实现“零排放”的原因是
(5)北京冬奥会恰逢中国农历春节,菜单突出“中国年味”
早餐中的清水牛肉,清淡而富有营养,牛肉为运动员提供的营养素主要是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】2019 年 12 月 17 日,“山东舰”在海南三亚某军港交付使用,“山东舰”是中国真正意义上的第一艘国产航空母舰。在“航母”的建造过程中,使用了大量的金属材料、无机非金属材料和有机高分子材料等,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金,它能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮氢合金从物质分类上属于______ 物。钢铁是制造轮船船身的主要金属材料,船身外通常按装一定数目比铁更活泼的金属块以防止船身被腐蚀,该活泼金属块可以选择下列各项中的______ (填下列各项序号字母)。
A.铜块 B.锌块 C.铅块 D.银块
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,反应的化学方程式为______ ,其基本反应类型为______ 。
②实验室常采用______ 操作进行沉淀分离,说出该原理在生活中的一种应用______ 。
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是______ 。
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______ (用化学方程式表示)。
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少______ 污染。20 世纪 30 年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______ 方法区分尼龙和蚕丝。
(1)金属材料中,有一类贮氢合金,它能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮氢合金从物质分类上属于
A.铜块 B.锌块 C.铅块 D.银块
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,反应的化学方程式为
②实验室常采用
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐3】义务教育均衡县的创建,让济南市的农村中小学都有了和城里学校一样的设施和条件。 所有农村中小学都建起了塑胶操场,极大改善了办学条件。一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(分子式C15 H10N2O2)。而不合格的材料中因含有大量甲醛(分子式HCHO)被禁止使用。

①二甲苯烷二异氰酸酯(C15 H10N2O2)属于__________________ (填“有机物”“无机物”)。
②二甲苯烷二异氰酸酯分子中氢、氧原子的个数比为___________________ (填最简整数比)。
③500g二甲苯烷二异氰酸酯中含氮元素的质量为___________________ g。
④化工原料甲醛(HCHO)是一种有刺激性气味的气体,易溶于水,这些属于甲醛的__________________ 性质(填“物理”或“化学”)。
⑤甲醛被世界卫生组织确定为致癌和致畸形物质。有关甲醛说法中正确的是_________________ (填序号) .
A 甲醛可作食品防腐剂
B 甲醛是营养物质
C 甲醛是调味品
D 甲醛能使人体蛋白质失去生理活性

①二甲苯烷二异氰酸酯(C15 H10N2O2)属于
②二甲苯烷二异氰酸酯分子中氢、氧原子的个数比为
③500g二甲苯烷二异氰酸酯中含氮元素的质量为
④化工原料甲醛(HCHO)是一种有刺激性气味的气体,易溶于水,这些属于甲醛的
⑤甲醛被世界卫生组织确定为致癌和致畸形物质。有关甲醛说法中正确的是
A 甲醛可作食品防腐剂
B 甲醛是营养物质
C 甲醛是调味品
D 甲醛能使人体蛋白质失去生理活性
您最近一年使用:0次



