向盛有一定质量氧化钙和碳酸钙混合物的烧杯中加入142g稀盐酸,恰好完全反应,一定温度下,得到153.2g不饱和溶液。则该不饱和溶液的溶质质量分数是(结果保留一位小数)___________ 。
更新时间:2023-04-04 21:00:04
|
相似题推荐
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐1】某化学社团在实验室探究工业废水的综合利用,他们设计了以下流程从废水中回收铜和硫酸锌。
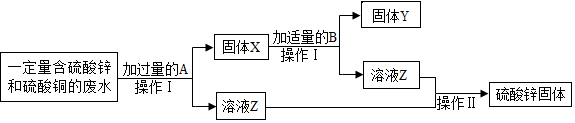
(1)操作I的名称是______ 。
(2)上述流程中,物质A可能是______ (写化学式)。
(3)操作I和操作Ⅱ中均使用到的玻璃仪器是______ 。
(4)若加入的物质B为稀硫酸,用量为100g,在此过程中恰好完全反应生成气体0.4g,则所用稀硫酸中溶质的质量分数为______ 。

(1)操作I的名称是
(2)上述流程中,物质A可能是
(3)操作I和操作Ⅱ中均使用到的玻璃仪器是
(4)若加入的物质B为稀硫酸,用量为100g,在此过程中恰好完全反应生成气体0.4g,则所用稀硫酸中溶质的质量分数为
您最近一年使用:0次
【推荐2】回答问题
(1)现有Mg和MgO的固体混合物3g,经测定镁元素的质量分数为80%,向固体混合物中加入100g一定溶质质量分数的稀盐酸,恰好完全反应,则混合物中镁的质量为_______ g,反应后溶液中的MgCl2的质量为_______ g,所用稀盐酸中溶质的质量分数为_______ 。
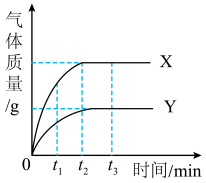
(2)已知活泼金属可以与稀酸反应。等质量的X、Y两种金属分别和足量的同体积、同浓度的稀盐酸反应,产生气体的质量与时间的关系如图所示,下列说法中不正确的是_______。
(1)现有Mg和MgO的固体混合物3g,经测定镁元素的质量分数为80%,向固体混合物中加入100g一定溶质质量分数的稀盐酸,恰好完全反应,则混合物中镁的质量为
(2)已知活泼金属可以与稀酸反应。等质量的X、Y两种金属分别和足量的同体积、同浓度的稀盐酸反应,产生气体的质量与时间的关系如图所示,下列说法中不正确的是_______。

| A.t1时,产生气体的质量:X>Y | B.t2时,消耗金属的质量:X>Y |
| C.t3时,消耗金属的质量:X=Y | D.t3时,消耗盐酸的质量:X=Y |
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐1】将7.3%的稀盐酸逐滴加入50g滴有少量酚酞的NaOH溶液中,溶液的pH和加入稀盐酸的质量关系如图。
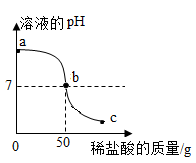
a点处溶液呈_____ 色,滴加稀盐酸后,酸与碱发生_____ 反应,溶液的pH不断_____ ,b点表示_____ ,此处溶液的pH_____ 7,至c点处时,溶液中的溶质为_____ ,原NaOH溶液的质量分数为_____ 。

a点处溶液呈
您最近一年使用:0次
【推荐2】铁是当今社会应用最广泛的金属。
(1)如图是铁在元素周期表中的相关信息及铁原子结构示意图,下列说法错误的是
(2)生产生活中的铁制品大多由铁合金制成。合金属于________ (填“合成材料”或“金属材料”);作为铁的一种合金,生铁可用于制作铁锅,利用的是铁具有良好的________ 性。
(3)工业上通过冶炼铁矿石获取铁。某同学利用下图装置在实验室模拟炼铁。________ 。
②从环保角度考虑,请写出一种尾气处理方法________ 。
③为检验B 装置中是否还有 NaOH,该同学取B 中溶液样品,加入足量的Ca(OH)2溶液,充分反应后,向上层清液滴加无色酚酞溶液进行检验。请找出该方案不合理之处并说明理由________ 。
(4)铁制品一旦锈蚀,需及时除锈。工业上常用稀硫酸除铁锈(Fe2O3), 该反应的化学方程式为_______________
(5)废弃铁制品还可以回收利用。某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现溶质质量分数为20%的废硫酸19.6t,与足量的废铁屑反应,可生产硫酸亚铁的质量是多少?
(1)如图是铁在元素周期表中的相关信息及铁原子结构示意图,下列说法错误的是
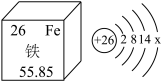
| A.铁原子的核电荷数为26 | B.铁的相对原子质量为55.85g |
| C.x=2 | D.铁位于元素周期表第四周期 |
(2)生产生活中的铁制品大多由铁合金制成。合金属于
(3)工业上通过冶炼铁矿石获取铁。某同学利用下图装置在实验室模拟炼铁。
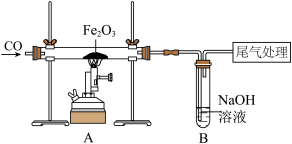
②从环保角度考虑,请写出一种尾气处理方法
③为检验B 装置中是否还有 NaOH,该同学取B 中溶液样品,加入足量的Ca(OH)2溶液,充分反应后,向上层清液滴加无色酚酞溶液进行检验。请找出该方案不合理之处并说明理由
(4)铁制品一旦锈蚀,需及时除锈。工业上常用稀硫酸除铁锈(Fe2O3), 该反应的化学方程式为
(5)废弃铁制品还可以回收利用。某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现溶质质量分数为20%的废硫酸19.6t,与足量的废铁屑反应,可生产硫酸亚铁的质量是多少?
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】学习和生活离不开化学知识。试回答下列问题。
(1)考试涂卡使用2B铅笔,铅笔芯的主要成分是______ ,中考填报志愿要求使用碳素墨水,原因是_________ 。
(2)新装修的房子甲醛超标、水中有异色异味,均可利用________ 的吸附性去除。
(3)生活中经常需要做一些清洗工作,如利用洗洁精的_______ 作用洗涤餐具;炉具清洁剂中__________ 能与油脂发生反应,烧水壶内的水垢可用厨房中的_______ 除去。
(1)考试涂卡使用2B铅笔,铅笔芯的主要成分是
(2)新装修的房子甲醛超标、水中有异色异味,均可利用
(3)生活中经常需要做一些清洗工作,如利用洗洁精的
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐2】某铝冶炼厂为了“变废为宝,点渣成金”,从含有Al2O3、SiO2等成分的工业废渣中提取金属铝,其工艺流程如下:
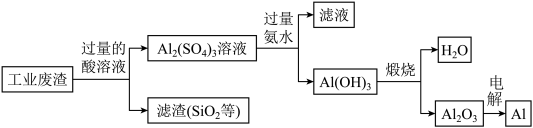
回答下列问题:
(1)流程图中含铝元素的物质中属于碱的是___________ 。
(2)“过量的酸溶液”中使用的酸是___________ (填字母序号)。
(3)电解A12O3生成两种单质,该反应的基本反应类型是___________ 反应。

回答下列问题:
(1)流程图中含铝元素的物质中属于碱的是
(2)“过量的酸溶液”中使用的酸是___________ (填字母序号)。
| A.醋酸(CH3COOH) | B.HNO3 | C.H2SO4 |
(3)电解A12O3生成两种单质,该反应的基本反应类型是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】化学服务生活、保障健康
(1)化学与健康生活
①人体部分体液的pH如图所示,图中呈酸性的体液是______ 。
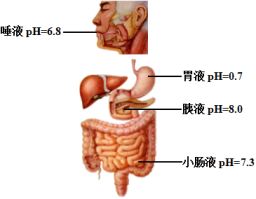
②某病人使用小苏打治疗胃酸(主要成分是盐酸)过多,其原理是______ (用化学方程式表示)
③国家推广是用加碘食盐,目的是______
(2)化学与便捷生活
①“自热火锅”中的发热包(主要成分含生石灰),加水后会释放出大量的热,原因是______ (用化学方程式表示)
②大雪后,向积雪的路面抛洒融雪剂能加快冰雪消融,原因是______
③生活中,要点购买的双氧水加砖红色粉末可迅速制氧,其原理是______ (用化学方程式表示)
(3)化学与环保生活
①工业炼铁的“高炉气体”中含N2、CO2、CO、SO2等,其中会引起酸雨的是______ ,可利用熟石灰吸收;尾气中CO通过燃烧法去除的原理是______ (用化学方程式表示)。
②目前众多餐饮行业用“纸质吸管”和“聚乳酸吸管”代替一次性塑料吸管,此举的目的是______ 。
(1)化学与健康生活
①人体部分体液的pH如图所示,图中呈酸性的体液是

②某病人使用小苏打治疗胃酸(主要成分是盐酸)过多,其原理是
③国家推广是用加碘食盐,目的是
(2)化学与便捷生活
①“自热火锅”中的发热包(主要成分含生石灰),加水后会释放出大量的热,原因是
②大雪后,向积雪的路面抛洒融雪剂能加快冰雪消融,原因是
③生活中,要点购买的双氧水加砖红色粉末可迅速制氧,其原理是
(3)化学与环保生活
①工业炼铁的“高炉气体”中含N2、CO2、CO、SO2等,其中会引起酸雨的是
②目前众多餐饮行业用“纸质吸管”和“聚乳酸吸管”代替一次性塑料吸管,此举的目的是
您最近一年使用:0次



