某化学兴趣小组测定黄铜(铜锌合金)的组成,称取30g黄铜置于烧杯中,用100g稀硫酸分5次加入,实验数据记录如下:
试分析并计算:
(1)实验数据表中m的值为______ 。
(2)计算恰好完全反应时所得溶液的溶质质量分数。(精确到0.1%)
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
残留金属的质量/g | 26.75 | m | 20.25 | 17 | 17 |
(1)实验数据表中m的值为
(2)计算恰好完全反应时所得溶液的溶质质量分数。(精确到0.1%)
2023·山东滨州·一模 查看更多[3]
更新时间:2023-04-22 14:45:14
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将铁粉和铜粉的混合物14 g,加入到盛有116.2 g稀盐酸的烧杯中,恰好完全反应。此时烧杯内各物质的总质量为129.8 g。试回答:
(1)写出铁与稀盐酸反应方程式_____ 。
(2)计算原混合物中铁粉的质量分数。
(3)计算反应后所得溶液中溶质的质量分数。
(1)写出铁与稀盐酸反应方程式
(2)计算原混合物中铁粉的质量分数。
(3)计算反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】小华有一只银手镯(银锌合金),她想用实验探究手镯中银的含量。先用电子秤称得手镯的质量是25.00克,再用稀盐酸分多次与此手镯充分反应。实验数据如下表:
根据上表中数据分析,完成下列问题:
(1)手镯中银的质量是______ 克。
(2)第四次实验结束后,溶液里溶质为______ (填化学式)。
(3)求所用稀盐酸中溶质的质量分数是多少?
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量(克) | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
| 充分反应后剩余固体的质量(克) | 24.35 | 23.70 | 23.05 | 23.00 | 23.00 |
(1)手镯中银的质量是
(2)第四次实验结束后,溶液里溶质为
(3)求所用稀盐酸中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某同学为了测定不纯的锌片中锌的含量,取不同质量的锌片依次放入盛有稀硫酸的烧杯中,反应完全后称出质量(杂质不参加反应,也不溶于水)。实验结果记录如下:
(1)将第2次和第5次实验后烧杯中剩余物质的总质量填在上表中。
(2)求该实验中所用锌片中锌的质量分数。
| 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入锌质量(g) | 20 | 40 | 60 | 80 | 100 | 120 |
| 稀硫酸的质量(g) | 200 | 200 | 200 | 200 | 200 | 200 |
| 烧杯中物质的总质量(g) | 219.6 | ______ | 258.8 | 278.4 | _______ | 318.4 |
(1)将第2次和第5次实验后烧杯中剩余物质的总质量填在上表中。
(2)求该实验中所用锌片中锌的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室中有一瓶标签破损的盐酸标签如图所示,某化学兴趣小组取黄铜样品粉末(假设样品中除两种主要成分外,无其他物质),做了如图所示实验:
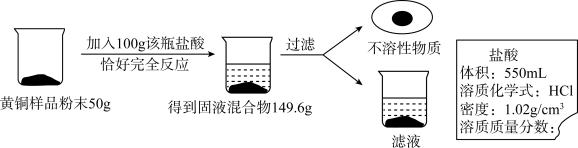
(1)若用瓶内盐酸配制成溶质质量分数为3.65%的稀盐酸100g,则需取瓶内盐酸的质量为______。
(2)过滤后得到的滤液为不饱和溶液,向其中加入87.4g水,求最终所得溶液中溶质的质量分数。

(1)若用瓶内盐酸配制成溶质质量分数为3.65%的稀盐酸100g,则需取瓶内盐酸的质量为______。
(2)过滤后得到的滤液为不饱和溶液,向其中加入87.4g水,求最终所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
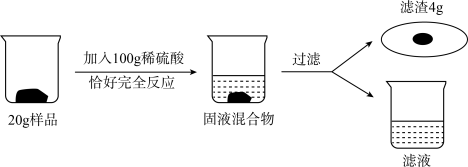
【推荐2】为测定某样品中锌的质量(样品中的其他物质既不与酸反应也不溶于水),某化学小组同学进行了如下图所示实验。请根据图中提供的数据进行计算:

(1)样品中锌的质量为______ g。
(2)计算实验结束后所得溶液的溶质质量分数。(计算结果精确到0.1%)

(1)样品中锌的质量为
(2)计算实验结束后所得溶液的溶质质量分数。(计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将20g赤铁矿样品加入100g稀硫酸中(杂质不溶于水,也不与酸反应,杂质中不含铁元素),恰好完全反应,实验过程测得数据如下,请回答问题:
(1)写出发生反应的化学方程式______ 。
(2)根据已知条件列出求解参加反应的稀硫酸中溶质质量(x)的比例式______ 。
(3)向反应后所得滤液中加入84g水,所得溶液溶质质量分数为______ 。
(4)若用质量分数98%的浓硫酸配制实验所用的稀硫酸,则需要浓硫酸与水的质量比为______ 。
(5)若工业上用100t上述赤铁矿炼铁(假设炼制过程中铁矿石的利用率为95%),能炼出含铁95%的生铁的质量为______ t。

(1)写出发生反应的化学方程式
(2)根据已知条件列出求解参加反应的稀硫酸中溶质质量(x)的比例式
(3)向反应后所得滤液中加入84g水,所得溶液溶质质量分数为
(4)若用质量分数98%的浓硫酸配制实验所用的稀硫酸,则需要浓硫酸与水的质量比为
(5)若工业上用100t上述赤铁矿炼铁(假设炼制过程中铁矿石的利用率为95%),能炼出含铁95%的生铁的质量为
您最近一年使用:0次



