实验小组同学对维C泡腾片非常感兴趣。把一颗维C泡腾片药片丢入水中,发现药片表面产生大量的气泡。
【查阅资料】维C泡腾片是一种较新的药物剂型,主要成分有:维生素C(C4H6O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7)等。
维生素C主要增强机体抵抗力,用于预防和治疗坏血病。温度超过80℃被破坏。
探究1:维C泡腾片水溶液酸碱性
【进行实验一】
(1)取1mL溶液于试管中,滴加2滴紫色石蕊溶液,发现溶液变红,说明泡腾片与水发生反应后,溶液显
探究2:反应产生的气体是什么?
【提出猜想】该气体可能是CO2、CO、O2、H2和N2中的一种或几种
(2)小明认真思考后认为:从药品安全角度考虑,排除了CO和H2;从元素守恒角度考虑,产生的气体也不可能是N2,因为
【进行实验二】
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验① | 操作1 | 澄清石灰水变浑浊 | 气体中含有CO2 |
实验② |
| 带火星的木条不燃烧 | 气体中不含有O2 |
(3)补全实验报告:操作1
(4)实验②中足量的氢氧化钠溶液是为了排除干扰,发生反应的化学方程式为
探究3:温度、泡腾片的形状对产生气体速率的影响
【进行实验三】将泡腾片与50mL水混合,利用压强传感器测量从0s至60s时增大的压强值。
实验序号 | 泡腾片的数目 | 泡腾片的形状 | 温度/℃ | 60s时增大的压强值/kPa |
① | 4 | 每颗切成4等份 | 25 | 10.67 |
② | 4 | 每颗切成4等份 | 37 | 18.75 |
③ | 4 | 每颗研碎成粉末 | 37 | 23.58 |
④ | 6 | 每颗切成4等份 | 25 | 13.86 |
⑤ | 6 | 每颗研碎成粉末 | x | 20.57 |
⑥ | 6 | 每颗研碎成粉末 | 37 | 25.46 |
【解释与结论】
(5)探究泡腾片形状会影响产生气体的速率的实验是
(6)通过对比实验①、②或⑤、⑥,得出的结论是
【结论与反思】
(7)通过实验,你对维C泡腾片的保存或使用注意事项等提出一项建议
相似题推荐
Ⅰ.不稳定性
(1)如下图所示进行实验,受热分解的化学方程式为,3.16g KMnO4产生O2的质量为
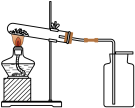
(2)用向上排空气法收集O2的原因是
Ⅱ.腐蚀性
【查阅资料】KMnO4 溶液呈中性、有腐蚀性
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表
| KMnO4 溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
| 鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
实验2:将铜片分别浸泡在4种浸泡相同时间,现象如下表。
| 编号 | ① | ② | ③ | ④ | |
| 实验 |  25mL0.1%KMnO4溶液 |  25mL0.1%KMnO4溶液+10滴浓硫酸 |  25mL蒸馏水+10滴浓硫酸 |  25mL1%KMnO4溶液+10滴浓硫酸 | |
| 铜片质量/g | 实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
| 18小时后 | 0.54 | 0.52 | 0.54 | 0.43 | |
【解释与结论】
(3)实验1的目的是
(4)实验2中通过对比②和④,得出的结论是
(5)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比
(6)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。
5Cu+2KMnO4+8H2SO4=5CuSO4+2MnSO4+K2SO4+
实验发现,收集到的O2大于理论产量,针对这一现象进行了如下探究:
【提出猜想】猜想1:反应生成的MnO2分解放出O2;猜想Ⅱ:反应生成的K2MnO4分解放出O2。他们做出上述猜想的理由是
【实验验证】同学们分为两组,分别进行了以下实验:
(1)一组同学取少量的MnO2,在250℃条件下加热,冷却后测得MnO2的质量不变。则猜想I错误。
(2)二组同学取少量的K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论。他们的实验方法是
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识?
【提出问题】一定质量的蔗糖在一定质量的氧气中生成什么气体?
【猜想与假设】猜想①H2O、CO2;猜想②CO、H2O、CO2;猜想③
【查阅资料】无色硫酸铜遇水变蓝色。
【实验探究】将一定质量蔗糖在一定质量的氧气中点燃,反应后将燃烧的产物依次通过装置A、B、C、D、E(夹持仪器省略)。

【实验记录】A装置无水硫酸铜变蓝色,B、D装置中澄清石灰水变浑浊,C装置中黑色固体变红色。
【实验结论】猜想
【反思评价】(1)实验时,先将氮气通入实验装置一段时间,再通入燃烧产物,加热,先通入氮气的目的是
(2)C装置中发生的化学方程式为
【实验拓展】(1)蔗糖富含营养素是
(2)氧气的质量不同,蔗糖燃烧的产物不同。34.2g蔗糖(C22H22O11)燃烧,生成物的质量为m,则m的取值范围为

①A 中的现象是
②反应结束后,将 D、E 中的废液倒入同一个洁净的烧杯中,观察到先有气泡产生,后有白 色沉淀生成。过滤,得到白色沉淀和无色滤液。该同学欲探究无色滤液中的溶质。
【分析】无色滤液中一定不含 HCl,理由
【提出问题】无色滤液中的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl和Na2CO3;④NaCl、CaCl2和Na2CO3。 你认为猜想
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想 |
| 取少量滤液于试管中,滴加少量 | 有气泡产生 |
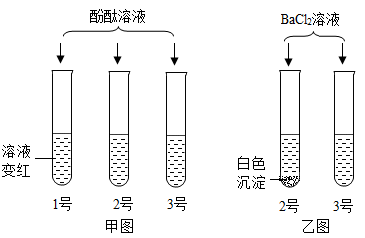
(1)1号试管中是
(2)乙图中2号试管内发生反应的化学方程式为
把该2号试管反应后的物质进行过滤。再将滤液和3号试管内的液体同时倒入烧杯内混合,过滤后得到白色沉淀和无色滤液。
【提出问题】除含有酚酞外,无色滤液中溶质的成分是什么?
【猜想假设】猜想一:HCl、NaCl;
猜想二:HCl、NaCl和
猜想三:HCl、NaCl和BaCl2。
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加适量的 | 产生白色沉淀 | 猜想二正确 |
【交流拓展】张茗同学为了测定3号试管内溶液的酸碱性,将一片pH试纸放在干燥的玻璃片上,用玻璃棒蘸取该滤液,滴到试纸上,立即将试纸显示的颜色与标准比色卡进行对照,读出pH=5。要将该溶液调至中性,可向溶液中加入足量的
A.铁粉 B.氯化钙溶液 C.石灰石
[提出问题]氢氧化钠溶液与稀盐酸是否发生化学反应?
[查阅资料] 酸与碱发生中和反应会放出热量。
[实验设计] 甲、乙、丙三位同学分别设计了实验方案,请你帮他们完成实验报告。
| 同学 | 实验操作 | 现象 |
| 甲 | 将稀盐酸慢慢滴入加有酚酞的NaOH 溶液中,并不断搅拌 | 溶液颜色的变化是 |
| 乙 |  | U型玻璃管中 |
| 丙 | 用pH传感器测量反应过程中溶液pH值的变化情况 。  | 实验过程中, 不断搅拌得到的烧杯中溶液PH值变化曲线。 |
[结论]氢氧化钠与稀盐酸发生了化学反应。
(1) 氢氧化钠与盐酸反应的化学方程式为
(2) 丙同学实验中,根据pH曲线判断,当加入A溶液
(3)丙同学实验中,当加入l6g A溶液时,烧杯中溶液的溶质是
[反思]后来,同学们一致认为乙方案不够合理,理由是


(1)通过分析实验一可知,氢氧化钠会吸收空气中的
(2)实验二中观察到3个塑料瓶变瘪的程度为A>B>C,可证明CO2能与NaOH、Ca(OH)2反应,其中C瓶在实验中起
(3)晓晓查阅资料了解到往Ba(OH)2溶液中滴加或通入下列图2中物质会产生如下现象:A中溶液显红色,B、C、D中均产生白色沉淀;
①写出D试管中反应的化学方程式
②不同的碱溶液中都含有OH-,所以,碱有一些相似的化学性质。上述关于Ba(OH)2性质的实验不能体现碱的相似性质的是
(4)冬冬发现工业上使用的氢氧化钠固体标签如图3所示,于是对其所含杂质进行了探究.
【提出问题】
【提出猜想】猜想Ⅰ:查阅资料可知,工业用氢氧化钠可能含有NaCl;
猜想Ⅱ:工业用氢氧化钠可能含有Na2CO3,原因是
【进行实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| 取适量固体样品于试管中,加水溶解 | 固体全部溶解 |  |
| 向所得溶液中滴加过量的 | 一开始无明显变化,一会儿后产生能使澄清石灰水变浑浊的气体 | 样品中含有Na2CO3 |
| 向所得溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有NaCl,反应的化学方程式为 |
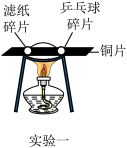
(1)如实验一所示,将同样大小的乒乓球碎片和滤纸碎片放在铜片上同时加热,观察到乒乓球碎片先燃烧起来。由此说明乒乓球碎片的着火点比滤纸碎片的着火点
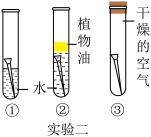
(2)如实验二所示,通过对比
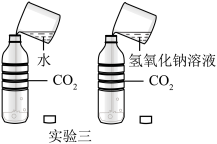
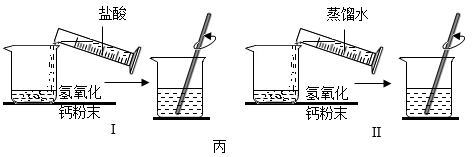
(3)如实验三所示,将等体积的水和氢氧化钠溶液,分别注入两个等容积的装满二氧化碳的同等材质的软塑料瓶中,迅速旋紧瓶盖充分振荡,发现倒入氢氧化钠溶液的软塑料瓶比倒入水的软塑料瓶变得更瘪。由此
(4)化学兴趣小组为了证明氧化铁也是过氧化氢分解的催化剂,设计以下实验方案。请完成下表并回答:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 实验Ⅰ | 取5mL5%的过氧化氢溶液于试管中,再伸入带火星的木条。 | 木条不复燃。 | 氧化铁是过氧化氢分解的催化剂。 |
| 实验Ⅱ | 取5mL5%的过氧化氢溶液于试管中,加入1g氧化铁,再伸入带火星的木条。 |
【拓展】
(5)取50g未知浓度的过氧化氢溶液和1g氧化铁混合制取氧气,充分反应后,称量剩余溶液和滤渣的质量为49.4g。通过计算可知过氧化氢溶液中溶质的质量分数为
已知:高炉气体中一定含有二氧化碳、氮气、极少量的氧气、稀有气体等,还可能含有一氧化碳、二氧化硫等有害气体。
[提出问题]高炉气体中的有害成分是什么?
[作出猜想]猜想一:只有CO; 猜想二:只有 SO2; 猜想三:CO 和SO2都有。
甲实验小组
[查阅资料]SO2与CO2具有许多相似的化学性质:
①都能与水反应。
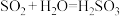 (亚硫酸);
(亚硫酸);②SO2也能使澄清石灰水变浑浊,生成亚硫酸钙(CaSO3)白色沉淀;
③都能与氢氧化钠溶液反应,分别生成可溶性的碳酸钠、亚硫酸钠(Na2SO3)和水。
不同之处:二氧化硫能使红色品红溶液褪色,可被酸性高锰酸钾溶液吸收。
[实验探究]甲组同学设计组装如下装置进行实验。
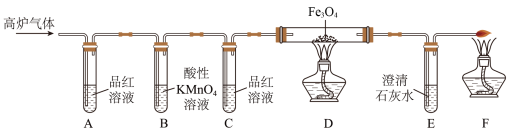
(1)A中品红溶液的作用是检验二氧化硫,B中酸性高锰酸钾溶液的作用是
(2)观察现象发现:A中品红溶液褪色,C中品红溶液不褪色,E中澄清石灰水变浑浊。
得出结论:高炉气体中含有SO2和CO。
反思评价:部分同学认为上述结论不够准确,理由是
[实验改进]同学们经过讨论后,在原有基础上改进了实验装置,如下图所示。
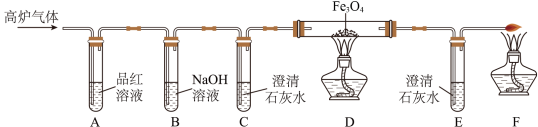
(3)用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是
乙实验小组
[查阅资料]一氧化碳能与红色氯化钯(PdCl2)溶液反应,生成黑色的金属钯(Pd)沉淀、盐酸和二氧化碳。
[实验探究]乙组同学设计如下实验装置并进行实验。
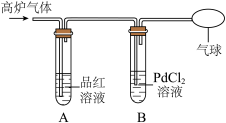
(4)B中反应的化学方程式为
[实验结论]炼铁厂排放的高炉气体中含有CO和SO2,直接排放会造成大气污染,需净化达标后才能排放。
[延伸拓展]二氧化硫排放到空气中会导致酸雨。二氧化硫与水反应生成亚硫酸,亚硫酸会被氧气进一步氧化生成硫酸。
为了研究酸雨的危害,同学们设计了如下实验探究:
②将硫燃烧的产物溶于水后,通入氧气,用所得溶液模拟硫酸型酸雨。
②模拟实验如下:
| 实验序号 | 所加物质 | 实验现象 |
| 1 | 树叶、果皮 | 树叶、果皮被腐蚀 |
| 2 | 细铁丝、镁条 | 产生气泡 |
| 3 | 石灰石、大理石碎片 | 产生气泡 |
实验结论:酸雨具有较强的危害性。
反思评价:
(5)实验室制取二氧化碳时,不能使用大理石与稀硫酸反应,但硫酸型酸雨却能腐蚀大理石雕像,其原因是
(6)同学们经过讨论认为,酸雨还会加剧“温室效应”。这种说法的依据是
I、种植茶树
(1)茶树适宜在pH为5~6的土壤中生长,土壤呈
(2)茶树生长过程中会将环境中的氟元素富集于体内,青少年缺氟易导致
Ⅱ、泡制茶汤
(3)选择茶具:现选用三种不同材质的茶具泡某品牌龙井茶,测量茶汤中风味物质儿茶素类和咖啡碱的含量。测量结果如下:
浸泡时间(min) | 儿茶素类含量(mg/g) | 咖啡碱含量(mg/g) | ||||
紫砂壶 | 瓷质盖碗 | 玻璃杯 | 紫砂壶 | 瓷质盖碗 | 玻璃杯 | |
2 | 155 | 162 | 151 | 25 | 26 | 26 |
4 | 201 | 223 | 214 | 32 | 36 | 35 |
以下属于该实验需控制的变量是
a.水温 b.水量 c.水样 d.煮水方式 e.茶叶用量
结论:不同材质的茶具对茶汤风味虽有一定影响,但差异不大,生活中按需选择即可。
(4)选择水:茶汤的滋味和香气与水的酸碱度和矿化度有较大关系。经研究发现水的pH值越低,茶汤的品质越高:水的矿化度(钙、镁离子含量)越低,茶汤的品质越高。选取三种不同水样测量,结果见下表。三种水祥中最适合泡茶的是
水样 | 虎跑泉水 | 当地自来水 | 某品牌纯净水 |
pH | 5.76 | 6.92 | 6.81 |
矿化度 | 低 | 高 | 低 |
Ⅱ、清洁茶具
长期使用的茶具中易出现茶垢(主要成分为碳酸钙),需定期清理。
(5)除垢原理
牙膏除垢:牙膏中有摩擦剂,利用摩擦作用,达到去污效果。
柠檬酸除垢:柠檬酸溶液能除垢的原因是
茶垢清洁剂除垢:茶垢清洁剂中的过碳酸钠遇热水产生大量气体,分解茶垢。
(6)自制除垢剂
①现有50g质量分数为40%的柠檬酸溶液,将其稀释为除垢所需的质量分数为10%的柠檬酸溶液,需加水
②用碳酸钠和30%的过氧化氢溶液为主要原料制备过碳酸钠(2Na2CO3·3H2O2),理论上碳酸钠与过氧化氢溶液投料的质量比为
实验一 探究H2O2质量分数、溶液pH、温度对反应速率的影响
(1)实验室用过氧化氢溶液制氧气的化学方程式为
(2)设计如下表实验方案
| 实验序号 | H2O2质量分数/% | pH | 温度/℃ | 每分钟气泡数 |
| 1 | 30 | 5 | 20 | |
| 2 | 30 | 6 | 20 | |
| 3 | 30 | 11 | 20 | |
| 4 | 15 | 11 | 30 | |
| 5 | a | 11 | b |
①实验1~3的实验目的是
②a=
实验二 探究制取氧气的适宜催化剂
(3)实验方案如下:
Ⅰ.MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用如图装置进行实验。改用其他三种微球,分别重复上述实验,得到如图的锥形瓶内压强随时间变化的曲线图。

①每次实验时,海藻酸钠微球数应相同的原因
②含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因可能是
③从实验曲线看,催化效果较好、反应温和的催化剂是
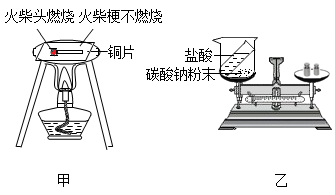
(1)实验甲发现火柴头燃烧了,火柴梗没燃烧,说明可燃物燃烧的条件之一是
(2)实验乙:观察到反应后天平不平衡,原因是
(3)为了验证盐酸与氢氧化钙之间是否反应我们做了实验丙。你认为要得到可靠的实验结论,需要保证实验Ⅰ、Ⅱ中




