氢能作为一种清洁、可再生能源受到越来越多的关注。氢能产业包含氢气的制备、储存、运输和应用等多个环节。

I.制备“氢气”:
(1)利用太阳能将水转化为氢能是一种理想途径。某中光分解水的过程如图1所示。
①与电解水相比,该方法的优点是______ 。
②用化学方程式表示反应Ⅰ的过程_______ 。
(2)CH4- H2O催化重整是目前大规模制取H2的重要方法,生产过程中涉及的重要反应有:
CH4+H2O CO+3H2;CO+H2O
CO+3H2;CO+H2O CO2+H2
CO2+H2
①若将8tCH4用于制取H2,假设每一步均完全反应,理论上可制得H2_____ t。
②如图2,向CH4- H2O催化重整体系中投入定量的CaO可提高H2百分含量,而投入纳米CaO时H2的百分含量最大,原因可能是_______ 。
II.储存“氢气”:
(3)氢气可以直接加压储存在储氢罐中,从微粒视角分析,主要原因是_____(填字录)。
(4)种镁铝合金可用于 储氢。将镁、铝单质按质量比为 34:27的比例在定条件下熔炼得到镁铝合金。该镁铝合金的化学式为______ 。
Ⅲ.运输“氢气”:
(5)主要有3种运输方式:管道、气瓶车和液氢槽车。H2的运输成本与运输距离的关系如图3所示。从图中可分析,运输成本受距离影响较大的运输方式是_______ 。
Ⅳ.应用“氢气”:
(6)氢气和氧气在Pd基催化剂表面可反应生成过氧化氢,其微观示意图如下。

“解离”时,结构被破坏的分子是_____ (填化学式)。
(7)该反应的化学方程式为______ 。

I.制备“氢气”:
(1)利用太阳能将水转化为氢能是一种理想途径。某中光分解水的过程如图1所示。
①与电解水相比,该方法的优点是
②用化学方程式表示反应Ⅰ的过程
(2)CH4- H2O催化重整是目前大规模制取H2的重要方法,生产过程中涉及的重要反应有:
CH4+H2O
 CO+3H2;CO+H2O
CO+3H2;CO+H2O CO2+H2
CO2+H2①若将8tCH4用于制取H2,假设每一步均完全反应,理论上可制得H2
②如图2,向CH4- H2O催化重整体系中投入定量的CaO可提高H2百分含量,而投入纳米CaO时H2的百分含量最大,原因可能是
II.储存“氢气”:
(3)氢气可以直接加压储存在储氢罐中,从微粒视角分析,主要原因是_____(填字录)。
| A.分子间有空隙 | B.分子非常小 | C.分子是不断运动的 |
Ⅲ.运输“氢气”:
(5)主要有3种运输方式:管道、气瓶车和液氢槽车。H2的运输成本与运输距离的关系如图3所示。从图中可分析,运输成本受距离影响较大的运输方式是
Ⅳ.应用“氢气”:
(6)氢气和氧气在Pd基催化剂表面可反应生成过氧化氢,其微观示意图如下。

“解离”时,结构被破坏的分子是
(7)该反应的化学方程式为
更新时间:2023-05-18 12:58:28
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】Na2SO4是制作纸张、药品、染料稀释剂等的重要原料。某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图1所示。

(1)加入NaOH溶液可除去的阳离子是____ (填离子符号),其反应的化学方程式为: ____ 。若添加的NaOH和Na2CO3过量,可加入适量____ (填名称)除去。
(2)溶液M中的溶质是Na2SO4和杂质NaCl,观察图2的溶解度曲线,则操作b是:先将溶液M蒸发浓缩,再降温结晶、过滤,降温结晶的最佳温度范围是__ ℃以下,因为Na2SO4的溶解度__ 。

(1)加入NaOH溶液可除去的阳离子是
(2)溶液M中的溶质是Na2SO4和杂质NaCl,观察图2的溶解度曲线,则操作b是:先将溶液M蒸发浓缩,再降温结晶、过滤,降温结晶的最佳温度范围是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3·xH2O),E、F、I为无色气体。根据图示回答下列问题。

(1)写出有关物质的化学式:E_______ ,J________ ,
(2)写出有关反应的化学方程式:
反应①:______________________________ ;
反应④:______________________________ ;
反应⑤:______________________________ ;
(3)反应④属于_______ 反应(填反应基本类型)。
(4)日常生活中为了阻止反应③发生,通常采取的措施是:___________________ (写一条)。

(1)写出有关物质的化学式:E
(2)写出有关反应的化学方程式:
反应①:
反应④:
反应⑤:
(3)反应④属于
(4)日常生活中为了阻止反应③发生,通常采取的措施是:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
真题
解题方法
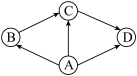
【推荐3】A、B、C、D为初中化学常见的物质,且都含有同一种元素,他们之间有如图所示的转化关系(“→”表示前一种物质经一步反应可转化为后一种物质,部分反应物、生成物及反应条件已略去),且这些转化都是初中化学常见的化学反应。
(1)若B、C、D属于同类物质,且常温下状态各不相同,则C的化学式是_____ ,写出一个符合A→D的化合反应_____ (用化学方程式表示)。
(2)若B的物质类别与A、C、D不同,D由两种元素组成。A为纯碱,则A的化学式是_____ ,C→D的化学方程式为:_____ 。
(1)若B、C、D属于同类物质,且常温下状态各不相同,则C的化学式是
(2)若B的物质类别与A、C、D不同,D由两种元素组成。A为纯碱,则A的化学式是

您最近一年使用:0次
【推荐1】CO2是重要的自然资源,和人类的活动息息相关。
(1)2022北京冬奥会国家速滑馆“冰丝带”的制冰过程中使用了环保的二氧化碳跨临界直冷技术。该技术是将气态二氧化碳通过加温加压形成液态二氧化碳,再减小压力使液态二氧化碳气化吸热实现制冷。请从微观角度解释液态二氧化碳气化的过程_____ 。
(2)生活中二氧化碳常可用于灭火,利用了二氧化碳的哪些性质?_____ 。
(3)用图1所示装置进行实验,先推入NaOH溶液,再推入稀盐酸,测得过程中压强变化如图2所示。

①用化学方程式解释ab段压强明显减小的原因_____ ;
②设计实验证明b点溶液中没有NaOH剩余_____ 。
(4)利用CO2是实现碳中和的一种途径,我国科学家合成的一种新型催化剂可以使CO2和H2发生反应,生成一种清洁燃料甲醇(CH3OH),反应的微观示意图如图所示。写出该反应的化学方程式____ 。

(5)CO2可与物质X相互转化。
若物质X是一种盐,且物质中金属元素的质量分数为40%,则X的化学式为_______ ;若物质X是一种氧化物,则X→CO2的化学方程式为_______ 。
(6)天然气的主要成分是甲烷,48g甲烷完全燃烧可排放多少二氧化碳?
(1)2022北京冬奥会国家速滑馆“冰丝带”的制冰过程中使用了环保的二氧化碳跨临界直冷技术。该技术是将气态二氧化碳通过加温加压形成液态二氧化碳,再减小压力使液态二氧化碳气化吸热实现制冷。请从微观角度解释液态二氧化碳气化的过程
(2)生活中二氧化碳常可用于灭火,利用了二氧化碳的哪些性质?
(3)用图1所示装置进行实验,先推入NaOH溶液,再推入稀盐酸,测得过程中压强变化如图2所示。

①用化学方程式解释ab段压强明显减小的原因
②设计实验证明b点溶液中没有NaOH剩余
(4)利用CO2是实现碳中和的一种途径,我国科学家合成的一种新型催化剂可以使CO2和H2发生反应,生成一种清洁燃料甲醇(CH3OH),反应的微观示意图如图所示。写出该反应的化学方程式

(5)CO2可与物质X相互转化。
若物质X是一种盐,且物质中金属元素的质量分数为40%,则X的化学式为
(6)天然气的主要成分是甲烷,48g甲烷完全燃烧可排放多少二氧化碳?
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】我国煤炭资源丰富。目前人们除了将煤作为燃料外,更是重要的化工原料。工业上以煤和空气为原料生产尿素[CO(NH2)2]的一种流程如图:

(1)煤的气化过程属________ 变化,从液态空气中分离出N2的过程属于________ (填“物理”或“化学”)变化。利用液态空气中________ 不同分离得到氮气。
(2)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是___________ 。
(3)水煤气在铜催化下实现CO的转化:CO+H2O CO2+X,其中X的化学式
CO2+X,其中X的化学式________ 。
(4)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为______ 。
(5)实际生产中,N2和H2不可能全部转化为NH3。上述流程中可以循环利用的物质有_______ 。
(6)以CO2和H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为2CO2+6H2 C2H6O+3H2O。已知:每克燃料完全燃烧放出的热量叫做热值。
C2H6O+3H2O。已知:每克燃料完全燃烧放出的热量叫做热值。
若将含12g碳的煤为原料合成的乙醇完全燃烧。理论上最多可放出________ kJ的热量,从而提高了煤的利用效率。

(1)煤的气化过程属
(2)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是
(3)水煤气在铜催化下实现CO的转化:CO+H2O
 CO2+X,其中X的化学式
CO2+X,其中X的化学式(4)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为
(5)实际生产中,N2和H2不可能全部转化为NH3。上述流程中可以循环利用的物质有
(6)以CO2和H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为2CO2+6H2
 C2H6O+3H2O。已知:每克燃料完全燃烧放出的热量叫做热值。
C2H6O+3H2O。已知:每克燃料完全燃烧放出的热量叫做热值。| 物 质 | 煤 | 乙 醇 |
| 热值/(kJ·g-1) | 约33 | 30 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】利用分子的性质解释下列事实:
(1)加油站里的汽油已贮存在油罐中,但在离油罐一定距离内仍要“严禁烟火”。_____________ 。
(2)液氧和氧气的状态不同,但具有相同的化学性质。________ 。
(3)酒精燃烧后生成水和二氧化碳。___________________ 。
(4)气体容易被压缩,而液体、固体难以压缩。___________ 。
(1)加油站里的汽油已贮存在油罐中,但在离油罐一定距离内仍要“严禁烟火”。
(2)液氧和氧气的状态不同,但具有相同的化学性质。
(3)酒精燃烧后生成水和二氧化碳。
(4)气体容易被压缩,而液体、固体难以压缩。
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】科学方法对化学学习起着事半功倍的作用。下图是某同学整理的铁及其化合物知识网络图。

(1)分类归纳是研究化学物质的重要方法。
①铁丝燃烧生成Fe3O4的过程中________ (选填“放出”或“吸收”)热量。
②铁制品的锈蚀过程,实际上是铁与空气中的_____________ 等发生化学反应的过程。
③与FeSO4中铁元素化合价相同的铁的氧化物的化学式是_____________ 。
(2)微观粒子模型化是研究化学变化的重要方法。

①图甲是钠与氯气反应生成氯化钠的示意图,该图说明在化学反应过程中一定发生变化的是__________ (填字母序号,下同)。
a.原子核 b.原子的最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应的示意图。从粒子角度分析该化学反应能发生的原因是___________________________ 。
(3)控制变量、设计对比实验是实验探究的重要方法。

①实验1中同时向两烧杯中各加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短。这是因为___________________________ 。
②实验2中使用铜片是为了对比_______________________ 不同。
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论正确的是___________ 。
a.铜不能与盐酸发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌粒和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多

(1)分类归纳是研究化学物质的重要方法。
①铁丝燃烧生成Fe3O4的过程中
②铁制品的锈蚀过程,实际上是铁与空气中的
③与FeSO4中铁元素化合价相同的铁的氧化物的化学式是
(2)微观粒子模型化是研究化学变化的重要方法。

①图甲是钠与氯气反应生成氯化钠的示意图,该图说明在化学反应过程中一定发生变化的是
a.原子核 b.原子的最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应的示意图。从粒子角度分析该化学反应能发生的原因是
(3)控制变量、设计对比实验是实验探究的重要方法。

①实验1中同时向两烧杯中各加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短。这是因为
②实验2中使用铜片是为了对比
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论正确的是
a.铜不能与盐酸发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌粒和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】(1)2018年10月,中科院大连化物所与福州大学化学学院 y合作发展了一种固态Z--机制复合光催化剂,实现了太阳能人工光合成燃料过程,反应的微观示意图如下图所示,该反应的化学方程式______ 。

(2)某兴趣小组在做硫酸铜固体溶于水的实验时,观察到如图1现象。

①溶解后,硫酸铜固体“消失”及液面比原水平线低的微观解析正确的是____________ (填标号)。
A微粒的体积变小了 B微粒不断运动 C微粒之间有间隔
②向 溶液中滴入
溶液中滴入 溶液至恰好完全反应。可以观察到的实验现象是
溶液至恰好完全反应。可以观察到的实验现象是_________ 。如图2表示该反应前后溶液中存在的主要离子,写出下列每种图形代表的离子(填离子符号):
_____ ,
_____


(2)某兴趣小组在做硫酸铜固体溶于水的实验时,观察到如图1现象。

①溶解后,硫酸铜固体“消失”及液面比原水平线低的微观解析正确的是
A微粒的体积变小了 B微粒不断运动 C微粒之间有间隔
②向
 溶液中滴入
溶液中滴入 溶液至恰好完全反应。可以观察到的实验现象是
溶液至恰好完全反应。可以观察到的实验现象是


您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】现有甲、乙、丙、丁、戊五种初中化学常见的物质,其中乙、丙、丁在通常状况下为三种不同状态的氧化物。图①中“一”表示两物质之间能发生反应,“→”表示两物质之间能发生一步转化。(部分反应物、生成物及反应条件已略去,部分反应在溶液中进行)。


(1)如图②是探究物质丙组成的实验,a处为电源的______ 极。
(2)乙与戊反应的实验现象为______ 。
(3)丙与丁发生反应的化学方程式为______ 。
(4)若甲经一步反应同时生成乙和丙,则甲不可能是( ) (只有一个正确选项)
A.单质 B.氧化物 C.酸 D.盐


(1)如图②是探究物质丙组成的实验,a处为电源的
(2)乙与戊反应的实验现象为
(3)丙与丁发生反应的化学方程式为
(4)若甲经一步反应同时生成乙和丙,则甲不可能是
A.单质 B.氧化物 C.酸 D.盐
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】(1)生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水。
①下列“水”中,属于纯净物的是________ (填序号);
a.海水 b.河水 c.蒸馏水 d.井水
②水在通电条件下分解的化学方程式为__________ ;
③生活中可用活性炭净水器来净水,是利用了活性炭的_______ ,生活中可用______ 的方法降低水的硬度。
(2)根据图中A、B、C三种物质的溶解度曲线回答下列问题。

①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_______ 。
②t2℃时,30gA物质投入到50g水中所得到溶液是质量为_______ g。
③如果A中混有少量的B,可采用_________ 进行提纯A。
①下列“水”中,属于纯净物的是
a.海水 b.河水 c.蒸馏水 d.井水
②水在通电条件下分解的化学方程式为
③生活中可用活性炭净水器来净水,是利用了活性炭的
(2)根据图中A、B、C三种物质的溶解度曲线回答下列问题。

①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
②t2℃时,30gA物质投入到50g水中所得到溶液是质量为
③如果A中混有少量的B,可采用
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】定性研究和定量研究既是化学的重要思想,也是研究化学变化的重要方法。“追梦”学习小组走进实验室,分别从定性、定量角度探究化学变化。

(1)定性探究“水在直流电作用下的变化”,请回答下列问题。在水电解器的玻璃管中注满水,接通直流电源。一段时间后,两电极都有气泡产生,左右两侧玻璃管中的液面有不同程度的下降。
①接通直流电源一段时间后,将燃着的木条放在b玻璃管口,打开活塞,气体燃烧,火焰呈淡蓝色,该气体是______ ;写出电解水的文字表达式为______ 。
②由上述实验可以得出:水是由______ (填元素名称)元素组成的。
③水通电分解时没有发生变化的是______ (选填序号之一)。
A.水分子的结构 B.氢原子和氧原子 C.水分子的能量
(2)“追梦”学习小组想用如图装置探究质量守恒定律,请回答下列问题。

①确定研究对象:可以选择的化学反应是______ 。(选填序号之一)
A.盐酸和大理石反应,生成氯化钙、水和二氧化碳
B.氢氧化钠溶液和硫酸铜溶液反应,生成硫酸钠和氢氧化铜
②进行实验:反应前后天平指针不发生偏转。
③得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
④迁移应用:下列现象能用质量守恒定律解释的是______ (答案合理均选)。
A.镁条燃烧时,生成的白色粉末的质量大于镁条质量
B.氢气燃烧时,参加反应的氢气和氧气的体积大于生成水的体积
(3)“追梦”学习小组用收集到的氧气做铁丝燃烧的实验时,观察到的现象有_______ ,反应的文字表达式为:_______ 。红热的铁丝在空气中不能燃烧,在纯氧中剧烈燃烧,请从微观角度解释:________ 。


(1)定性探究“水在直流电作用下的变化”,请回答下列问题。在水电解器的玻璃管中注满水,接通直流电源。一段时间后,两电极都有气泡产生,左右两侧玻璃管中的液面有不同程度的下降。
①接通直流电源一段时间后,将燃着的木条放在b玻璃管口,打开活塞,气体燃烧,火焰呈淡蓝色,该气体是
②由上述实验可以得出:水是由
③水通电分解时没有发生变化的是
A.水分子的结构 B.氢原子和氧原子 C.水分子的能量
(2)“追梦”学习小组想用如图装置探究质量守恒定律,请回答下列问题。

①确定研究对象:可以选择的化学反应是
A.盐酸和大理石反应,生成氯化钙、水和二氧化碳
B.氢氧化钠溶液和硫酸铜溶液反应,生成硫酸钠和氢氧化铜
②进行实验:反应前后天平指针不发生偏转。
③得出结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
④迁移应用:下列现象能用质量守恒定律解释的是
A.镁条燃烧时,生成的白色粉末的质量大于镁条质量
B.氢气燃烧时,参加反应的氢气和氧气的体积大于生成水的体积
(3)“追梦”学习小组用收集到的氧气做铁丝燃烧的实验时,观察到的现象有

您最近一年使用:0次



