加热氯酸钾和二氧化锰的混合物制取氧气,充分反应后剩余固体40.8g,对剩余固体,做如下实验。试回答下列问题:
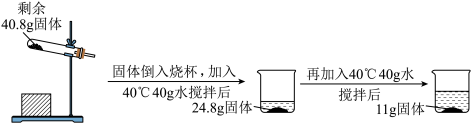
(1)制取氧气发生的化学反应方程式为___________ 。
(2)根据已知条件列出求解参加反应的氯酸钾质量(x)的比例式___________ 。
(3)上述实验制得氧气的质量___________ 。
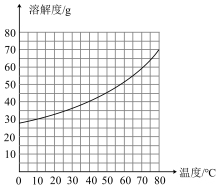
(4)所得溶液的溶质在40℃下溶解度为___________ 。
(5)将最终所得固液混合物过滤,再向滤液中加入39.2g水,计算最终所得溶液中溶质的质量分数。

(1)制取氧气发生的化学反应方程式为
(2)根据已知条件列出求解参加反应的氯酸钾质量(x)的比例式
(3)上述实验制得氧气的质量
(4)所得溶液的溶质在40℃下溶解度为
(5)将最终所得固液混合物过滤,再向滤液中加入39.2g水,计算最终所得溶液中溶质的质量分数。

更新时间:2023-05-21 09:39:19
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】Ⅰ.明代宋应星所著的《天工开物》中有煅烧炉甘石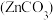 和煤炭(C)炼锌的记载,其化学反应原理为:
和煤炭(C)炼锌的记载,其化学反应原理为: 。某化学兴趣小组在实验室用
。某化学兴趣小组在实验室用 和
和 模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其他因素对结果的影响):
模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其他因素对结果的影响):

回答下列问题:
(1)按如图连接好装置后,装入药品前,首先应进行的操作是__________ 。
(2)A装置试管中加入足量稀硫酸充分反应后,仍有少量黑色固体剩余,说明粗锌中一定含有________ 。
(3)B装置中澄清石灰水变浑浊,此时B装置中发生反应的化学方程式为_________ ,B装置的作用是__________ 。
(4)综合以上实验现象可知,粗锌含有的杂质有__________ 。
Ⅱ.“三寸粉笔,三尺讲台系国运”这是对教师的礼赞。教师授课离不开粉笔,粉笔主要成分为石灰石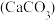 和石膏
和石膏 。如图,将16g制作好的粉笔末放于硬质玻璃管中加热使其充分反应,冷却后称量剩余固体的质量为11.6 g。
。如图,将16g制作好的粉笔末放于硬质玻璃管中加热使其充分反应,冷却后称量剩余固体的质量为11.6 g。
已知:硫酸钙受热不分解,也不与 反应。其他杂质不参与反应。
反应。其他杂质不参与反应。

回答下列问题:
(5) 的相对分子质量为
的相对分子质量为__________ 。
(6)计算16g粉笔末中 的质量分数。(写出计算过程)
的质量分数。(写出计算过程)
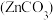 和煤炭(C)炼锌的记载,其化学反应原理为:
和煤炭(C)炼锌的记载,其化学反应原理为: 。某化学兴趣小组在实验室用
。某化学兴趣小组在实验室用 和
和 模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其他因素对结果的影响):
模拟古法炼锌。实验结束后,同学们设计实验对2.0g粗锌产品中含有的杂质进行探究并测定粗锌中单质锌的含量。实验装置设计如下(忽略其他因素对结果的影响):
回答下列问题:
(1)按如图连接好装置后,装入药品前,首先应进行的操作是
(2)A装置试管中加入足量稀硫酸充分反应后,仍有少量黑色固体剩余,说明粗锌中一定含有
(3)B装置中澄清石灰水变浑浊,此时B装置中发生反应的化学方程式为
(4)综合以上实验现象可知,粗锌含有的杂质有
Ⅱ.“三寸粉笔,三尺讲台系国运”这是对教师的礼赞。教师授课离不开粉笔,粉笔主要成分为石灰石
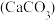 和石膏
和石膏 。如图,将16g制作好的粉笔末放于硬质玻璃管中加热使其充分反应,冷却后称量剩余固体的质量为11.6 g。
。如图,将16g制作好的粉笔末放于硬质玻璃管中加热使其充分反应,冷却后称量剩余固体的质量为11.6 g。已知:硫酸钙受热不分解,也不与
 反应。其他杂质不参与反应。
反应。其他杂质不参与反应。
回答下列问题:
(5)
 的相对分子质量为
的相对分子质量为(6)计算16g粉笔末中
 的质量分数。(写出计算过程)
的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】实验室常用过氧化氢溶液与二氧化锰混合制取氧气,现将2.5g二氧化锰放入盛有50g过氧化氢溶液的锥形瓶中,完全反应后,放出气体的质量与反应时间的关系如图所示。
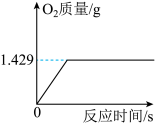
(1)完全反应后生成的氧气______ g。
(2)写出过氧化氢溶液制取氧气的符号表达式:______ 。
(3)反应结束后,过滤、洗涤并烘干滤渣,称得滤渣的质量为______ g。
(4)如果改用分离液态空气法来得到以上质量的氧气,大概需要多少L的空气?(写出计算过程,已知氧气的密度是1.429g/L)

(1)完全反应后生成的氧气
(2)写出过氧化氢溶液制取氧气的符号表达式:
(3)反应结束后,过滤、洗涤并烘干滤渣,称得滤渣的质量为
(4)如果改用分离液态空气法来得到以上质量的氧气,大概需要多少L的空气?(写出计算过程,已知氧气的密度是1.429g/L)
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐3】乙烯(CaHb)是一种重要的基本化工原料。能燃烧;在一定条件下,可与H2O发生加成反应(属于化合反应)制备乙醇;由乙烯之间的相互加成可以得到聚乙烯[(CaHb)n],聚乙烯制品在现代生活中用途很广。请你完成下列问题,体会“科学思维”的魅力。
(1)乙烯完全燃烧的化学方程式为:CaHb+3O2 2CO2+xH2O;则乙烯的化学式为
2CO2+xH2O;则乙烯的化学式为_______ ,聚乙烯中C、H元素的质量比为______ (填最简整数)。
(2)已知完全燃烧7份质量的乙烯生成22份质量的CO2。若完全燃烧14kg乙烯经加成反应制备的乙醇,则会生成CO2_______ kg。
(3)化工厂用560kg乙烯与H2O发生加成反应,最多可制备出多少乙醇?(请写出计算过程)
(1)乙烯完全燃烧的化学方程式为:CaHb+3O2
 2CO2+xH2O;则乙烯的化学式为
2CO2+xH2O;则乙烯的化学式为(2)已知完全燃烧7份质量的乙烯生成22份质量的CO2。若完全燃烧14kg乙烯经加成反应制备的乙醇,则会生成CO2
(3)化工厂用560kg乙烯与H2O发生加成反应,最多可制备出多少乙醇?(请写出计算过程)
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】用28g氧化钙与足量的水反应,计算生成Ca(OH)2的质量。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】实验室利用一氧化碳还原4g氧化铜,理论上能得到铜的质量是多少?
您最近一年使用:0次
计算题
|
较易
(0.85)
真题
解题方法
【推荐1】某创新小组的同学,在用MnO2,作催化剂制取O2的实验过程中遇到了困惑,通过老师点拨,他们厘清了思路,找到了解决问题的办法,小华将图像绘制在黑板上,并将方法分享给其他同学。
(1)观点分享:b曲线始终不变的原因是______ 。
(2)展示交流:结合黑板上的试题要求,请在答题卡上写出解题过程(最后结果精确到0.01)。
(1)观点分享:b曲线始终不变的原因是
(2)展示交流:结合黑板上的试题要求,请在答题卡上写出解题过程(最后结果精确到0.01)。
实验室用KC1O3和MnO2的混合物制取O2,其中MnO2为2g,它在固体混合物中的质量分数为25%,求KClO3完全反应后生成O2的质量。 |
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:

求:
(1)该同学制得氧气的质量________ g。
(2)反应前固体中所含氯酸钾的质量。

求:
(1)该同学制得氧气的质量
(2)反应前固体中所含氯酸钾的质量。
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】实验室用氯酸钾与二氧化锰混合来制取氧气。2KClO3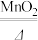 2KCl+3O2↑现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量。
2KCl+3O2↑现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量。
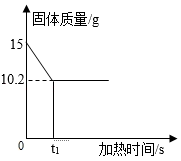
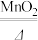 2KCl+3O2↑现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量。
2KCl+3O2↑现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】20℃时,硝酸钾的溶解度为31.6g,将20g硝酸钾投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数.
您最近一年使用:0次
计算题
|
较易
(0.85)
真题
解题方法
【推荐2】食盐中常添加少量的碘酸钾(KIO3)。已知30℃时,碘酸钾的溶解度为10g。(1) 碘酸钾中钾元素与氧元素的质量比为 。
(2)30℃时,碘酸钾饱和溶液中溶质的质量分数为 (精确到0 1%)。
(2)30℃时,碘酸钾饱和溶液中溶质的质量分数为 (精确到0 1%)。
您最近一年使用:0次

 。若通过该反应消耗二氧化碳22 kg,理论上可产生水的质量是多少?
。若通过该反应消耗二氧化碳22 kg,理论上可产生水的质量是多少?