下表是硝酸钾和氯化钾在不同温度时的溶解度,请回答下列问题。
(1)两种物质中溶解度受温度影响较小的是______ 。若硝酸钾中混有少量氯化钾,可采用______ 方法提纯硝酸钾。
(2)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是______ 。
(3)40℃时,将25g氯化钾加入50g水中,所得溶液质量为______ 。
(4)从表中数据可知,在温度为______ 的范围内,氯化钾和硝酸钾的溶解度相同。
温度℃ | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | 硝酸钾 | 31.6 | 45.8 | 63.8 | 85.5 | 110 |
氯化钾 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
(2)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是
(3)40℃时,将25g氯化钾加入50g水中,所得溶液质量为
(4)从表中数据可知,在温度为
2023·广西南宁·二模 查看更多[4]
2023年广西壮族自治区南宁市西乡塘区中考二模化学试题2023年广西省南宁市第二十四中学中考三模化学试题(已下线)9.2 溶解度(专题训练)【十三大题型】-2023-2024学年九年级化学下册同步考点解读与专题训练(人教版)(已下线)2024年中考风向标-广西-溶液、溶解度和溶解度曲线的应用
更新时间:2023-05-25 12:33:05
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:

(1)在____________ ℃时,A和C的饱和溶液中溶质的质量分数相等.
(2)t2℃时,将20gA放入50g水中充分溶解后,所得溶液质量是____________ g.
(3)若B中含有少量A,可用____________ 的方法提纯B.
(4)将A、B、C的饱和溶液从t3℃降温到t1℃,析出晶体质量最多的是____________ (填“A”、“B”、“C”或“无法确定”)

(1)在
(2)t2℃时,将20gA放入50g水中充分溶解后,所得溶液质量是
(3)若B中含有少量A,可用
(4)将A、B、C的饱和溶液从t3℃降温到t1℃,析出晶体质量最多的是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
真题
名校
【推荐2】下图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:
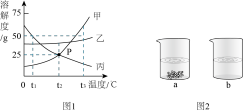
(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是_________ 。
(2)P点表示,t2℃时,甲、丙两种物质的饱和溶液中,溶质与溶剂的质量比相等,均为_____ 。
(3)t2℃时,取甲、乙两种固体各15g分别加入40g水中充分溶解,实验现象如图2所示,
则烧杯a中溶解的物质是________ (填“甲”或‘‘乙”),所得溶液的质量为 ______ g。
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用______ (填(“降温”或“蒸发”)结晶的方法提纯甲物质。
(5)下列说法正确的是____ (填字母序号)。
A 将甲物质的溶液由t3℃降温到t2℃,一定有晶体析出
B 将甲物质的饱和溶液由t2℃升温至t3℃时,其溶质质量分数增大
C 将t3℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
D 将t3℃三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数:乙>甲=丙

(1)t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是
(2)P点表示,t2℃时,甲、丙两种物质的饱和溶液中,溶质与溶剂的质量比相等,均为
(3)t2℃时,取甲、乙两种固体各15g分别加入40g水中充分溶解,实验现象如图2所示,
则烧杯a中溶解的物质是
(4)当甲中含有少量的乙和丙(甲、乙、丙相互间均不发生化学反应)时,可采用
(5)下列说法正确的是
A 将甲物质的溶液由t3℃降温到t2℃,一定有晶体析出
B 将甲物质的饱和溶液由t2℃升温至t3℃时,其溶质质量分数增大
C 将t3℃时三种物质的饱和溶液恒温蒸发等质量的水,析出溶质的质量:甲>乙>丙
D 将t3℃三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数:乙>甲=丙
您最近一年使用:0次
【推荐3】海洋是一个巨大的资源宝库。
(1)金属镁广泛应用于火箭、导弹和飞机制造业,目前世界上60%的镁是从海水(主要含NaCl和MgCl2)中提取的。主要步骤如下图所示,试回答以下问题:

写出过程步骤②反应的化学方程式________ ,该反应属于_____ (填“化合”“分解”“置换”“复分解”之一)反应。海水或卤水中本来就含有氯化镁,为什么还要经过①②两个步骤,重新制得氯化镁?原因是____________ 。
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如图所示,试回答下列问题:
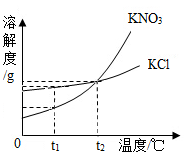
①在____________ ℃时,KCl和KNO3的溶解度相等。
②已知30℃时,KNO3的溶解度为46g。30℃时,向50g水中加入28g KNO3固体,形成的溶液是此温度下KNO3的__________ (填“饱和”或“不饱和”之一)溶液。此时溶液中溶质质量分数为___________ (计算结果精确至0.1%)。
③当KNO3固体中含有少量KCl时,可采用__________ 的方法提纯KNO3(填“降温结晶”、“蒸发结晶”之一)。
(3)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源——“可燃冰”。请写出“可燃冰”充分燃烧的反应的化学方程式_________ ;下列有关“可燃冰”的说法正确的是___________ 。

A.“可燃冰”是可再生能源
B.“可燃冰”燃烧产物只有水,无污染
C.“可燃冰”热值高,燃烧后几乎不产生任何残渣和废气,被誉为“未来能源”
(4)从浩瀚的海洋中获取淡水,对解决淡水危机具有重要意义。下列方法中能淡化海水的是_______(填字母)。
(1)金属镁广泛应用于火箭、导弹和飞机制造业,目前世界上60%的镁是从海水(主要含NaCl和MgCl2)中提取的。主要步骤如下图所示,试回答以下问题:

写出过程步骤②反应的化学方程式
(2)海水中除了蕴含大量的钠元素和镁元素外,还含有大量的钾元素。KCl和KNO3的溶解度曲线如图所示,试回答下列问题:

①在
②已知30℃时,KNO3的溶解度为46g。30℃时,向50g水中加入28g KNO3固体,形成的溶液是此温度下KNO3的
③当KNO3固体中含有少量KCl时,可采用
(3)海底不仅蕴藏着大量的煤、石油、天然气等常规化石燃料,人们还在海底发现了一种新型矿产资源——“可燃冰”。请写出“可燃冰”充分燃烧的反应的化学方程式

A.“可燃冰”是可再生能源
B.“可燃冰”燃烧产物只有水,无污染
C.“可燃冰”热值高,燃烧后几乎不产生任何残渣和废气,被誉为“未来能源”
(4)从浩瀚的海洋中获取淡水,对解决淡水危机具有重要意义。下列方法中能淡化海水的是_______(填字母)。
| A.过滤法 | B.多级闪急蒸馏法 | C.沉淀法 | D.分解法 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
(1)两种物质中,溶解度受温度影响变化较大的是_________。
(2)60℃时,按图示操作:

A中溶质是_____(填“饱和”或“不饱和”)溶液,C中溶液的总质量是______g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液_____(填“大于”“等于”或“小于”) KNO3溶液。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
(2)60℃时,按图示操作:

A中溶质是_____(填“饱和”或“不饱和”)溶液,C中溶液的总质量是______g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液_____(填“大于”“等于”或“小于”) KNO3溶液。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图是甲、乙、丙三种物质的溶解度曲线.请根据图中信息回答下列问题:_______ (任填一种);
(2)t3℃时,把30 g甲充分溶解在50 g水中,所得溶液质量是_______ g。
(3)t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是_______ 。
(4)若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是_______ 。

(2)t3℃时,把30 g甲充分溶解在50 g水中,所得溶液质量是
(3)t3℃时,甲、乙、丙三种物质的等质量饱和溶液中,所含溶剂质量最多的是
(4)若甲中混有少量乙,要得到纯净的甲,常用的提纯方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】A、B两种物质溶解度曲线如图1所示,20℃时将A、B两种固体各50g分别加到各有100g水的烧杯中,充分搅拌后现象如图2所示,升温到50℃时A、B两种固体在水中的溶解情况如图3所示,请回答下列问题。

(1)图1中能表示A物质溶解度随温度变化的曲线是________ (填“甲”或“乙”)。
(2)P点表示的意义________ 。
(3)50℃时,A溶液为________ (填“不饱和”或“饱和”)溶液。
(4)图1中欲将50℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是________ 。
(5)分别将50℃时80g甲、乙的饱和溶液降温到20℃,以下说法正确的是________。

(1)图1中能表示A物质溶解度随温度变化的曲线是
(2)P点表示的意义
(3)50℃时,A溶液为
(4)图1中欲将50℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是
(5)分别将50℃时80g甲、乙的饱和溶液降温到20℃,以下说法正确的是________。
| A.溶液的质量:甲<乙 | B.溶剂的质量:甲=乙 |
| C.溶质的质量分数:甲>乙 | D.甲溶液析出的固体质量:35g |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如表是硝酸钾、氯化钠在不同温度下的溶解度.
(1)从表中数据分析,溶解度受温度影响较大的物质是__________ ,硝酸钾和氯化钠溶解度曲线的交点在__________ (填字母序号)之间.
A.20℃~30℃ B.30℃~40℃ C.40℃~50℃
(2)20℃,将50g硝酸钾与100g水混合,充分搅拌后静置,得到的溶液的质量是_________ ,是硝酸钾的__________ (“饱和”或“不饱和”)溶液,若将温度升高到40℃,该溶解溶质的质量分数为__________ (精确到0.1%).
(3)保持温度为20℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法__________ 。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 硝酸钾的溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
| 氯化钠的溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)从表中数据分析,溶解度受温度影响较大的物质是
A.20℃~30℃ B.30℃~40℃ C.40℃~50℃
(2)20℃,将50g硝酸钾与100g水混合,充分搅拌后静置,得到的溶液的质量是
(3)保持温度为20℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水与溶液对于生产、生活有着重要意义。
(1)家庭生活中常用净水器,净水器滤芯中可用____________ 去除水中杂质。
(2)在水中加入洗涤剂可以除去衣物上的油污,这是利用了洗涤剂的__________ 作用。
(3)下表是碳酸钠的部分溶解度数据。
①由表中数据可知,碳酸钠属于____________ 物质(“易溶”“可溶”“微溶”或“难溶”)
②小东同学进行了如下图所示的实验,若使烧杯③中的溶液达到饱和,至少需再加入________ g碳酸钠;升温至60℃时,烧杯④中会出现的现象是______ 。

③20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是______ (填字母序号),该物质形成的溶液中存在的微粒有_______ 。
A.氢氧化钠 B.碳酸钙 C.硝酸铵 D.氯化钠
(4)现有
 两个反应,其反应规律和金属与金属化合物溶液的置换反应类似,则Br2、C12、12三种非金属活动性顺序由大到小为
两个反应,其反应规律和金属与金属化合物溶液的置换反应类似,则Br2、C12、12三种非金属活动性顺序由大到小为_____ 。
(1)家庭生活中常用净水器,净水器滤芯中可用
(2)在水中加入洗涤剂可以除去衣物上的油污,这是利用了洗涤剂的
(3)下表是碳酸钠的部分溶解度数据。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
②小东同学进行了如下图所示的实验,若使烧杯③中的溶液达到饱和,至少需再加入

③20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是
A.氢氧化钠 B.碳酸钙 C.硝酸铵 D.氯化钠
(4)现有

 两个反应,其反应规律和金属与金属化合物溶液的置换反应类似,则Br2、C12、12三种非金属活动性顺序由大到小为
两个反应,其反应规律和金属与金属化合物溶液的置换反应类似,则Br2、C12、12三种非金属活动性顺序由大到小为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】图1是甲、乙、丙三种物质的溶解度曲线,据图回答:_____ 。
(2)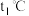 时,30g甲物质加到50g水中不断搅拌,形成的溶液质量是
时,30g甲物质加到50g水中不断搅拌,形成的溶液质量是_____ g。
(3)将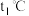 时甲、乙、丙三种物质饱和溶液的温度升高到
时甲、乙、丙三种物质饱和溶液的温度升高到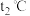 时,溶质质量分数由大到小的关系是
时,溶质质量分数由大到小的关系是_____ 。
(4)当甲中混有少量的乙时,应采用_____ 方法提纯甲。
(5)如图2所示,20℃时,将盛有饱和 溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____。(填字母序号)
溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____。(填字母序号)

(2)
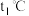 时,30g甲物质加到50g水中不断搅拌,形成的溶液质量是
时,30g甲物质加到50g水中不断搅拌,形成的溶液质量是(3)将
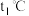 时甲、乙、丙三种物质饱和溶液的温度升高到
时甲、乙、丙三种物质饱和溶液的温度升高到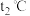 时,溶质质量分数由大到小的关系是
时,溶质质量分数由大到小的关系是(4)当甲中混有少量的乙时,应采用
(5)如图2所示,20℃时,将盛有饱和
 溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____。(填字母序号)
溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的_____。(填字母序号)| A.氢氧化钠固体 | B.生石灰固体 | C.冰块 | D.硝酸铵固体 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:

(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲_____ 乙(填“<”“>“或“=”);
(2)P点的含义_____ ;
(3)t2℃时,把20g固体甲放入50g水中,充分搅拌,所得溶液的质量是_____ g;
(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是_____ ;
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用_____ 的方法。
(6)若将t3℃时甲和乙的饱和溶解降温至t1℃时,所得溶液的溶质质量分数关系为_____ 。

(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲
(2)P点的含义
(3)t2℃时,把20g固体甲放入50g水中,充分搅拌,所得溶液的质量是
(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用
(6)若将t3℃时甲和乙的饱和溶解降温至t1℃时,所得溶液的溶质质量分数关系为
您最近一年使用:0次
【推荐2】生活中处处有化学。
(1)五味调和醋为先,可用 (填标号)测定食醋的酸碱度。
(2)木糖醇和蔗糖的溶解度曲线如下图,30℃时___ (填“能”或“不能”)配得70%的蔗糖溶液;将60℃时95g木糖醇饱和溶液降温到30℃,理论上析出木糖醇的质量是____ g。

(3)硬水有苦涩味,将其通过阳离子交换柱后可转化成软水(如图,阴离子未画出),交换后的水仍然呈电中性。1个Ca2+可以交换出___ 个Na+。欲证明交换后的水是否为软水,可向样品中加入____ ,振荡后观察泡沫的多少。家庭中软化硬水的方法是____ 。

(1)五味调和醋为先,可用 (填标号)测定食醋的酸碱度。
| A.石蕊溶液 | B.pH 试纸 | C.酚酞溶液 |
(2)木糖醇和蔗糖的溶解度曲线如下图,30℃时

(3)硬水有苦涩味,将其通过阳离子交换柱后可转化成软水(如图,阴离子未画出),交换后的水仍然呈电中性。1个Ca2+可以交换出

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】如图是A、B两种固体物质的溶解度曲线。

(1)固体A的溶解度随温度的升高而__________ 填“增大”或“减小”)
(2)t1℃时,A、B两种固体___________ (填“能”或“不能”)配制成溶质质量分数相等的饱和溶液。
(3)t2℃时,将A、B两种固体分别溶解在100g水中形成饱和溶液,所得溶液的质量关系是A_______ B(填“大于”、“小于”或“等于”)。
(4)t2℃时,向100g水中加入55gA固体,发现固体全部溶解,一段时间后又有部分晶体析出。“全部溶解”的原因可能是_______________ 。

(1)固体A的溶解度随温度的升高而
(2)t1℃时,A、B两种固体
(3)t2℃时,将A、B两种固体分别溶解在100g水中形成饱和溶液,所得溶液的质量关系是A
(4)t2℃时,向100g水中加入55gA固体,发现固体全部溶解,一段时间后又有部分晶体析出。“全部溶解”的原因可能是
您最近一年使用:0次



