取100g稀硫酸于烧杯中,将20g镁粉分5次加入烧杯中,实验过程中每次生成氢气的质量如下表所示。
请计算:
(1)表格中m的值为______ 。
(2)稀硫酸中溶质的质量分数为多少。(保留一位小数)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 镁粉的质量/g | 4 | 4 | 4 | 4 | 4 |
| 生成氢气的质量/g | 0.1 | m | 0.1 | 0.1 | 0 |
(1)表格中m的值为
(2)稀硫酸中溶质的质量分数为多少。(保留一位小数)
更新时间:2023-06-03 23:26:25
|
相似题推荐
【推荐1】小王同学为测定某样品中铁的质量分数,做了如下实验(样品中的杂质不与稀硫酸反应),请完成下列分析以及计算:

(1)生成氢气的质量为______ g;
(2)求该样品中铁的质量分数(写出具体的计算过程)。

(1)生成氢气的质量为
(2)求该样品中铁的质量分数(写出具体的计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】黄铜是铜和锌的合金,可用来制造电器零件及日用品。同学们要测定某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质)。称取10g黄铜样品放入烧杯中,量取45mL稀硫酸分三次加入其中,每次充分反应后,测定生成氢气的质量,实验数据如表。请据表回答:
(1)m的数值____ 。
(2)第三次实验结束后,烧杯中所得溶液的溶质为________ 。
(3)此黄铜样品中铜的质量分数是多少?(写出计算过程)
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸的体积(mL) | 15 | 15 | 15 |
| 生成氢气的质量(g) | 0.05 | m | 0.02 |
(2)第三次实验结束后,烧杯中所得溶液的溶质为
(3)此黄铜样品中铜的质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】工业上用N2和H2合成NH3是人类科学技术的一项重大突破。NH3与氰酸(HOCN)反应生成尿素【CO(NH2)2】。
(1)尿素为农作物生长提供的主要营养元素为___________ 。
(2)尿素可用于去除大气污染物中的NO,其化学反应为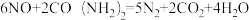 。若去除废气中6gNO,理论上所质量分数为10%的尿素溶液的质量是多少?
。若去除废气中6gNO,理论上所质量分数为10%的尿素溶液的质量是多少?
(1)尿素为农作物生长提供的主要营养元素为
(2)尿素可用于去除大气污染物中的NO,其化学反应为
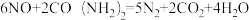 。若去除废气中6gNO,理论上所质量分数为10%的尿素溶液的质量是多少?
。若去除废气中6gNO,理论上所质量分数为10%的尿素溶液的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在实验室里称量一定质量的Na2CO3放入烧杯中,加入一定质量分数的稀硫酸100g,恰好完全反应,共生成2.2g的CO2气体(假设产生的气体完全逸出,水的挥发忽略不计)。已知实验中发生的化学反应:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
(1)Na2CO3样品的质量为_________ g。
(2)100g稀硫酸的溶质质量分数为________ (写出计算过程)。
(3)反应后烧杯中溶液的溶质质量分数为_____ (写出计算过程,结果精确到0.1%)。
(1)Na2CO3样品的质量为
(2)100g稀硫酸的溶质质量分数为
(3)反应后烧杯中溶液的溶质质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】Mg(OH)2 具有广泛的应用,常用菱镁矿制备。研究人员向一定质量的菱镁矿粉中加入过量的稀硫酸,充分溶解后除杂、过滤,得到只含 MgSO4 和 H2SO4 的混合溶液,为确定混合溶液中镁的含量,取 4 份混合溶液各 100g 向每份混合溶液中加入一定质量的 4%NaOH 溶液,得到实验数据如下表所示:
求:100g 混合溶液中含 MgSO4 的质量为多少 g?(要求写出完整计算过程)
| 实验编号 | ① | ② | ③ | ④ |
| NaOH 溶液质量/g | 10.0 | 20.0 | 30.0 | 40.0 |
| Mg(OH)2质量/g | 0.232 | 0.522 | 0.580 | 0.580 |
求:100g 混合溶液中含 MgSO4 的质量为多少 g?(要求写出完整计算过程)
您最近一年使用:0次




