兴趣小组同学向某BaCl2溶液中加入一定量的稀硫酸,二者恰好完全反应,反应前后溶液的总质量变化如图所示。请计算:

(1)反应后生成沉淀的质量为_______ g。
(2)恰好完全反应后所得溶液的溶质质量分数______ 。(结果精确到0.1%)

(1)反应后生成沉淀的质量为
(2)恰好完全反应后所得溶液的溶质质量分数
更新时间:2023-06-28 17:00:11
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室常用溶质质量分数为5%的过氧化氢溶液制取氧气。

(1)某兴趣小组打算用如图所示的整瓶溶液配制溶质质量分数为5%的过氧化氢溶液,需加水______ g。
(2)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是______ 。
(3)为测定该瓶溶液的溶质质量分数,他们取23.2g该溶液放入锥形瓶中并加入一定量的二氧化锰,不同时间电子秤的读数如下表所示(不考虑H2O逸出):
请回答:
①反应生成氧气的总质量为______ g。
②该瓶过氧化氢溶液的溶质质量分数是多少?______ (写出计算过程,结果保留到0.1%)

(1)某兴趣小组打算用如图所示的整瓶溶液配制溶质质量分数为5%的过氧化氢溶液,需加水
(2)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是
(3)为测定该瓶溶液的溶质质量分数,他们取23.2g该溶液放入锥形瓶中并加入一定量的二氧化锰,不同时间电子秤的读数如下表所示(不考虑H2O逸出):
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 锥形瓶+瓶内物质的总质量/g | 320.00 | 318.78 | 317.56 | 316.8 | 316.80 | 316.80 | 316.80 |
①反应生成氧气的总质量为
②该瓶过氧化氢溶液的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某学习小组在实验室中用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应过程中固体质量变化如图所示。
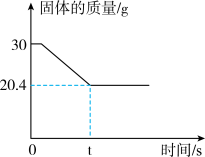
请计算∶
(1)制取氧气的质量是______ g。
(2)原混合物中氯酸钾的质量为______ g。

请计算∶
(1)制取氧气的质量是
(2)原混合物中氯酸钾的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐3】2010年全国两会期间,与会人员领到的会议通知、日程表、便签纸等都是外观与普通纸相似的“石头纸”。“石头纸”的主要原料为碳酸钙,加上少量聚乙烯和胶合剂制成(聚乙烯和胶合剂不溶于水且不与盐酸反应)。
(1)“石头纸”中的碳酸钙属于______ (选填“单质”、“氧化物”、“酸”、“碱”或“盐”)。
(2)为了测定某种“石头纸”中碳酸钙的质量分数,某同学取该种“石头纸”样品l0克,加入100克7.3%的盐酸溶液充分反应。反应后烧杯内剩余物质的总质量为106.48克;经过滤干燥后称得固体残渣质量为2克;
该同学想出甲、乙、丙三种计算方案:
甲:根据“反应后烧杯内剩余物质的总质量106 .48克,可知二氧化碳的质量,……”求解;
乙:根据“反应后经过滤干燥后称得固体残渣的质量2克,可知样品中碳酸钙的质量, ……”求解;
丙:根据“100克7.3%的盐酸溶液,可知参加反应的氯化氢质量,……”求解。
以上方案中,不正确的是___________________ 。
(3)根据上述的某个正确方案计算该“石头纸”中碳酸钙的质量分数。_______________
(1)“石头纸”中的碳酸钙属于
(2)为了测定某种“石头纸”中碳酸钙的质量分数,某同学取该种“石头纸”样品l0克,加入100克7.3%的盐酸溶液充分反应。反应后烧杯内剩余物质的总质量为106.48克;经过滤干燥后称得固体残渣质量为2克;
该同学想出甲、乙、丙三种计算方案:
甲:根据“反应后烧杯内剩余物质的总质量106 .48克,可知二氧化碳的质量,……”求解;
乙:根据“反应后经过滤干燥后称得固体残渣的质量2克,可知样品中碳酸钙的质量, ……”求解;
丙:根据“100克7.3%的盐酸溶液,可知参加反应的氯化氢质量,……”求解。
以上方案中,不正确的是
(3)根据上述的某个正确方案计算该“石头纸”中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】我市某玻璃厂排放的废水中含有碳酸钠,易造成环境污染。化学兴趣小组根据该厂设计的废水处理方案进行了如下实验:取过滤后的水样100 g,逐滴加入稀盐酸至恰好不再产生气体为止。反应过程中生成气体与所加稀盐酸的质量关系如图所示。请回答下列问题(不考虑水样中杂质的影响)。

(1)反应生成CO2气体的质量是______________。
(2)100 g水样中碳酸钠的质量是______________?(写出计算过程)
(3)加入稀盐酸的质量为a g时,溶液中的钠元素的质量是__________g。

(1)反应生成CO2气体的质量是______________。
(2)100 g水样中碳酸钠的质量是______________?(写出计算过程)
(3)加入稀盐酸的质量为a g时,溶液中的钠元素的质量是__________g。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】煤燃烧能产生大量污染气体,严重破坏环境和危害生态健康。利用尿素溶液能吸收污染气体中的二氧化氮,其反应方程式为: 。现用1000g溶质质量分数为24%的过量尿素溶液,充分吸收138g二氧化氮气体,请回答:
。现用1000g溶质质量分数为24%的过量尿素溶液,充分吸收138g二氧化氮气体,请回答:
(1)尿素中氧、氢元素的质量比为__________ ,反应中导致酸雨的气体是__________ (填化学式);
(2)充分反应后,剩余溶液溶质质量分数为多少?(不考虑气体溶于水或与水反应形成的溶质,结果保留0.1%)
(3)要使剩余溶液恢复到最初浓度,需要加入多少尿素充分溶解。(保留到0.1g)。
 。现用1000g溶质质量分数为24%的过量尿素溶液,充分吸收138g二氧化氮气体,请回答:
。现用1000g溶质质量分数为24%的过量尿素溶液,充分吸收138g二氧化氮气体,请回答:(1)尿素中氧、氢元素的质量比为
(2)充分反应后,剩余溶液溶质质量分数为多少?(不考虑气体溶于水或与水反应形成的溶质,结果保留0.1%)
(3)要使剩余溶液恢复到最初浓度,需要加入多少尿素充分溶解。(保留到0.1g)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现有NaOH和Na2CO3的固体混合物10g,将其全部放入一洁净的烧杯中,然后加入足量蒸馏水,搅拌,使固体完全溶解。再向烧杯中逐滴加入溶质质量分数为10%的BaC12溶液,反应过程中产生沉淀的质量写所滴入BaC12溶液的质量关系如下图所示。试回答:

(1)当滴入BaCl2溶液___________ g时,恰好完全反应;
(2)当滴入BaCl2溶液150g时,烧杯中溶液里存在的酸根阴离子是_____________ (填离子符号);
(3)试通过计算,求10g该固体混合物中Na2CO3的质量______________ 。(写出计算过程,结果精确至0.1g)

(1)当滴入BaCl2溶液
(2)当滴入BaCl2溶液150g时,烧杯中溶液里存在的酸根阴离子是
(3)试通过计算,求10g该固体混合物中Na2CO3的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】溶液对动植物的生理活动和人类的生产,科研活动具有重要意义。
(1)室温下,某实验小组欲配制100g溶质质量分数为10%的Na2CO3溶液,按以下步骤操作。
①计算:需Na2CO3_______ g,水________ ml(室温时,水的密度约为1.0g/mL)。
②称量:称量所需的碳酸钠粉末时,发现托盘天平的指针偏左,此时应_____ (填写序号A、B、C之一)。
A.调节天平平衡螺母
B.增加适量Na2CO3
C.减少适量Na2CO3
③配制溶液:用量筒量取所需的水,倒入盛有Na2CO3的烧杯中,用玻璃棒搅拌、搅拌的目的是_____________ 。
(2)实验小组的同学把上述配制的Na2CO3溶液,逐滴加入到盛有100g质量分数7.3%的稀盐酸的烧杯中,生成气体的质量与加入Na2CO3溶液的质量关系如下图所示。请根据题意回答下列问题:

①当滴入Na2CO3溶液53g时(即图中A点),溶液显酸性,此时烧杯中溶液里含有的溶质为________ 和_________ 。
②当滴入10%的Na2CO3溶液106g时(即图中B点),恰好完全反应,试通过计算,求生成气体的质量。________
(1)室温下,某实验小组欲配制100g溶质质量分数为10%的Na2CO3溶液,按以下步骤操作。
①计算:需Na2CO3
②称量:称量所需的碳酸钠粉末时,发现托盘天平的指针偏左,此时应
A.调节天平平衡螺母
B.增加适量Na2CO3
C.减少适量Na2CO3
③配制溶液:用量筒量取所需的水,倒入盛有Na2CO3的烧杯中,用玻璃棒搅拌、搅拌的目的是
(2)实验小组的同学把上述配制的Na2CO3溶液,逐滴加入到盛有100g质量分数7.3%的稀盐酸的烧杯中,生成气体的质量与加入Na2CO3溶液的质量关系如下图所示。请根据题意回答下列问题:

①当滴入Na2CO3溶液53g时(即图中A点),溶液显酸性,此时烧杯中溶液里含有的溶质为
②当滴入10%的Na2CO3溶液106g时(即图中B点),恰好完全反应,试通过计算,求生成气体的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示。

回答下列问题:
(1)从图中看出生成沉淀的最大质量是________g。
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原因是________。
(3)如图,当滴加碳酸钠溶液质量为5g时,溶液中的溶质是_________(写化学式)
(4)计算原滤液中氯化钙的质量分数为_______________。(请写出计算过程)

回答下列问题:
(1)从图中看出生成沉淀的最大质量是________g。
(2)开始加入碳酸钠溶液至10g时,还没有沉淀的原因是________。
(3)如图,当滴加碳酸钠溶液质量为5g时,溶液中的溶质是_________(写化学式)
(4)计算原滤液中氯化钙的质量分数为_______________。(请写出计算过程)
您最近一年使用:0次




