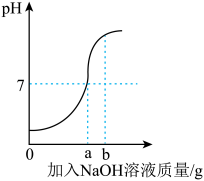
常温下,向盛有100.0g氢氧化钠溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计测定反应过程中溶液的pH,所得数据如表:
(1)加入80.0g稀盐酸时,烧杯中溶液含有的阴离子有______ 种;
(2)当氢氧化钠溶液与稀盐酸恰好完全反应时,所得溶液的pH为_____ ;
(3)请计算该氢氧化钠溶液中溶质的质量分数。
【解】设:氢氧化钠溶液中溶质的质量是x。
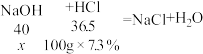
列出比例式____
求解:x=8.0g
氢氧化钠溶液中溶质的质量分数是______ (列式并计算结果)
答:氢氧化钠溶液中溶质的质量分数是略。
| 加入稀盐酸的质量/g | 60.0 | 80.0 | 100.0 | 120.0 |
| 烧杯中溶液的pH | 13.7 | 13.3 | 7.0 | 0.7 |
(2)当氢氧化钠溶液与稀盐酸恰好完全反应时,所得溶液的pH为
(3)请计算该氢氧化钠溶液中溶质的质量分数。
【解】设:氢氧化钠溶液中溶质的质量是x。
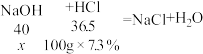
列出比例式
求解:x=8.0g
氢氧化钠溶液中溶质的质量分数是
答:氢氧化钠溶液中溶质的质量分数是略。
更新时间:2023-07-19 09:42:05
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在实验室将25克石灰石样品(杂质不参加反应,也不溶于水)放入盛有100克溶质质量分数为14.6%的稀盐酸中,恰好完全反应。求:反应后所得溶液的溶质质量分数。(计算结果精确到1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某兴趣小组同学为了测定大理石中碳酸钙的质量分数,取一定量的大理石样品放入烧杯中,将50g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下,请根据信息回答下列问题:
(1)m的值分别为___________,该大理石样品中碳酸钙的质量分数为______________。
(2)计算所用稀盐酸溶质的质量分数。(写出计算过程,结果精确到0.1%)
(3)向上述反应后的滤液中滴加碳酸钠溶液。(已知氯化钙溶液呈中性)在溶液中插入pH传感器,测得pH变化曲线如图所示,下列有关说法不正确的是___________(填字母序号)。
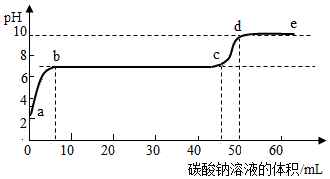
A、开始时溶液pH=2是因为滤液中还有盐酸
B、c点溶液中含有的溶质是Na2CO3和NaCl
C、c点表示此时溶液呈中性
D、ab段表示随着Na2CO3溶液的滴入,CaCO3沉淀的质量逐渐增加
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
| 剩余固体质量/g | 9.0 | 7.0 | m | 3.0 | 1.1 |
(1)m的值分别为___________,该大理石样品中碳酸钙的质量分数为______________。
(2)计算所用稀盐酸溶质的质量分数。(写出计算过程,结果精确到0.1%)
(3)向上述反应后的滤液中滴加碳酸钠溶液。(已知氯化钙溶液呈中性)在溶液中插入pH传感器,测得pH变化曲线如图所示,下列有关说法不正确的是___________(填字母序号)。

A、开始时溶液pH=2是因为滤液中还有盐酸
B、c点溶液中含有的溶质是Na2CO3和NaCl
C、c点表示此时溶液呈中性
D、ab段表示随着Na2CO3溶液的滴入,CaCO3沉淀的质量逐渐增加
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】取 和
和 的混合物
的混合物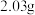 ,放入烧杯中,加水溶解配制成
,放入烧杯中,加水溶解配制成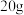 的溶液,逐滴滴入溶质质量分数为
的溶液,逐滴滴入溶质质量分数为 的稀盐酸,溶液的
的稀盐酸,溶液的 与滴入稀盐酸质量的关系如图所示。
与滴入稀盐酸质量的关系如图所示。
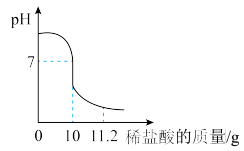
(1)当滴入稀盐酸的质量为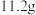 时,溶液中的溶质是
时,溶液中的溶质是___________  填化学式
填化学式 。
。
(2)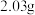 混合物中
混合物中 的质量为
的质量为___________  。
。
(3)求当滴入 稀盐酸时,反应后所得溶液中溶质的质量分数。
稀盐酸时,反应后所得溶液中溶质的质量分数。
 和
和 的混合物
的混合物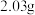 ,放入烧杯中,加水溶解配制成
,放入烧杯中,加水溶解配制成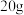 的溶液,逐滴滴入溶质质量分数为
的溶液,逐滴滴入溶质质量分数为 的稀盐酸,溶液的
的稀盐酸,溶液的 与滴入稀盐酸质量的关系如图所示。
与滴入稀盐酸质量的关系如图所示。
(1)当滴入稀盐酸的质量为
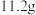 时,溶液中的溶质是
时,溶液中的溶质是 填化学式
填化学式 。
。(2)
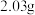 混合物中
混合物中 的质量为
的质量为 。
。(3)求当滴入
 稀盐酸时,反应后所得溶液中溶质的质量分数。
稀盐酸时,反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】我国第一艘国产航母的许多电子元件使用了黄铜(假设合金中仅含铜,锌),兴趣小组同学向盛有30g黄铜样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如图所示,计算:
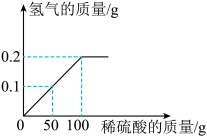
(1)充分反应后生成氢气的质量为_____g
(2)合金样品中铜的质量。_____
(3)恰好完全反应时,所得溶液中溶质的质量分数。_____ (结果保留到0.1%)

(1)充分反应后生成氢气的质量为_____g
(2)合金样品中铜的质量。_____
(3)恰好完全反应时,所得溶液中溶质的质量分数。_____ (结果保留到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为了测定混有少量氯化钠的碳酸氢钠(NaHCO3)固体的质量分数。现进行如下实验:向盛有9.6g该样品的烧杯中加入94.8g盐酸,恰好完全反应。反应过程用精密仪器测得烧杯和药品的质量与反应时间的数据记录如下:
(1)完全反应后生成气体的质量是 g;
(2)样品中NaHCO3的质量分数是 ;
(3)反应后溶液中溶质质量分数是多少? (写出计算过程, 结果保留一位小数)
| 反应时间 | T0 | T1 | T2 | T3 | T4 | T5 |
| 烧杯和药品的质量/g | 210 | 207.8 | 206.6 | 205.9 | 205.6 | 205.6 |
(1)完全反应后生成气体的质量是 g;
(2)样品中NaHCO3的质量分数是 ;
(3)反应后溶液中溶质质量分数是多少? (写出计算过程, 结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
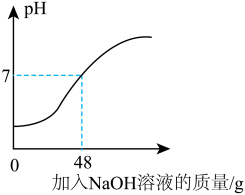
【推荐1】为测定某瓶标签受损的硫酸的溶质质量分数,某同学取10g该硫酸样品于烧杯中,逐滴滴加溶质质量分数为5%的NaOH溶液,同时不断搅拌,用pH传感器测定反应过程中溶液的pH变化如图所示。请计算该硫酸样品的溶质质量分数。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】预防新型冠状病毒,需要掌握科学的消毒方法。专家辟谣“熏醋”并不能杀灭新型冠状病毒。“熏醋”主要使用的是食醋,食醋中的醋酸含量约为3.5%~5%,病毒可以在这种环境下生存。某化学兴趣学习小组为测定市场出售的食醋总酸量(国家规定食醋中总酸量3.5g/100mL~5g/100mL),拟配制一定质量分数的氢氧化钠溶液,然后进行测定。请你参与该小组的实验研究,并回答相关问题。
(1)配制100g质量分数为5%的氢氧化钠溶液需要水_________ mL(水的密度为1g/cm3)。量取水时若仰视读数,所配得的溶液质量分数会_________ (填“不变”或“偏大”或“偏小”)。
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的方程式为: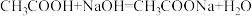 ,现有食醋500mL,甲同学从中取出10mL食醋,加入5%的氢氧化钠溶液5.0g,恰好完全反应。请通过计算判断该食醋是否合格?(写出计算过程)
,现有食醋500mL,甲同学从中取出10mL食醋,加入5%的氢氧化钠溶液5.0g,恰好完全反应。请通过计算判断该食醋是否合格?(写出计算过程)
(1)配制100g质量分数为5%的氢氧化钠溶液需要水
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的方程式为:
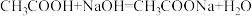 ,现有食醋500mL,甲同学从中取出10mL食醋,加入5%的氢氧化钠溶液5.0g,恰好完全反应。请通过计算判断该食醋是否合格?(写出计算过程)
,现有食醋500mL,甲同学从中取出10mL食醋,加入5%的氢氧化钠溶液5.0g,恰好完全反应。请通过计算判断该食醋是否合格?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
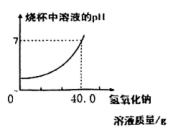
【推荐1】为了测定稀硫酸的中溶质的质量分数,化学兴趣小组同学取50.0g稀硫酸于烧杯中,逐滴滴入质量分数为20.0%的氢氧化钠溶液,所得溶液pH与加入氢氧化钠溶液质量的变化关系如图所示。
(1)实验过程中溶液的pH值_______ (填“增大”、“减小”或“不变”)。
(2)计算稀硫酸中溶质的质量分数(精确到0.1%)。
(1)实验过程中溶液的pH值
(2)计算稀硫酸中溶质的质量分数(精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
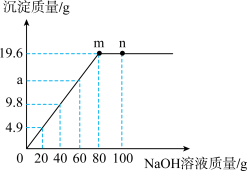
【推荐2】在实验室里,某化学兴趣小组的同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中测得实验数据如图所示:
请问:
(1)图中a的值为_________ 。
(2)n点溶液的pH_________ 7(填“>”或“<”或“=”);
(3)求恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)

请问:
(1)图中a的值为
(2)n点溶液的pH
(3)求恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为测定某氯化钙溶液的溶质质量分数,取该溶液 ,逐滴滴入10%的碳酸钠溶液,随着碳酸钠溶液的滴入,一段时间内溶液中溶质种类如下表:
,逐滴滴入10%的碳酸钠溶液,随着碳酸钠溶液的滴入,一段时间内溶液中溶质种类如下表:
请分析并计算:
(1)③溶液的
______ (填“<”、“>”或“=”)7。
(2)计算氯化钙溶液的溶质质量分数。
 ,逐滴滴入10%的碳酸钠溶液,随着碳酸钠溶液的滴入,一段时间内溶液中溶质种类如下表:
,逐滴滴入10%的碳酸钠溶液,随着碳酸钠溶液的滴入,一段时间内溶液中溶质种类如下表:| 先后次序 | 碳酸钠溶液的质量/g | 溶液中溶质的种类 |
| ① | 105 | 2 |
| ② | 106 | 1 |
| ③ | 110 | 2 |
(1)③溶液的

(2)计算氯化钙溶液的溶质质量分数。
您最近一年使用:0次