水是人类赖以生存和发展不可缺少的重要物质资源之一,请你用水的知识回答下列问题:
(1)下列物质属于纯净物的是___________(填字母)。
(2)3月22日是“世界水日”,自来水厂净水过程中不涉及的步骤是___________(填字母)。
(3)如图是KNO3和NH4Cl的溶解度曲线,根据图示填空
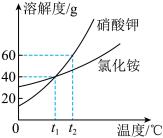
①将NH4Cl的不饱和溶液变成饱和溶液,方法有___________ (填一条即可)。
②t2℃时,KNO3饱和溶液中溶质的质量分数是___________ 。
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是___________ (填“KNO3”或“NH4Cl”)溶液。
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。
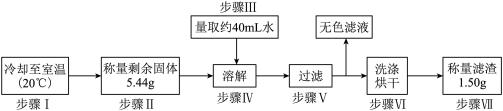
(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为___________ g。
②步骤Ⅲ中水量约为40mL而不是30mL的原因___________ 。
(1)下列物质属于纯净物的是___________(填字母)。
| A.海水 | B.冰水混合物 | C.矿泉水 | D.自来水 |
| A.沉淀 | B.蒸馏 | C.吸附 | D.消毒 |

①将NH4Cl的不饱和溶液变成饱和溶液,方法有
②t2℃时,KNO3饱和溶液中溶质的质量分数是
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。

(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为
②步骤Ⅲ中水量约为40mL而不是30mL的原因
更新时间:2023-07-19 08:45:53
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】起亚汽车出没在响水的大街小巷,而汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请根据所学知识按要求答题
(1)钢铁车壳表面喷漆不仅美观,而且可有效防止与空气中的氧气和_____ (填物质名称)接触而生锈
(2)铝的活动性比较强,但在生活中常在铁的表面涂上铝粉,其原因是_____
(3)小王同学从起亚汽车厂整理处一包铜和另一种金属X的混合物(X可能是Ag或Fe),取少量混合物加入足量的稀硫酸有气泡产生,则X不可能是_____ .另取一定量的原混合物投入到一定量的AgNO3溶液中,充分反应后,得到固体和溶液,则所得溶液中一定含有的溶质是_____ (填化学式)
(4)为测定某汽车厂Cu﹣Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物的质量为49.9g,计算原合金中铜的质量分数是__________ .
(1)钢铁车壳表面喷漆不仅美观,而且可有效防止与空气中的氧气和
(2)铝的活动性比较强,但在生活中常在铁的表面涂上铝粉,其原因是
(3)小王同学从起亚汽车厂整理处一包铜和另一种金属X的混合物(X可能是Ag或Fe),取少量混合物加入足量的稀硫酸有气泡产生,则X不可能是
(4)为测定某汽车厂Cu﹣Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物的质量为49.9g,计算原合金中铜的质量分数是
您最近一年使用:0次
【推荐2】钙是维持人体正常功能所必需的元素。
(1)人体缺钙有可能导致_____ (选填序号)。
a、骨质疏松症b、贫血症c、佝偻病d、发育停滞、智力低下
(2)某钙片的主要成分是碳酸钙,兴趣小组同学想通过实验测定该钙片中碳酸钙的质量分数。(钙片中的其他成分不溶于水,且不与稀盐酸反应)
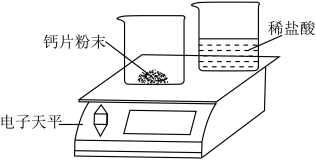
①取该钙片 10 克,研磨成粉末,置于大烧杯内,并在小烧杯中盛放足量稀盐酸,将两个烧杯放在电子天平上,记录天平读数。
②将稀盐酸倒入钙片粉末中,若观察到_____ 的现象,证明反应已经结束。
实验记录如下,试计算该品牌钙片中碳酸钙的质量分数_____ 。
(1)人体缺钙有可能导致
a、骨质疏松症b、贫血症c、佝偻病d、发育停滞、智力低下
(2)某钙片的主要成分是碳酸钙,兴趣小组同学想通过实验测定该钙片中碳酸钙的质量分数。(钙片中的其他成分不溶于水,且不与稀盐酸反应)

①取该钙片 10 克,研磨成粉末,置于大烧杯内,并在小烧杯中盛放足量稀盐酸,将两个烧杯放在电子天平上,记录天平读数。
②将稀盐酸倒入钙片粉末中,若观察到
实验记录如下,试计算该品牌钙片中碳酸钙的质量分数
| 实验进程 | 起始(/g) | 最终(/g) |
| 电子天平读数 | 173.20 | 171.00 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】“绿色化学”是化工生产中的重要理念。利用尿素工厂废气和磷肥工厂废渣(液)联合生产氮肥硫酸铵[(NH4)2SO4]的工艺流程如下:_______ 。
(2)沉淀池中发生反应的化学方程式为_______ 。
(3)该工艺流程中体现“绿色化学”理念的设计有_______ (答一点即可)。
(4)消耗17gNH3理论上制得(NH4)2SO4的质量为_______ g。
(5)施肥时,为了不降低肥效,下列物质中不宜与硫酸铵混合使用的是_____。

(2)沉淀池中发生反应的化学方程式为
(3)该工艺流程中体现“绿色化学”理念的设计有
(4)消耗17gNH3理论上制得(NH4)2SO4的质量为
(5)施肥时,为了不降低肥效,下列物质中不宜与硫酸铵混合使用的是_____。
| A.熟石灰 | B.氯化铵 | C.硫酸钾 | D.草木灰(含碳酸钾) |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ:A、B、C、D、E五种物质都是已学化学内容中涉及到的常见物质,其转化关系如下图所示:
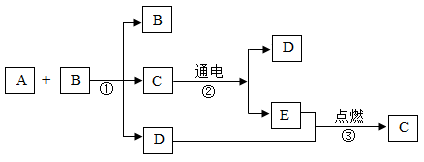
(1)写出物质A的化学式:______ 。
(2)物质E的一种用途______ 反应③的实验现象是______ 。
(3)从微观的角度:分析A与C化学性质不同的原因是______ 。
(4)写出反应①的文字表达式______ 。
Ⅱ:小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如图所示。请回答以下问题:
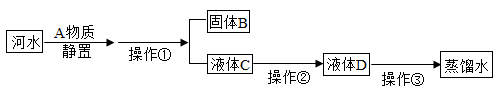
(5)最常用的A物质是______ ,操作①的名称是______ ,该操作中用到的玻璃仪器有______ 。(回答一个即可)
(6)操作②主要是利用物质的______ (选填“物理”或“化学”)性质。

(1)写出物质A的化学式:
(2)物质E的一种用途
(3)从微观的角度:分析A与C化学性质不同的原因是
(4)写出反应①的文字表达式
Ⅱ:小刚收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如图所示。请回答以下问题:

(5)最常用的A物质是
(6)操作②主要是利用物质的
您最近一年使用:0次
【推荐2】“天宫课堂”由中国航天员担任“太空教师”,以青少年为主要对象,采取天地协同互动方式进行太空授课。课堂上演示了许多有趣的实验。
(1)水球光学实验使用了“人造空气”,“人造空气”中氧气、氮气、二氧化碳的体积分数分别为 21%、78%、0.7%。上述气体中可供给呼吸的是__________ 。
(2)太空“冰雪”实验:从一个袋子中缓缓挤出一个圆圆的液体球,随后用沾有晶体粉末的小棒触碰一下,液体球迅速“结冰”,成为一个通体洁白的“冰球”悬浮在空中。液体球“结冰”实际是溶液中析出了晶体。无论降温结晶还是蒸发结晶,饱和溶液析出晶体后,一定减小的是 。(填字母序号)
(3)地面分课堂的同学提出问题:“在空间站里,氧气和二氧化碳是怎么循环的呢?”下图展示了空间站中氧气和二氧化碳的循环流程。

i .在氧气生成系统中,运用电解水的方法制氧气,反应的化学方程式是__________ ,每位航天员每天大概会消耗 25 mol 氧气,需要电解_________ g 水。
ii .在萨巴蒂尔反应系统中,发生的反应为 ,则 X 的化学式为
,则 X 的化学式为__________ ,构成 X 的微粒是__________ (填名称)。
(4)机场、车站等公共场所设有许多直饮水机,能将自来水进一步净化处理得到可直接饮用水,其处理水的过程如下图所示。紫外线灯管照射的作用是__________ ,净化后的直接饮用水属于__________ (填“纯净物”或“混合物”)。

(1)水球光学实验使用了“人造空气”,“人造空气”中氧气、氮气、二氧化碳的体积分数分别为 21%、78%、0.7%。上述气体中可供给呼吸的是
(2)太空“冰雪”实验:从一个袋子中缓缓挤出一个圆圆的液体球,随后用沾有晶体粉末的小棒触碰一下,液体球迅速“结冰”,成为一个通体洁白的“冰球”悬浮在空中。液体球“结冰”实际是溶液中析出了晶体。无论降温结晶还是蒸发结晶,饱和溶液析出晶体后,一定减小的是 。(填字母序号)
| A.溶质质量 | B.溶剂质量 | C.溶质的质量分数 |
(3)地面分课堂的同学提出问题:“在空间站里,氧气和二氧化碳是怎么循环的呢?”下图展示了空间站中氧气和二氧化碳的循环流程。

i .在氧气生成系统中,运用电解水的方法制氧气,反应的化学方程式是
ii .在萨巴蒂尔反应系统中,发生的反应为
 ,则 X 的化学式为
,则 X 的化学式为(4)机场、车站等公共场所设有许多直饮水机,能将自来水进一步净化处理得到可直接饮用水,其处理水的过程如下图所示。紫外线灯管照射的作用是

您最近一年使用:0次
【推荐3】(一)从化学视角回答下列生活、生产问题。
(1)氮气充入食品包装袋防腐,是因为_______ 。
(2)切洋葱时人会流眼泪,是因为________ 从分子的角度解释)。
(3)小明晚上切完西瓜后将刀放在菜板上,第二天发现刀生锈了。刀生锈的原因是铁与空气中的____ 发生了反应。
(4)目前人们利用最多的能源是煤、_______ 和天然气等化石燃料。2019年12月2日,中俄东线天然气管道投产通气,未来30年俄罗斯将向中国供应1万亿立方米天然气。天然气是_______ (填“纯净物”或“混合物”),其充分燃烧的主要化学方程式为_______ 。关闭燃气开关灭火,运用的原理是_______ 。
(二)请用所学知识回答下列问题:

(1)我国的北斗导航卫星系统采用铷原子钟,提供精确时间。从图A可知,铷原子的质子数为_______ ,其中子数和质子数之差约为_______ 。
(2)B~E是四种粒子的结构示意图,D在化学反应中易_______ 电子(填“得”或“失”);其中与E化学性质相似的粒子是_______ (填字母)。
(3)元素D和E形成的化合物的化学式为_______ 。
(三)水很容易透过细胞膜被吸收,使人体器官中的乳酸脱氢酶活力增强,从而有效提高人体的免疫力以抵抗病毒。
(1)下图是自来水厂净化水的主要步骤。有关说法错误的是_______ (填字母)。

A步骤①中可加入明矾作絮凝剂B X试剂可以是活性炭
C步骤④的作用是消毒杀菌D净化后的水为纯净物
(2)ClO2被称为“第四代”饮用水杀虫剂,因其高效、无污染而被广泛使用。北京永利科技有限公司用电解法生产ClO2.其反应原理为:4HClO3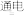 4ClO2+O2↑+2X,其中X的化学式
4ClO2+O2↑+2X,其中X的化学式_______ 。
(3)用如图所示装置进行电解水的实验,电解时,在水中加入少量_______ 能增强导电性;b玻璃管中收集到的气体名称是_______ 。

(4)保护水资源,人人有责。请你写出水体污染源之一_______ 。
(四)75%乙醇(俗称酒精)溶液做消毒剂可以有效灭活新型冠状病毒。
(1)装运酒精的包装箱应贴的图标是_______ (填字母)。

(2)居家使用医用酒精消毒时,采用喷洒的方式比在物体表面擦拭更易引起火灾的原因是_______ ,请写出酒精燃烧的化学方程式_______ 。
(3)工业酒精不同于医用酒精,含有96%乙醇和1%甲醇,而甲醇有毒,若用于皮肤消毒会被人体吸收,严重可导致失明甚至死亡。但甲醇并非百害而无一利,由甲醇制乙烯气体是我国重要的化工技术。下图是该反应的微观示意图,其化学方程式为____ 。

(1)氮气充入食品包装袋防腐,是因为
(2)切洋葱时人会流眼泪,是因为
(3)小明晚上切完西瓜后将刀放在菜板上,第二天发现刀生锈了。刀生锈的原因是铁与空气中的
(4)目前人们利用最多的能源是煤、
(二)请用所学知识回答下列问题:

(1)我国的北斗导航卫星系统采用铷原子钟,提供精确时间。从图A可知,铷原子的质子数为
(2)B~E是四种粒子的结构示意图,D在化学反应中易
(3)元素D和E形成的化合物的化学式为
(三)水很容易透过细胞膜被吸收,使人体器官中的乳酸脱氢酶活力增强,从而有效提高人体的免疫力以抵抗病毒。
(1)下图是自来水厂净化水的主要步骤。有关说法错误的是

A步骤①中可加入明矾作絮凝剂B X试剂可以是活性炭
C步骤④的作用是消毒杀菌D净化后的水为纯净物
(2)ClO2被称为“第四代”饮用水杀虫剂,因其高效、无污染而被广泛使用。北京永利科技有限公司用电解法生产ClO2.其反应原理为:4HClO3
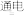 4ClO2+O2↑+2X,其中X的化学式
4ClO2+O2↑+2X,其中X的化学式(3)用如图所示装置进行电解水的实验,电解时,在水中加入少量

(4)保护水资源,人人有责。请你写出水体污染源之一
(四)75%乙醇(俗称酒精)溶液做消毒剂可以有效灭活新型冠状病毒。
(1)装运酒精的包装箱应贴的图标是

(2)居家使用医用酒精消毒时,采用喷洒的方式比在物体表面擦拭更易引起火灾的原因是
(3)工业酒精不同于医用酒精,含有96%乙醇和1%甲醇,而甲醇有毒,若用于皮肤消毒会被人体吸收,严重可导致失明甚至死亡。但甲醇并非百害而无一利,由甲醇制乙烯气体是我国重要的化工技术。下图是该反应的微观示意图,其化学方程式为

您最近一年使用:0次
【推荐1】酸、碱、盐是重要的化合物。
(1)打开盛有浓盐酸的试剂瓶瓶盖后,瓶口出现白雾,说明浓盐酸具有 (填标号)。
(2)氯碱工业指的是利用电解饱和食盐水制得氢氧化钠、氢气和氯气,并以它们为原料生产一系列化工产品。次氯酸钠(NaClO)是氯碱工业的产品之一、氯化钠、次氯酸钠固体的溶解度曲线如图。_____ (填“增大”“减小”或“不变”)。
②30℃时,溶解度:NaClO_____ NaCl(填“>”“<”或“=”)。
③下列关于氢氧化钠用途的叙述,错误的是_____ (填标号)
A.治疗胃酸过多 B.制取肥皂
C.制作炉具清洁剂D.作某些气体的干燥剂
(3)中和反应是重要的化学反应。
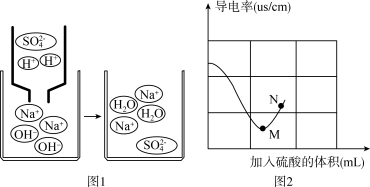
①图1是氢氧化钠溶液和稀硫酸反应的示意图,该反应的实质是______ 。______ ,N点溶质为K2SO4和______ (填化学式)。
(1)打开盛有浓盐酸的试剂瓶瓶盖后,瓶口出现白雾,说明浓盐酸具有 (填标号)。
| A.还原性 |
| B.酸性 |
| C.挥发性 |
| D.腐蚀性 |
(2)氯碱工业指的是利用电解饱和食盐水制得氢氧化钠、氢气和氯气,并以它们为原料生产一系列化工产品。次氯酸钠(NaClO)是氯碱工业的产品之一、氯化钠、次氯酸钠固体的溶解度曲线如图。
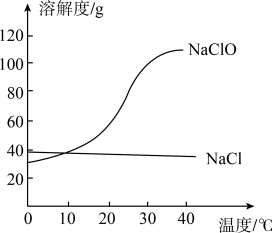
②30℃时,溶解度:NaClO
③下列关于氢氧化钠用途的叙述,错误的是
A.治疗胃酸过多 B.制取肥皂
C.制作炉具清洁剂D.作某些气体的干燥剂
(3)中和反应是重要的化学反应。
①图1是氢氧化钠溶液和稀硫酸反应的示意图,该反应的实质是
您最近一年使用:0次
【推荐2】海水是一种宝贵的资源。
(1)海水晒盐提取食盐后留下的母液叫卤水,卤水中除含NaCl还含有KCl、MgCl2、MgSO4等物质。它们的溶解度曲线如图所示。下列说法正确的是_____________。
(2)海上航行缺乏饮用水时可采用如图装置获得淡水。_____________ g。
(3)某同学往模拟海水(含NaCl、KCl、MgCl2、MgSO4)中加入NaOH溶液,有白色沉淀生成,请写出反应的化学方程式_____________ (写一个)
(1)海水晒盐提取食盐后留下的母液叫卤水,卤水中除含NaCl还含有KCl、MgCl2、MgSO4等物质。它们的溶解度曲线如图所示。下列说法正确的是_____________。

| A.0℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgCl2 |
| B.三种物质的溶解度都随温度升高而不断增大 |
| C.t3℃时将agMgCl2固体加入100g水,可得(100+a)g溶液 |
| D.t1°C时KCl和MgSO4的饱和溶液一定含相同质量的溶质 |
(2)海上航行缺乏饮用水时可采用如图装置获得淡水。

(3)某同学往模拟海水(含NaCl、KCl、MgCl2、MgSO4)中加入NaOH溶液,有白色沉淀生成,请写出反应的化学方程式
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】下图是甲、乙、丙三种固体物质的溶解度曲线,据图回答下列问题。
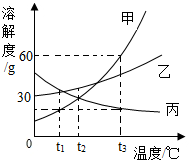
(1)0℃时,乙物质的溶解度是___________ 。
(2)除去甲中混有的氯化钠,可采用的方法是__________ 。
(3)t3℃时,将甲、丙两物质的饱和溶液同时降温至___________ ℃,它们溶质的质量分数相等。
(4)下列说法正确的是 。

(1)0℃时,乙物质的溶解度是
(2)除去甲中混有的氯化钠,可采用的方法是
(3)t3℃时,将甲、丙两物质的饱和溶液同时降温至
(4)下列说法正确的是 。
| A.向t2℃时甲的饱和溶液m1g和丙的饱和溶液m2g中分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等 |
| B.t2℃时,分别向甲和乙的饱和溶液中加入等质量的水,所得溶液的质量分数可能相等 |
| C.t3℃时,向50.0g质量分数为30%的甲溶液中加入10.0g固体甲,所得溶液中溶质的质量分数为37.5% |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】溶液是生产生活中常见的物质,依据相关信息回答问题。资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
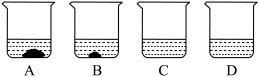
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
①(填字母序号)______ 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为_________ g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是_____ (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
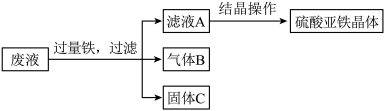
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:
请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤______ ;
②流程中生成气体B的反应的化学方程式是:__________ 。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。

①(填字母序号)
②使B烧杯的溶液升温至50℃时,溶液的质量为
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:

请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤
②流程中生成气体B的反应的化学方程式是:
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】如表是KNO3和NH4Cl分别在不同温度时的溶解度。
(1)根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:下列说法错误的是______。(填序号)。

(2)60℃时,c点的KNO3溶液属于______ (填“饱和”或“不饱和”)状态。欲将处于c点的KNO3溶液转变为b点,可以采取______ (填“降低温度”或“增加溶质”)的措施。
(3)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,能析出NH4Cl晶体的质量为______ g。
(4)将t1℃时M、N的饱和溶液,均升温到60℃,所得两溶液的溶质质量分数的大小关系是M______ N(填“>”、“<”或“=”)。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
(1)根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:下列说法错误的是______。(填序号)。

| A.二者的溶解度均随温度升高而增大 |
| B.曲线M为KNO3的溶解度曲线 |
| C.a点对应的温度在30℃与40℃之间 |
| D.a点对应的溶解度在37.2g与41.4g之间 |
(2)60℃时,c点的KNO3溶液属于
(3)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,能析出NH4Cl晶体的质量为
(4)将t1℃时M、N的饱和溶液,均升温到60℃,所得两溶液的溶质质量分数的大小关系是M
您最近一年使用:0次
【推荐3】NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如表所示。
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高至____________ (填“增大”或“减小”);除去碳酸钠中混有少量氯化钠的方法是_____________ ;
(2)20℃时,饱和食盐水溶质的质量分数为___________ (计算结果精确到0.1%)。
(3)常温下,将5gNaCl粉末放入10mL乙醇中,振荡时形成的是_________ (填“溶液”、“悬浊液”或“乳浊液”)。
(4)为证明CO2能与NaOH反应生成Na2CO3,小明同学将CO2通入饱和NaOH的乙醇溶液中,请推测实验可观察到的现象___________ ,推测依据是_____________________ 。
表1 NaOH、Na2CO3、NaCl分别在水中的溶解度(S/g)
| t/℃ | NaOH | Na2CO3 | NaCl |
| 0 | 42 | 7.1 | 35.7 |
| 10 | 51 | 12.2 | 35.8 |
| 20 | 109 | 21.8 | 36.0 |
| 30 | 119 | 39.7 | 36.3 |
表2 常温下,NaOH、Na2CO3、NaCl分别在乙醇中的溶解度(S/g)
| NaOH | Na2CO3 | NaCl |
| 17.3 | <0.01 | 0.1 |
根据表1和表2提供的数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高至
(2)20℃时,饱和食盐水溶质的质量分数为
(3)常温下,将5gNaCl粉末放入10mL乙醇中,振荡时形成的是
(4)为证明CO2能与NaOH反应生成Na2CO3,小明同学将CO2通入饱和NaOH的乙醇溶液中,请推测实验可观察到的现象
您最近一年使用:0次



