溶液是生产生活中常见的物质,依据相关信息回答问题。资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
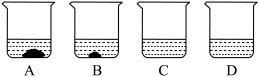
①(填字母序号)______ 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为_________ g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是_____ (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:
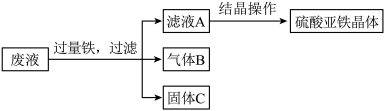
请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤______ ;
②流程中生成气体B的反应的化学方程式是:__________ 。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。

①(填字母序号)
②使B烧杯的溶液升温至50℃时,溶液的质量为
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:

请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤
②流程中生成气体B的反应的化学方程式是:
更新时间:2019-01-22 17:23:19
|
相似题推荐
【推荐1】水是人类赖以生存和发展不可缺少的重要物质资源之一,请你用水的知识回答下列问题:
(1)下列物质属于纯净物的是___________(填字母)。
(2)3月22日是“世界水日”,自来水厂净水过程中不涉及的步骤是___________(填字母)。
(3)如图是KNO3和NH4Cl的溶解度曲线,根据图示填空
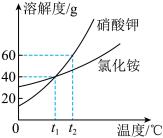
①将NH4Cl的不饱和溶液变成饱和溶液,方法有___________ (填一条即可)。
②t2℃时,KNO3饱和溶液中溶质的质量分数是___________ 。
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是___________ (填“KNO3”或“NH4Cl”)溶液。
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。
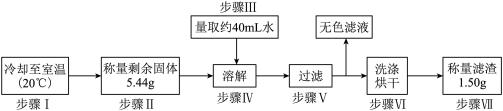
(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为___________ g。
②步骤Ⅲ中水量约为40mL而不是30mL的原因___________ 。
(1)下列物质属于纯净物的是___________(填字母)。
| A.海水 | B.冰水混合物 | C.矿泉水 | D.自来水 |
| A.沉淀 | B.蒸馏 | C.吸附 | D.消毒 |

①将NH4Cl的不饱和溶液变成饱和溶液,方法有
②t2℃时,KNO3饱和溶液中溶质的质量分数是
③t2℃时,分别将200g KNO3饱和溶液和200gNH4Cl饱和溶液蒸发10g水,再恢复到t2℃后过滤,所得溶液质量较大的是
(4)某小组称取4.90g氯酸钾和1.50g二氧化锰混合后进行制取氧气,收集一定量氧气后结束实验,为回收剩余固体中的二氧化锰,进行如下实验。

(20℃时氯酸钾、氯化钾的溶解度分别为7g、34g;假设溶液中两种物质的溶解度相互无影响,此时水的密度为1g/ml)
①5.44g剩余固体中含有的氯酸钾质量为
②步骤Ⅲ中水量约为40mL而不是30mL的原因
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】碳酸钠是一种重要的化工原料,获取和制备碳酸钠有多种方法。
I、我国有许多盐碱湖,湖中溶有大量的碳酸钠和氯化钠,请据下图回答问题。
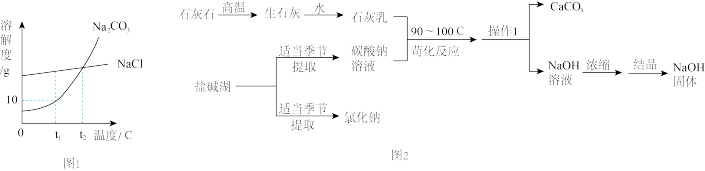
(1)根据图1溶解度曲线分析,提取碳酸钠的季节最好是______ ,配制等质量分数的碳酸钠和氯化钠的饱和溶液,需要将温度控制在______ 。
(2)图2流程图,苛化反应时将温度升高至99-100℃的原因是______ 。
Ⅱ、侯氏制碱法。1943年我国科学家侯德榜创造性地将制碱与制氨两种工艺联合起来,发明了侯氏制碱法,促进世界制碱工业的发展。模拟流程图如下图所示。

(3)操作a名称是______ 。
(4)步骤Ⅲ中,NaCl、NH4Cl、NaHCO3三种物质中溶解度最小的是______ ,写出该步骤中的化学反应方程式______ 。
(5)“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠。某兴趣小组的同学称取6g纯碱样品,加入过量的CaCl2溶液,过滤出的沉淀物经洗涤、干燥后称重得5.0g沉淀。
①判断沉淀洗涤干净的方法是:向最后一次的洗涤液中滴加______ ,若无沉淀生成,则表示沉淀已洗涤干净。
②计算该纯碱样品中Na2CO3的质量分数______ (计算结果精确到0.1%)。
I、我国有许多盐碱湖,湖中溶有大量的碳酸钠和氯化钠,请据下图回答问题。

(1)根据图1溶解度曲线分析,提取碳酸钠的季节最好是
(2)图2流程图,苛化反应时将温度升高至99-100℃的原因是
Ⅱ、侯氏制碱法。1943年我国科学家侯德榜创造性地将制碱与制氨两种工艺联合起来,发明了侯氏制碱法,促进世界制碱工业的发展。模拟流程图如下图所示。

(3)操作a名称是
(4)步骤Ⅲ中,NaCl、NH4Cl、NaHCO3三种物质中溶解度最小的是
(5)“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠。某兴趣小组的同学称取6g纯碱样品,加入过量的CaCl2溶液,过滤出的沉淀物经洗涤、干燥后称重得5.0g沉淀。
①判断沉淀洗涤干净的方法是:向最后一次的洗涤液中滴加
②计算该纯碱样品中Na2CO3的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】溶液在生活、生产中有广泛的用途。
(1)在农业生产上,常需要用质量分数为16%的氧化钠溶液选种。某同学配制1000g质量分数为16%的氯化钠溶液,需要氯化钠的质量为_____ g;水的体积为 _____ mL(水的密度近似看作1g/mL)。
(2)利用风吹日晒可以从海水中提取粗盐,粗盐中一般含有少量泥沙等杂质。以下是制备较纯氯化钠的实验流程,请回答问题。
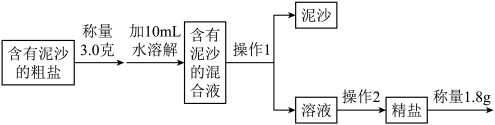
操作1的原理是_____ ,此操作中玻璃棒的作用是 _____ ,操作2的名称是 _____ ,其中用到的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、坩埚钳、 _____ ,实验结束后计算精盐的产率为 _____ ,如果该产率超过100%,可能的原因是 _____ (填序号)。
A 食盐没有全部溶解就进行过滤
B 操作2溶液飞溅
C 实验结束后称量的精盐很潮湿
D 过滤时滤纸有破损
(3)已知食盐在不同温度下的溶解度数据如下表所示:
常温下Ⅱ的实验流程中加10mL水,能否使3.0g粗盐中的氯化钠全部溶解?说明理由 _____ 。
化学课上同学们研究物质溶解性的实验如下图所示:
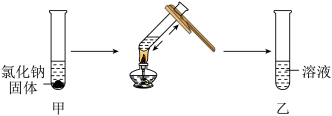
某同学将1.85g氯化钠加入5mL水中,充分振荡后静置,现象如图甲所示,他认为图甲试管中的溶液为该温度下氧化钠的饱和溶液,判断的依据是_____ 。再对该试管进行加热,得到如图乙所示的溶液,则可判断加热溶液的温度范围是 _____ 。该同学认为得到的是不饱和溶液,你同意他的判断吗?说出理由 _____ 。
(1)在农业生产上,常需要用质量分数为16%的氧化钠溶液选种。某同学配制1000g质量分数为16%的氯化钠溶液,需要氯化钠的质量为
(2)利用风吹日晒可以从海水中提取粗盐,粗盐中一般含有少量泥沙等杂质。以下是制备较纯氯化钠的实验流程,请回答问题。

操作1的原理是
A 食盐没有全部溶解就进行过滤
B 操作2溶液飞溅
C 实验结束后称量的精盐很潮湿
D 过滤时滤纸有破损
(3)已知食盐在不同温度下的溶解度数据如下表所示:
| 温度(°C) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度(克) | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37.0 | 37.3 |
化学课上同学们研究物质溶解性的实验如下图所示:

某同学将1.85g氯化钠加入5mL水中,充分振荡后静置,现象如图甲所示,他认为图甲试管中的溶液为该温度下氧化钠的饱和溶液,判断的依据是
您最近一年使用:0次
【推荐1】中国在5000多年前,就开始刮取海滨咸土,淋卤煎盐。结合资料,回答“从海水到餐桌上的食盐”的有关问题:
(1)获得食盐宜采用蒸发结晶的方法,其原因是_______ 。
(2)请从微观角度解释风和日丽的天气晒盐效率更高的原因__________ 。如图是硝酸钾和氯化钠的溶解度数据表和溶解度曲线。
(溶解度单位:g/100g水)
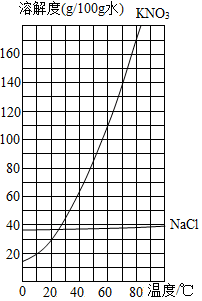
①补全表格中的溶解度数据______ 。
②相对溶解度数据表溶解度曲线的优点是_______ (只写一点)。
(3)按下图所示进行实验:
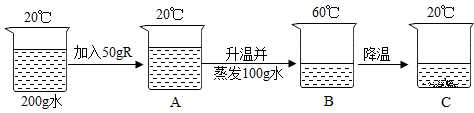
①R是_____ (选填“氯化钠”或“硝酸钾”),A、B、C三个烧杯中溶液的溶质质量分数的大小关系是_________ 。
②如果将含27.0 gNaCl、63.2gKNO3的混合物溶于mg热水,然后冷却至20℃。若要使KNO3析出而NaCl不析出,则m的取值范围是______ 。
(1)获得食盐宜采用蒸发结晶的方法,其原因是
(2)请从微观角度解释风和日丽的天气晒盐效率更高的原因
(溶解度单位:g/100g水)
| 温度(℃) | 20 | 40 | 60 | 80 |
| S(KNO3) | 31.6 | 63.9 | 169 | |
| S (NaCl) | 36.0 | 36.6 | 37.3 | 38.4 |

①补全表格中的溶解度数据
②相对溶解度数据表溶解度曲线的优点是
(3)按下图所示进行实验:

①R是
②如果将含27.0 gNaCl、63.2gKNO3的混合物溶于mg热水,然后冷却至20℃。若要使KNO3析出而NaCl不析出,则m的取值范围是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】下表为氯化钠和硝酸钾的溶解度(g/100g 水)
①60℃时,KNO3 的溶解度为__ ;表中“37.8”的意义是__ 。
②20℃时 KNO3 的溶解度__ (选填“大于”“小于”)NaCl 的溶解度。随着温度升高,NaCl 的溶解度_____ (选填“变大”“变小”或“不变”)。
③20℃时,完全溶解 18gNaCl 恰好得到饱和溶液,所需水量是__ g,该溶液质量分数为__ 。
④20℃时,向 10gKNO3 固体不断加水,有关图像正确的是__ (选填编号)
A. B.
B.  C.
C.  D.
D. 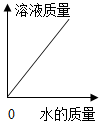
⑤现有 150gKNO3 和 4gNaCl 的混合物,能得到较纯净的 KNO3 且质量最多的操作是__ (选填编号)。
a.20℃时,投入 12mL 水中,充分搅拌、溶解、过滤。
b.取 80℃时 100g 水溶液,冷却到 20℃时,过滤。
c.100g 水溶解,加热蒸发至有晶体析出停止加热,冷却至 20℃,过滤。
d.20℃时,投入 10mL 水中,加热至 80℃,趁热过滤。
| 温度 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
①60℃时,KNO3 的溶解度为
②20℃时 KNO3 的溶解度
③20℃时,完全溶解 18gNaCl 恰好得到饱和溶液,所需水量是
④20℃时,向 10gKNO3 固体不断加水,有关图像正确的是
A.
 B.
B.  C.
C.  D.
D. 
⑤现有 150gKNO3 和 4gNaCl 的混合物,能得到较纯净的 KNO3 且质量最多的操作是
a.20℃时,投入 12mL 水中,充分搅拌、溶解、过滤。
b.取 80℃时 100g 水溶液,冷却到 20℃时,过滤。
c.100g 水溶解,加热蒸发至有晶体析出停止加热,冷却至 20℃,过滤。
d.20℃时,投入 10mL 水中,加热至 80℃,趁热过滤。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】下图是甲、乙、丙三种固体物质的溶解度曲线,据图回答下列问题。
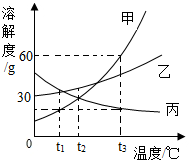
(1)0℃时,乙物质的溶解度是___________ 。
(2)除去甲中混有的氯化钠,可采用的方法是__________ 。
(3)t3℃时,将甲、丙两物质的饱和溶液同时降温至___________ ℃,它们溶质的质量分数相等。
(4)下列说法正确的是 。

(1)0℃时,乙物质的溶解度是
(2)除去甲中混有的氯化钠,可采用的方法是
(3)t3℃时,将甲、丙两物质的饱和溶液同时降温至
(4)下列说法正确的是 。
| A.向t2℃时甲的饱和溶液m1g和丙的饱和溶液m2g中分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等 |
| B.t2℃时,分别向甲和乙的饱和溶液中加入等质量的水,所得溶液的质量分数可能相等 |
| C.t3℃时,向50.0g质量分数为30%的甲溶液中加入10.0g固体甲,所得溶液中溶质的质量分数为37.5% |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】已知KNO3和KCl在不同温度时的溶解度如下表。请回答下列问题:
(1)依据上表数据,绘制了KNO3和KCl的溶解度曲线如图,能代表KNO3溶解度曲线的是_______ (填“a”或“b”)。
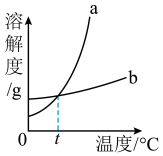
(2)分析表中数据,t的范围为_______(填字母序号)。
(3)40℃时,分别将30gKNO3和KCl加到50g水中,充分溶解后一定能形成饱和溶液的物质是_______ ,其溶液的溶质质量分数为_______ (结果精确到0.1%)。
(4)若KNO3中混有少量KCl,可采用_______ 的方法提纯KNO3。
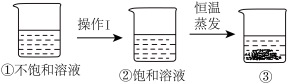
(5)下图是有关KNO3溶液的实验操作及变化情况。下列说法中正确的是_______。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
(1)依据上表数据,绘制了KNO3和KCl的溶解度曲线如图,能代表KNO3溶解度曲线的是

(2)分析表中数据,t的范围为_______(填字母序号)。
A. | B. | C. | D. |
(3)40℃时,分别将30gKNO3和KCl加到50g水中,充分溶解后一定能形成饱和溶液的物质是
(4)若KNO3中混有少量KCl,可采用
(5)下图是有关KNO3溶液的实验操作及变化情况。下列说法中正确的是_______。

| A.操作Ⅰ一定是降温 | B.①与②的溶液质量可能相等 |
| C.②与③的溶质质量一定相等 | D.②与③的溶质质量分数一定相等 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】认真分析下列各图,回答相关问题:

(1)根据图1分析,20℃时,将 加入
加入 水中形成溶液的质量为
水中形成溶液的质量为 _____ g.
(2)图2中打开可乐瓶冒出大量气泡,说明气体的溶解度与_____ 有关。
(3)在图3所示的烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象是_____ ;乙试管内的溶液是 _____ (填“饱和”或“不饱和”)溶液.
(4)用氯化钠固体和水配制100g质量分数为6%的NaCl溶液,其步骤有:计算、_____ 、量取、溶解;其中在溶解过程中玻璃棒的作用是 _____ .

(1)根据图1分析,20℃时,将
 加入
加入 水中形成溶液的质量为
水中形成溶液的质量为 (2)图2中打开可乐瓶冒出大量气泡,说明气体的溶解度与
(3)在图3所示的烧杯中加入一定量的硝酸铵,溶解后甲试管内出现的现象是
(4)用氯化钠固体和水配制100g质量分数为6%的NaCl溶液,其步骤有:计算、
您最近一年使用:0次
【推荐3】我国既是陆地大国,也是海洋大国。党的十九届五中全会《建议》提出:“坚持海陆统筹,发展海洋经济,建设海洋强国。”海洋对人类社会生存和发展具有重要意义。
(1)海水中蕴含着丰富的化学资源,我们应予以合理开发及综合利用。
①海水淡化的常见方法有______ (至少答一条)。
②海水制镁工艺中,电解熔融状态的氯化镁制取金属镁的化学方程式为______ 。
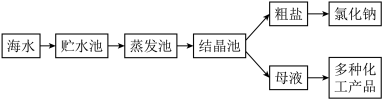
③利用海水提取粗盐的过程如图所示,回答有关问题。
一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会______ (填“增大”、“不变”或“减小”)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到玻璃棒,其中在过滤操作中玻璃棒的作用是______ ,在蒸发操作时,当蒸发皿中______ 时停止加热。
④我国已经成为全球领先掌握可燃冰试采核心技术的国家。可燃冰作为“未来能源”的理由是______ 。
(2)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①t1℃时,若有不同质量的Na2CO3饱和溶液和NaCl的饱和溶液,分别升温到t2℃,则所得Na2CO3溶液质量分数______ NaCl溶液溶质质量分数(填“大于”“小于”“无法确定”)。
②t1℃时,200g水中加入40g Na2CO3固体,经充分溶解,所得溶液中溶质与溶剂的质量之比为______ (填最简整数比)。
③t2℃时,将相同质量的碳酸钠和氯化钠的饱和溶液分别降温至t1℃,析出晶体的质量碳酸钠______ 氯化钠(选填“大于”“等于”“小于”“无法判断”之一)。
④Na2CO3中混有少量的NaCl,提纯Na2CO3的方法为______ (填“蒸发结晶”或“降温结晶”)。
(1)海水中蕴含着丰富的化学资源,我们应予以合理开发及综合利用。
①海水淡化的常见方法有
②海水制镁工艺中,电解熔融状态的氯化镁制取金属镁的化学方程式为
③利用海水提取粗盐的过程如图所示,回答有关问题。

一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量会
④我国已经成为全球领先掌握可燃冰试采核心技术的国家。可燃冰作为“未来能源”的理由是
(2)1926年我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图所示,试回答下列问题:

①t1℃时,若有不同质量的Na2CO3饱和溶液和NaCl的饱和溶液,分别升温到t2℃,则所得Na2CO3溶液质量分数
②t1℃时,200g水中加入40g Na2CO3固体,经充分溶解,所得溶液中溶质与溶剂的质量之比为
③t2℃时,将相同质量的碳酸钠和氯化钠的饱和溶液分别降温至t1℃,析出晶体的质量碳酸钠
④Na2CO3中混有少量的NaCl,提纯Na2CO3的方法为
您最近一年使用:0次



