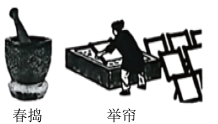
造纸是我国四大发明之一、北宋诗人曾对“敲冰纸”写下“寒溪浸楮春夜月,敲冰举帘匀割脂” 的赞美诗句。该造纸的部分生产情景如如图:
(1)“寒溪”是制得质量上佳纸张的重要原因。因为冬天气温低,水中可溶性杂质溶解度变_____ 。
(2)“楮”指树皮,树皮属于_____ (选填“天然”或“合成”)有机高分子材料。
(3)“帘”是带筛网的捞纸工具,“举帘”工作原理与实验室中_____ (填一操作名称)相似。
(4)古代造纸工艺中常加入“碱液”蒸煮,有利于脱胶和分散纤维,你认为可能加入的物质是 (填字母序号)。
(5)人们常采用喷洒二乙基锌Zn(C2H5)2溶液的方法来保护纸质文物:Zn(C2H5)2可以与水反应生成一种金属氧化物和乙烷(C2H6)气体,请写出该反应的化学方程式_____ 。

(1)“寒溪”是制得质量上佳纸张的重要原因。因为冬天气温低,水中可溶性杂质溶解度变
(2)“楮”指树皮,树皮属于
(3)“帘”是带筛网的捞纸工具,“举帘”工作原理与实验室中
(4)古代造纸工艺中常加入“碱液”蒸煮,有利于脱胶和分散纤维,你认为可能加入的物质是 (填字母序号)。
| A.食盐水 | B.草木灰水 | C.食醋 | D.泥水 |
更新时间:2023-07-03 19:23:12
|
相似题推荐
【推荐1】如表是KCl和KNO3在不同温度时的溶解度。请回答下列问题。
(1)50℃时,等质量的水中最多溶解的KCl和KNO3的质量比为______ 。
(2)T℃时,某KCl溶液恒温进行如图操作,现象如图1所示。则n=______ ,T=______ 。______ (填“变大”、“变小”或“不变”)。
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
(1)50℃时,等质量的水中最多溶解的KCl和KNO3的质量比为
(2)T℃时,某KCl溶液恒温进行如图操作,现象如图1所示。则n=


您最近一年使用:0次
【推荐2】t2 ℃时,将甲,乙各80 g分别放到盛有100 g水的两个烧杯中,充分溶解后,恢复到t2 ℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:

(1)固体甲对应的溶解度曲线是________ (填“a”或“b”)。
(2)M点的含义________________________________________ 。
(3)向烧杯①的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是______________________________________ 。
(4)将t2 ℃等质量的甲、乙饱和溶液分别降温到t1 ℃时,所得溶液的有关说法正确的是________ (填字母)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙

(1)固体甲对应的溶解度曲线是
(2)M点的含义
(3)向烧杯①的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是
(4)将t2 ℃等质量的甲、乙饱和溶液分别降温到t1 ℃时,所得溶液的有关说法正确的是
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】从钴酸锂废极片(主要成分LiCoO2)中回收得到Co2O3和Li2CO3的一种工艺流程如下。

(1)在实验室中完成操作1、2时,用到的玻璃仪器是______ (填一种即可)。
(2)操作3中,CoC2O4在空气中焙烧生成Co2O3和一种气体,推测该气体是CO2,从元素守恒的角度说明理由:______ 。
(3)操作4中,洗涤固体Li2CO3时,用热水比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而______ 。

(1)在实验室中完成操作1、2时,用到的玻璃仪器是
(2)操作3中,CoC2O4在空气中焙烧生成Co2O3和一种气体,推测该气体是CO2,从元素守恒的角度说明理由:
(3)操作4中,洗涤固体Li2CO3时,用热水比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐1】“加碘盐”是指向食盐中加入KIO3作补碘剂。工业上以KClO3为原料制备KIO3的工艺流程如图所示:

请回答下列问题:(资料:氯气易溶于水,有毒)
(1)步骤2中“逐Cl2”即除去Cl2,加热可以将溶液中Cl2除去,原因是_____
(2)步骤3中操作X的名称是_____
(3)步骤4中玻璃棒的作用是_____
(4)步骤5中可以用_____ 测溶液的酸碱度,步骤5中反应物为KOH和_____ 。

请回答下列问题:(资料:氯气易溶于水,有毒)
(1)步骤2中“逐Cl2”即除去Cl2,加热可以将溶液中Cl2除去,原因是
(2)步骤3中操作X的名称是
(3)步骤4中玻璃棒的作用是
(4)步骤5中可以用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】我校防疫“新冠肺炎”期间,班级常用的防疫物资有:口罩、洗手液、75%的医用酒精和84消毒液,有效成分为次氯酸钠(NaClO)等。
(1)口罩是抗击“新冠病毒”的重要物资,其核心材料是熔喷布,它是以聚丙烯(CH2CHCH3)n超细纤维为主要原料制成的高静电过滤材质,具有很好的空气过滤性。聚丙烯超细纤维属于______ 。
A合成材料B复合材料C有机高分子化合物D无机非金属材料

(2)用七步洗手法清洁手部污物和细菌,以减少细菌病毒的传播。洗手中洗手液起到______ 作用。
(3)75%的酒精被称为“医用酒精”,常用于杀菌消毒,其中的溶剂是______ 。
(4)班级等公共场所常用“84消毒液”杀菌消毒。测得稀释后的消毒液的pH=9,该溶液显______ 性。
制备其主要成分次氯酸钠(NaClO)的化学方程式为: ,则X的化学式为
,则X的化学式为______ 。
(1)口罩是抗击“新冠病毒”的重要物资,其核心材料是熔喷布,它是以聚丙烯(CH2CHCH3)n超细纤维为主要原料制成的高静电过滤材质,具有很好的空气过滤性。聚丙烯超细纤维属于
A合成材料B复合材料C有机高分子化合物D无机非金属材料

(2)用七步洗手法清洁手部污物和细菌,以减少细菌病毒的传播。洗手中洗手液起到
(3)75%的酒精被称为“医用酒精”,常用于杀菌消毒,其中的溶剂是
(4)班级等公共场所常用“84消毒液”杀菌消毒。测得稀释后的消毒液的pH=9,该溶液显
制备其主要成分次氯酸钠(NaClO)的化学方程式为:
 ,则X的化学式为
,则X的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】节假日里,某班同学去郊外进行野炊活动,请回答下列问题。
①他们所带的下列物品中,主要材料属于合成材料的是______ (填序号)
A纯净水 B棉布围裙 C铸铁锅 D塑料凳子
②学生野炊的食谱如下:主食:米饭; 配菜: 红烧肉、鲫鱼汤、烤鸡翅。从膳食平衡角度来看,你认为应补充的营养素是________ 。
③同学们烧烤时所用的煤属于_______ (填“可再生”或“不可再生”)能源。
④同学们的电动车使用的是铅蓄电池。电池中使用的是质量分数为20%的稀硫酸,若用50g、98%的浓硫酸来配制该稀硫酸,则需加水_______ mL(水的密度为1g/mL)
①他们所带的下列物品中,主要材料属于合成材料的是
A纯净水 B棉布围裙 C铸铁锅 D塑料凳子
②学生野炊的食谱如下:主食:米饭; 配菜: 红烧肉、鲫鱼汤、烤鸡翅。从膳食平衡角度来看,你认为应补充的营养素是
③同学们烧烤时所用的煤属于
④同学们的电动车使用的是铅蓄电池。电池中使用的是质量分数为20%的稀硫酸,若用50g、98%的浓硫酸来配制该稀硫酸,则需加水
您最近一年使用:0次
【推荐2】化学基础与常识。
(1)如图,超市手推车各部件中,由有机合成材料制成的是把手和_____ 。

(2)保持二氧化硫化学性质的最小微粒是_______ (填符号)。
(3)工业生产硫酸中的某一步反应用微观模型图表示如图:

参加反应的反应物间分子个数比是_______ 。
(4)钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTO3)制备钛的流程如图:

①钛酸亚铁(FeTiO3)不属于_______ (双项选择,填序号)。
A、化合物
B、有机物
C、纯净物
D、单质
②电解厂参加反应的物质为_______ 。
(1)如图,超市手推车各部件中,由有机合成材料制成的是把手和

(2)保持二氧化硫化学性质的最小微粒是
(3)工业生产硫酸中的某一步反应用微观模型图表示如图:

参加反应的反应物间分子个数比是
(4)钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTO3)制备钛的流程如图:

①钛酸亚铁(FeTiO3)不属于
A、化合物
B、有机物
C、纯净物
D、单质
②电解厂参加反应的物质为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学就在我们身边,人类的衣、食、住、行都离不开化学,请回答下列问题:
(1)生活中用汽油或洗涤剂都能去除衣服上的油污,二者对应的原理均发生了_________ 变化选填“物理”或“化学”)。
(2)水果、蔬菜富含的营养素是_________ ,该营养素可以调节新陈代谢、预防疾病,维持身体健康。
(3)家里的防盗门材料通常用不锈钢属于_________ 材料(选填“合成”或“复合”或“金属”)。
(4)使用尾气净化装置,使燃油汽车尾气中的_________ (填一种气体的化学式)和氮的氧化物反应生成 和
和 。
。
(1)生活中用汽油或洗涤剂都能去除衣服上的油污,二者对应的原理均发生了
(2)水果、蔬菜富含的营养素是
(3)家里的防盗门材料通常用不锈钢属于
(4)使用尾气净化装置,使燃油汽车尾气中的
 和
和 。
。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】化学实验基本操作是实验探究的重要保证,观察下列4个实验基本操作,回答下列问题:
A.称量固体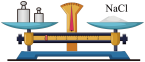 B.检查气密性
B.检查气密性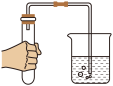
C.加热液体 D.过滤
D.过滤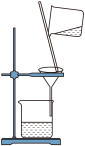
(1)四个化学实验操作中完全正确的是_______ (填字母序号);
(2)A实验中砝码质量15g,游码在1.6g刻度处,其称得NaC1的实际质量是_______ g;
(3)B实验是检查装置气密性,从图中观察到该装置是否漏气_______ 。
(4)C实验时用酒精灯外焰加热试管出现炸裂,其原因是_______ 。
(5)D实验中玻璃棒的作用是_______ ,若过滤后发现滤液仍浑浊,应当_______ 。
A.称量固体
 B.检查气密性
B.检查气密性
C.加热液体
 D.过滤
D.过滤
(1)四个化学实验操作中完全正确的是
(2)A实验中砝码质量15g,游码在1.6g刻度处,其称得NaC1的实际质量是
(3)B实验是检查装置气密性,从图中观察到该装置是否漏气
(4)C实验时用酒精灯外焰加热试管出现炸裂,其原因是
(5)D实验中玻璃棒的作用是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】MgSO4·7H2O是一种重要的化工原料,某研究性学习小组设计了利用菱镁矿石(主要成分是MgCO3,并含有MnCO3、SiO2等杂质)制取MgSO4·7H2O的实验流程如下。 ;
;
②SiO2不溶于稀硫酸。
(1)酸浸时,为了提高反应速率,可以采取的措施是______ 。
(2)写出酸浸时MgCO3发生反应的化学反应方程式:______ 。
(3)过滤1得到的滤渣主要成分是______ 。
(4)过滤2得到的滤液在浓缩结晶后,要经过______ 、洗涤、干燥等步骤才可得到MgSO4·7H2O。
(5)若制得MgSO4·7H2O的质量为82.00g,测得MnCO3的质量为2.30g,且测得过滤1滤渣质量为4.70g,忽略各物质在溶液中的溶解损失,可计算出菱镁矿石中MgCO3的质量分数为______ (写出计算过程)。

 ;
;②SiO2不溶于稀硫酸。
(1)酸浸时,为了提高反应速率,可以采取的措施是
(2)写出酸浸时MgCO3发生反应的化学反应方程式:
(3)过滤1得到的滤渣主要成分是
(4)过滤2得到的滤液在浓缩结晶后,要经过
(5)若制得MgSO4·7H2O的质量为82.00g,测得MnCO3的质量为2.30g,且测得过滤1滤渣质量为4.70g,忽略各物质在溶液中的溶解损失,可计算出菱镁矿石中MgCO3的质量分数为
您最近一年使用:0次




