身边的二氧化碳燃料在使用过程中的碳循环如图:
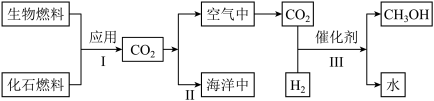
(1)化石燃料包括煤、______ 和天然气,过程Ⅰ应用化石燃料发生燃烧时都会产生二氧化碳,原因是______ ,在燃烧煤块前需粉碎,这样做的目的是______ 。
(2)过程Ⅱ利用海水进行碳储存,可以缓解空气中CO2过多的问题。向海水中通入足量的CO2,大约有1%的CO2会和水反应,该反应的化学方程式为______ 。反应的基本类型为______ 。过程Ⅲ中二氧化碳发生转化时发生化学反应的方程式为______ 。
(3)为验证绿色植物通过光合作用吸收CO2,某小组利用如图装置制备CO2并进行实验,回答下列问题。
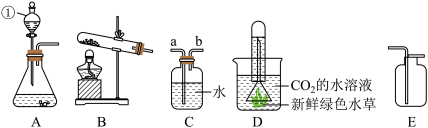
Ⅰ.①仪器①的名称是______ 。检查装置A气密性的方法是______ 。
②为制得CO2的水溶液,CO2应从装置C的______ (填“a”或“b”)端通入。
③将CO2的水溶液转移至烧杯,并组装置如图D所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是______ 。
Ⅱ.查阅资料知,高铁酸钾(K2FeO2)固体可用于制取氧气。
方案一:
方案二: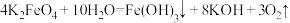
①若用方案一制取氧气,应该选用的发生装置是______ ,若收集一瓶干燥的氧气可选用的仪器是______ 。
②下列关于以上两种方案制取氧气的说法正确的是______ (填序号)。
a.方案一发生的是分解反应
b.方案二更简便、节能
c.制取等质量的氧气,两种方案所需高铁酸钾的质量相等

(1)化石燃料包括煤、
(2)过程Ⅱ利用海水进行碳储存,可以缓解空气中CO2过多的问题。向海水中通入足量的CO2,大约有1%的CO2会和水反应,该反应的化学方程式为
(3)为验证绿色植物通过光合作用吸收CO2,某小组利用如图装置制备CO2并进行实验,回答下列问题。

Ⅰ.①仪器①的名称是
②为制得CO2的水溶液,CO2应从装置C的
③将CO2的水溶液转移至烧杯,并组装置如图D所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是
Ⅱ.查阅资料知,高铁酸钾(K2FeO2)固体可用于制取氧气。
方案一:

方案二:
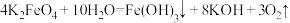
①若用方案一制取氧气,应该选用的发生装置是
②下列关于以上两种方案制取氧气的说法正确的是
a.方案一发生的是分解反应
b.方案二更简便、节能
c.制取等质量的氧气,两种方案所需高铁酸钾的质量相等
更新时间:2023-07-19 10:05:39
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】氧气是初中化学学习的重要内容。
(1)按体积计算,氧气大约占空气成分的_______ %,空气污染指数中属于氧化物的有___________ 、____________ (任填两个)。
(2)氧气是________ (多选题)
A.单质 B.混合物 C.氧化物 D.化合物 E.纯净物
(3)下图是元素周期表中的一格和氧元素的原子结构示意图。从图中获取的信息不正确的是_____________ ;

A.氧的原子序数是8 B.氧的相对原子质量是16.00g
C.氧属于非金属元素 D.氧原子有两个电子层,最外层电子数为6
(4)如下图,用带火星的木条分别以甲乙两种方式迅速插入盛有氧气的集气瓶中,发现木条复燃,且在甲中燃烧比在乙中更旺。这说明氧气具有哪些性质?
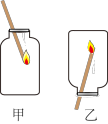
①__________________________________________
②___________________________________________
(5)加热31.6克高锰酸钾制取一定质量的氧气,生成氧气的质量是________ ?
(1)按体积计算,氧气大约占空气成分的
(2)氧气是
A.单质 B.混合物 C.氧化物 D.化合物 E.纯净物
(3)下图是元素周期表中的一格和氧元素的原子结构示意图。从图中获取的信息不正确的是

A.氧的原子序数是8 B.氧的相对原子质量是16.00g
C.氧属于非金属元素 D.氧原子有两个电子层,最外层电子数为6
(4)如下图,用带火星的木条分别以甲乙两种方式迅速插入盛有氧气的集气瓶中,发现木条复燃,且在甲中燃烧比在乙中更旺。这说明氧气具有哪些性质?

①
②
(5)加热31.6克高锰酸钾制取一定质量的氧气,生成氧气的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
解题方法
【推荐2】如图是氧气的实验室制取与性质实验。

(1)试管口棉花的作用是________________________ 。
(2)检验氧气集满的方法是________________________ 。
(3)制取氧气的主要步骤如下,正确的顺序是___________ (填序号)。
①装入药品,开始加热 ②停止加热 ③收集气体 ④组装仪器,检查气密性
(4)硫在氧气中燃烧的现象是_________ 。
(5)根据化学方程式计算,制取0.96g氧气,至少需要高锰酸钾的质量是______ ?

(1)试管口棉花的作用是
(2)检验氧气集满的方法是
(3)制取氧气的主要步骤如下,正确的顺序是
①装入药品,开始加热 ②停止加热 ③收集气体 ④组装仪器,检查气密性
(4)硫在氧气中燃烧的现象是
(5)根据化学方程式计算,制取0.96g氧气,至少需要高锰酸钾的质量是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】如图所示为实验室中常见的气体制备和收集装置。请回答下列问题:

(1)用B装置制取氧气时,反应的化学方程式为_______ ;长颈漏斗下端浸没在液面以下的原因是_______ 。
(2)实验室用高锰酸钾制取一瓶干燥的氧气应选用的一套装置为_____ (填字母代号);其反应的化学方程式为____ ;实验结束时,要先把导管移出水面,再熄灭酒精灯。请解释原因_______ 。
(3)氧气可采用D装置收集并用带火星的木条检验,这是利用了氧气_______ 的性质;欲使用装置E代替排水法收集氧气,其操作是_______ 。
(4)在实验室里加热30g氯酸钾和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g请计算原混合物中氯酸钾的质量分数______ 。

(1)用B装置制取氧气时,反应的化学方程式为
(2)实验室用高锰酸钾制取一瓶干燥的氧气应选用的一套装置为
(3)氧气可采用D装置收集并用带火星的木条检验,这是利用了氧气
(4)在实验室里加热30g氯酸钾和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g请计算原混合物中氯酸钾的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】根据下列实验装置图,回答问题:


(1)实验室用图一中A、E装置组合制取氧气的化学方程式为_____________ 。
(2)实验室制取氢气可选用F装置收集,氢气应从_______ 端通入(填m或n);氢气是未来理想的能源,目前还不能大量使用的主要原因是______________ 。
(3)装置B和G都能用于实验室制取二氧化碳,用C装置的优点是_______________ 。
(4)用图二所示实验探究CO2的性质,其中a为干燥的紫色石磊小花,b为湿润的紫色石蕊小花。通入CO2一段时间后,观察到______________ ,证明CO2可以与水反应,该反应的化学方程式为______________ 。烧杯中蜡烛由低到高依次熄灭。据此可以说明CO2的性质有_______ 。
(5)实验室用电子秤称取2.5g大理石放入20g稀盐酸(足量)中,充分反应后(杂质不反应),容器内所有物质总质量为21.62g,则该大理石中碳酸钙的质量分数是多少?


(1)实验室用图一中A、E装置组合制取氧气的化学方程式为
(2)实验室制取氢气可选用F装置收集,氢气应从
(3)装置B和G都能用于实验室制取二氧化碳,用C装置的优点是
(4)用图二所示实验探究CO2的性质,其中a为干燥的紫色石磊小花,b为湿润的紫色石蕊小花。通入CO2一段时间后,观察到
(5)实验室用电子秤称取2.5g大理石放入20g稀盐酸(足量)中,充分反应后(杂质不反应),容器内所有物质总质量为21.62g,则该大理石中碳酸钙的质量分数是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】某小组同学对二氧化碳的制取和相关性质进行探究。

(1)用图一所示的装置制取二氧化碳。
Ⅰ.该装置能随时控制反应的发生和停止,请简述使反应停止的原理___________ 。
Ⅱ.若制得0.1摩尔二氧化碳,理论上需要消耗___________ g碳酸钙(根据化学方程式列式计算)
(2)用实验证明碳酸型饮料中含有二氧化碳。
Ⅰ.用图二所示的装置进行实验:打开汽水瓶盖,立即塞上带导管的橡皮塞,将导管另一端伸入装有试剂的试管中。
甲同学在试管中加入少量澄清石灰水,观察到试管内___________ ,由此得到结论:该汽水中含有二氧化碳。乙同学在试管中加入少量紫色石蕊溶液,观察到试管内___________ ,乙同学认为也能得到甲同学的结论。
Ⅱ.小组同学对甲、乙两位同学的实验方案进行评价。
认为甲同学的方案比较合理,其试管中发生反应的化学方程式为___________ 。质疑乙同学的方案不够严密,认为也可能是该汽水中的柠檬酸随气体进入试管,而引起紫色石蕊溶液的变色。
Ⅲ.针对质疑,乙同学又进行了如下探究:
查阅资料:柠檬酸为无色晶体,易溶于水,常温稳定,分解温度约为175℃。
乙同学在自己实验的基础上,未添加试剂,只进行了一步实验操作,该操作是___________ ,观察到___________ ,确认不是因为柠檬酸随气体进入试管而引起紫色石蕊溶液的变色。

(1)用图一所示的装置制取二氧化碳。
Ⅰ.该装置能随时控制反应的发生和停止,请简述使反应停止的原理
Ⅱ.若制得0.1摩尔二氧化碳,理论上需要消耗
(2)用实验证明碳酸型饮料中含有二氧化碳。
Ⅰ.用图二所示的装置进行实验:打开汽水瓶盖,立即塞上带导管的橡皮塞,将导管另一端伸入装有试剂的试管中。
甲同学在试管中加入少量澄清石灰水,观察到试管内
Ⅱ.小组同学对甲、乙两位同学的实验方案进行评价。
认为甲同学的方案比较合理,其试管中发生反应的化学方程式为
Ⅲ.针对质疑,乙同学又进行了如下探究:
查阅资料:柠檬酸为无色晶体,易溶于水,常温稳定,分解温度约为175℃。
乙同学在自己实验的基础上,未添加试剂,只进行了一步实验操作,该操作是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】CO2对人类的生命活动非常重要。我们可以从多角度认识二氧化碳。

(1)正常雨水的pH<7,是因为雨水降落过程中遇到了空气中的二氧化碳,与二氧化碳反应生成______ (写该物质名称),使雨水呈酸性。
(2)如图,大理石和盐酸制取纯净、干燥的二氧化碳,并用排空气法收集CO2(碳酸氢钠可以与盐酸反应生成 二氧化碳)。仪器的连接顺序为a接d,e接b,c接_____ ,原因是 _____ 。仪器①的名 称是_____ 仪器②的名称是_____ 。
(3)二氧化碳是一种重要的化工原料。
①在纳米纤维催化剂条件下,二氧化碳和氢气反应制得液体燃料甲醇(CH3OH),并生成水。该反应的化学方程式为_____ 。
②在高温、高压条件下,二氧化碳和NH3反应制得重要肥料尿素[CO(NH2)2],并生成水。该反应的化学方程式为_____ 。
(4)将15g石灰石样品(主要成分为碳酸钙),放入质量为20g的烧杯中,再加入50g稀盐酸,充分反应后,称的剩余总质量为80.6g,求石灰石中碳酸钙的质量。

(1)正常雨水的pH<7,是因为雨水降落过程中遇到了空气中的二氧化碳,与二氧化碳反应生成
(2)如图,大理石和盐酸制取纯净、干燥的二氧化碳,并用排空气法收集CO2(碳酸氢钠可以与盐酸反应生成 二氧化碳)。仪器的连接顺序为a接d,e接b,c接
(3)二氧化碳是一种重要的化工原料。
①在纳米纤维催化剂条件下,二氧化碳和氢气反应制得液体燃料甲醇(CH3OH),并生成水。该反应的化学方程式为
②在高温、高压条件下,二氧化碳和NH3反应制得重要肥料尿素[CO(NH2)2],并生成水。该反应的化学方程式为
(4)将15g石灰石样品(主要成分为碳酸钙),放入质量为20g的烧杯中,再加入50g稀盐酸,充分反应后,称的剩余总质量为80.6g,求石灰石中碳酸钙的质量。
您最近一年使用:0次
【推荐1】二氧化碳捕集和资源化利用是碳中和领域研究热点。
Ⅰ.“碳”减排
(1)节能减排是我国的基本国策。过多排放二氧化碳造成______ 效应。
(2)化石燃料的燃烧是CO2排放的主要因素。化石燃料主要包括煤炭、石油和________ 。
Ⅱ.“碳”捕捉,利用NaOH捕捉CO2,得到高纯度CO2的流程如图。

(3)捕捉室内发生的化学反应方程式为_________ 。
(4)转化中可循环使用的物质有_____ 。
Ⅲ.“碳”利用。我国科学家利用CO2合成葡萄糖,该方案先用碳电还原法将CO2转化为醋酸,再利用微生物发酵获得葡萄糖。

(5)通电条件下,装置1中CO2分解成CO和常见单质X,X的化学式为_______ 。
(6)理论上合成葡萄糖所需CO2与H2O的质量比为________ 。
Ⅰ.“碳”减排
(1)节能减排是我国的基本国策。过多排放二氧化碳造成
(2)化石燃料的燃烧是CO2排放的主要因素。化石燃料主要包括煤炭、石油和
Ⅱ.“碳”捕捉,利用NaOH捕捉CO2,得到高纯度CO2的流程如图。

(3)捕捉室内发生的化学反应方程式为
(4)转化中可循环使用的物质有
Ⅲ.“碳”利用。我国科学家利用CO2合成葡萄糖,该方案先用碳电还原法将CO2转化为醋酸,再利用微生物发酵获得葡萄糖。

(5)通电条件下,装置1中CO2分解成CO和常见单质X,X的化学式为
(6)理论上合成葡萄糖所需CO2与H2O的质量比为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】能源利用和环境保护是人类共同关注的问题。
(1)化石燃料包括煤、______ 、天然气。
(2)煤燃烧时排放的 等污染物会形成
等污染物会形成______ 。目前世界各国都大力提倡使用新能源,请写出一种新能源的名称______ 。
(3)为推动形成绿色低碳的生产方式和生活方式,在工业生产中,要尽量吸收不可避免的碳排放。一种利用NaOH溶液来吸收 的流程如图所示。回答下列问题。
的流程如图所示。回答下列问题。______ 。
②一定条件下,合成塔中发生的反应生成甲醇( )和一种常见的液体物质,则发生反应的化学方程式为
)和一种常见的液体物质,则发生反应的化学方程式为______ 。
③甲醇是一种无色透明,具有挥发性的液体,有毒性,能损伤视神经。在空气中燃烧生成水和二氧化碳。可用于制造生长促进剂,还可以用来生产甲醛。下列有关甲醇的用途,说法正确的是______ (填标号)。
A.作为燃料 B.用于配制饮用酒
C.制甲醛 D.制造生长促进剂
(1)化石燃料包括煤、
(2)煤燃烧时排放的
 等污染物会形成
等污染物会形成(3)为推动形成绿色低碳的生产方式和生活方式,在工业生产中,要尽量吸收不可避免的碳排放。一种利用NaOH溶液来吸收
 的流程如图所示。回答下列问题。
的流程如图所示。回答下列问题。
②一定条件下,合成塔中发生的反应生成甲醇(
 )和一种常见的液体物质,则发生反应的化学方程式为
)和一种常见的液体物质,则发生反应的化学方程式为③甲醇是一种无色透明,具有挥发性的液体,有毒性,能损伤视神经。在空气中燃烧生成水和二氧化碳。可用于制造生长促进剂,还可以用来生产甲醛。下列有关甲醇的用途,说法正确的是
A.作为燃料 B.用于配制饮用酒
C.制甲醛 D.制造生长促进剂
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】我国科学家发现了CO2高效转化新过程,首次把二氧化碳加氢“变”成汽油,这一技术有望减轻对传统化石能源的依赖。
(1)化石能源主要包含煤、石油、天然气,化石燃料属于___________ (填“纯净物”、“混合物”),在使用过程中排放出大量的CO2造成的环境问题是___________ 。
(2)植物通过___________ 吸收二氧化碳,生成葡萄糖和氧气,该过程___________ (填“是”、“否”)属于缓慢氧化。
(3)制氢、二氧化碳加氢制备汽油流程如下图
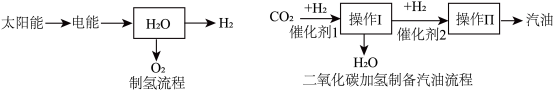
①制氢流程中生成H2和O2的质量比是___________ 。
②若汽油主要成分为C8H18,则二氧化碳加氢制备C8H18的化学式的表达式为___________ 。
(1)化石能源主要包含煤、石油、天然气,化石燃料属于
(2)植物通过
(3)制氢、二氧化碳加氢制备汽油流程如下图

①制氢流程中生成H2和O2的质量比是
②若汽油主要成分为C8H18,则二氧化碳加氢制备C8H18的化学式的表达式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】实验室利用如图所示实验装置进行有关化学实验,回答下列问题:
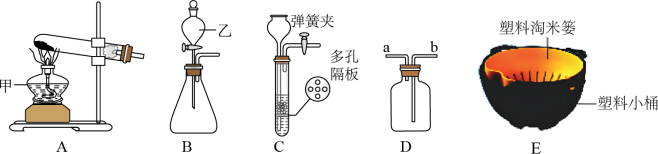
(1)写出图中仪器乙的名称:_____ 。
(2)实验室用高锰酸钾制取氧气,发生装置可选择图中的_____ (填标号),写出该反应的化学方程式_____ ,用D收集氧气的验满方法是_____ 。
(3)实验室制取二氧化碳的化学方程式是_____ ,可以在D装置中盛放_____ (填名称)来检验二氧化碳,气体应从_____ (填“a”或“b”)通入。反应的化学方程式是_____ ,实验结束后老师要求同学们将反应剩余物倒入如图E所示的下有小桶的塑料淘米篓中,这样做除了可以集中处理废液以外,还可以回收_____ 。
(4)装置B、C均可用于实验室制取二氧化碳,装置C与装置B相比其优点是_____ ,停止反应时应采取的措施_____ 。
(5)某课外小组对过氧化氢分解反应进行探究,实验条件及产生的现象见下表:
根据以上信息回答下列问题:
I.写出实验④的化学方程式是:_____ 。
Ⅱ.实验①与②探究的目的是:_____ 。
Ⅲ.实验③与④的实验结论是:_____ 。
Ⅳ.通过实验①与④的实验现象对比,可知道FeC13可以改变反应速率,但为了证明FeCl3是该反应的催化剂,还需验证FeC13在反应前后_____ 不变。
(6)实验室常用5%的H2O2溶液在二氧化锰催化作用下获得平稳的氧气流。现有17%的H2O2溶液,能达到此效果的最佳装置是______。

(1)写出图中仪器乙的名称:
(2)实验室用高锰酸钾制取氧气,发生装置可选择图中的
(3)实验室制取二氧化碳的化学方程式是
(4)装置B、C均可用于实验室制取二氧化碳,装置C与装置B相比其优点是
(5)某课外小组对过氧化氢分解反应进行探究,实验条件及产生的现象见下表:
| 实验序号 | 实验温度℃ | 催化剂 | 5%H2O2溶液体积 | 实验现象 |
| ① | 20 | 无 | 10mL | 无明显现象 |
| ② | 50 | 无 | 10mL | 有气泡产生 |
| ③ | 20 | 1gCuSO4 | 10mL | 有气泡产生 |
| ④ | 20 | 1gFeCl3 | 10mL | 有气泡产生【比③快速】 |
I.写出实验④的化学方程式是:
Ⅱ.实验①与②探究的目的是:
Ⅲ.实验③与④的实验结论是:
Ⅳ.通过实验①与④的实验现象对比,可知道FeC13可以改变反应速率,但为了证明FeCl3是该反应的催化剂,还需验证FeC13在反应前后
(6)实验室常用5%的H2O2溶液在二氧化锰催化作用下获得平稳的氧气流。现有17%的H2O2溶液,能达到此效果的最佳装置是______。
A.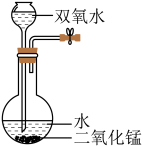 | B. |
C.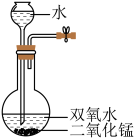 | D.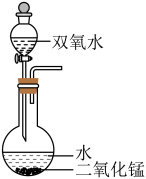 |
您最近一年使用:0次
【推荐2】碳和氧元素是重要元素,是化学研究的重要内容。

(1)碳元素的价类二维图如图所示。图中a为_____ ,从微观的角度解释Z和Y化学性质有差异的原因_____ 。
(2)下图是实验室制取气体的常用装置。

①A装置试管口略向下倾斜的原因_____ 。
②写出利用B装置制取氧气的化学方程式_____ 。
③收集某气体只能采用E装置,该气体具有的物理性质是_____ 。
④用盛满水的G装置收集氧气,并测定气体的体积,应在_____ 端(填“左、右”)连接上一个量筒。
⑤常温下块状电石(主要成分CaC2)与水会剧烈反应,快速产生乙炔(C2H2)气体,乙炔气体难溶于水。实验室如果利用该反应制取一瓶乙炔气体。你认为最适合一套装置为_____ 。
⑥小明用加热高锰酸钾的方法制取氧气,反应前高锰酸钾和试管的总质量为26.4克,完全反应后剩余固体与试管的总质量为24.8克,反应前试管中的高锰酸钾的质量是多少克_____ 。

(1)碳元素的价类二维图如图所示。图中a为
(2)下图是实验室制取气体的常用装置。

①A装置试管口略向下倾斜的原因
②写出利用B装置制取氧气的化学方程式
③收集某气体只能采用E装置,该气体具有的物理性质是
④用盛满水的G装置收集氧气,并测定气体的体积,应在
⑤常温下块状电石(主要成分CaC2)与水会剧烈反应,快速产生乙炔(C2H2)气体,乙炔气体难溶于水。实验室如果利用该反应制取一瓶乙炔气体。你认为最适合一套装置为
⑥小明用加热高锰酸钾的方法制取氧气,反应前高锰酸钾和试管的总质量为26.4克,完全反应后剩余固体与试管的总质量为24.8克,反应前试管中的高锰酸钾的质量是多少克
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】碳及其化合物是初中化学学习的重要内容,某化学兴趣小组做了关于碳的实验研究。
(1)构成物质的微粒有多种,其中由分子构成的是____ (填字母)。
a.石墨 b. c.金刚石 d.木炭
c.金刚石 d.木炭
(2)我国春秋时期已经开始冶铁和使用铁器,如图是实验室用 还原
还原 模拟炼铁的装置图;
模拟炼铁的装置图;____________ ,装置B中的实验现象是___________ ;
②从环保角度考虑,写出一种尾气处理的方法______________ ;
(3)如图是实验室制取气体的部分装置________ ;
②实验室制取纯净干燥的 ,所需装置从左到右的正确连接顺序为a接
,所需装置从左到右的正确连接顺序为a接______ ,______ 接______ ,______ 接______ (填导管口处小写字母);
③实验室用电石固体与饱和食盐水在常温下发生剧烈反应制取乙炔 气体,同时有糊状
气体,同时有糊状 生成,选择的发生装置是
生成,选择的发生装置是__________ (填“A”或“B”)。
(4)为测定某石灰石样品中碳酸钙的质量分数,称取 石灰石(杂质不参加反应)放入烧杯中,加入
石灰石(杂质不参加反应)放入烧杯中,加入 稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为
稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为 (气体的溶解忽略不计),请计算该样品中碳酸钙的质量分数。
(气体的溶解忽略不计),请计算该样品中碳酸钙的质量分数。
(1)构成物质的微粒有多种,其中由分子构成的是
a.石墨 b.
 c.金刚石 d.木炭
c.金刚石 d.木炭(2)我国春秋时期已经开始冶铁和使用铁器,如图是实验室用
 还原
还原 模拟炼铁的装置图;
模拟炼铁的装置图;
②从环保角度考虑,写出一种尾气处理的方法
(3)如图是实验室制取气体的部分装置

②实验室制取纯净干燥的
 ,所需装置从左到右的正确连接顺序为a接
,所需装置从左到右的正确连接顺序为a接③实验室用电石固体与饱和食盐水在常温下发生剧烈反应制取乙炔
 气体,同时有糊状
气体,同时有糊状 生成,选择的发生装置是
生成,选择的发生装置是(4)为测定某石灰石样品中碳酸钙的质量分数,称取
 石灰石(杂质不参加反应)放入烧杯中,加入
石灰石(杂质不参加反应)放入烧杯中,加入 稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为
稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为 (气体的溶解忽略不计),请计算该样品中碳酸钙的质量分数。
(气体的溶解忽略不计),请计算该样品中碳酸钙的质量分数。
您最近一年使用:0次



