图甲为KNO3与NaC1的溶解度曲线,请根据图中信息,回答下列问题。
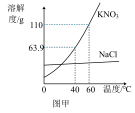
(1)60℃时,KNO3和NaCl中溶解度较小的是______ 。
(2)60℃时,对一定质量的KNO3溶液进行恒温蒸发溶剂的操作,溶液质量与蒸发水的质量变化关系如图乙所示,则下列相关说法中错误的是______。

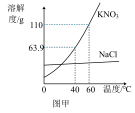
(1)60℃时,KNO3和NaCl中溶解度较小的是
(2)60℃时,对一定质量的KNO3溶液进行恒温蒸发溶剂的操作,溶液质量与蒸发水的质量变化关系如图乙所示,则下列相关说法中错误的是______。

| A.恒温蒸发到最后烧杯中大约剩61.9g固体 |
| B.b、c、d点对应溶液溶质质量分数一定相等,且大于a点溶液溶质质量分数 |
| C.c点对应溶液的质量为77.5g |
| D.a点对应溶液质量为155g |
| E.若要把硝酸钾全部从其溶液中提取出来,须采用蒸发结晶的方法 |
| F.线段bc长度与线段cd长度的比值无法确定 |
更新时间:2023-07-09 22:17:36
|
相似题推荐
【推荐1】溶液是生活中常用的混合物。
(1)硫酸铜溶液可用于游泳池消毒,硫酸铜溶液中的溶质是_______ 。
(2)市售的过氧乙酸(CH3COOOH)溶液中溶质的质量分数大多为40%,稳定性差,室温下就可分解成乙酸(CH3COOH),并释放出氧气,该反应的化学方程式为_______ 。将40% 的过氧乙酸溶液稀释成2%,可用于空气消毒, 稀释过程中浓溶液与所加水的质量比为 _______ 。
(3)甲、乙两种固体物质的溶解度曲线如图2所示。20℃时,将等质量的甲、乙分别放入盛有100g水的烧杯中,充分搅拌并升温至50℃时,实验现象如图1所示。请结合图示回答下列问题:

①曲线N表示_______ (填“甲”或“乙”)的溶解度随温度变化的情况。
②图1所示的四种溶液中,溶质质量分数最小的是_______ (填字母序号,下同),一定不饱和的是 _______ 。
(1)硫酸铜溶液可用于游泳池消毒,硫酸铜溶液中的溶质是
(2)市售的过氧乙酸(CH3COOOH)溶液中溶质的质量分数大多为40%,稳定性差,室温下就可分解成乙酸(CH3COOH),并释放出氧气,该反应的化学方程式为
(3)甲、乙两种固体物质的溶解度曲线如图2所示。20℃时,将等质量的甲、乙分别放入盛有100g水的烧杯中,充分搅拌并升温至50℃时,实验现象如图1所示。请结合图示回答下列问题:

①曲线N表示
②图1所示的四种溶液中,溶质质量分数最小的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】下图是A、B、C是三种固体物质不含结晶水)的溶解度曲线,根据图示回答:

①d点的含义_________________
②t1℃时将20克A物质与50克水混合所得溶液是__________ (填“饱和"或“不饱和")溶液。
③t2℃等质量的A、B、C三种溶液分别加入水配成该温度下的饱和溶液,所得溶液质量由大到小的顺序为__________
④将40克c点所在的溶液降温到a点,析出晶体_________ 克。
⑤将t3℃时等质量的A、B、C三种物质的饱和溶液降温到tl℃,下列说法正确的是________
Ⅰ.都是饱和溶液 Ⅱ.析出溶质的质量:A>B>C
Ⅲ.溶剂质量A>B>C Ⅳ.溶液质量C>B>A

①d点的含义
②t1℃时将20克A物质与50克水混合所得溶液是
③t2℃等质量的A、B、C三种溶液分别加入水配成该温度下的饱和溶液,所得溶液质量由大到小的顺序为
④将40克c点所在的溶液降温到a点,析出晶体
⑤将t3℃时等质量的A、B、C三种物质的饱和溶液降温到tl℃,下列说法正确的是
Ⅰ.都是饱和溶液 Ⅱ.析出溶质的质量:A>B>C
Ⅲ.溶剂质量A>B>C Ⅳ.溶液质量C>B>A
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验。


(1)t2℃时,氯化铵的饱和溶液中溶质质量分数是______ (结果精确到0.1%)。
(2)根据图1、图2信息可推出M是_______ 。(填化学式)
(3)关于图2中烧杯内的物质,以下几种说法正确的有 (填字母序号)。
(4)将t3℃时等质量硝酸钾和氯化铵的饱和溶液,降温至t1℃,所得溶液中溶质质量的大小关系是 (填字母序号)。


(1)t2℃时,氯化铵的饱和溶液中溶质质量分数是
(2)根据图1、图2信息可推出M是
(3)关于图2中烧杯内的物质,以下几种说法正确的有 (填字母序号)。
| A.①和②的溶液中,溶质质量相等 |
| B.若使③中的固体溶解,可采用加水或升温的方法 |
| C.①、②、③的溶液中,上层清液是饱和溶液的有③ |
| D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小 |
(4)将t3℃时等质量硝酸钾和氯化铵的饱和溶液,降温至t1℃,所得溶液中溶质质量的大小关系是 (填字母序号)。
| A.硝酸钾=氯化铵 | B.硝酸钾<氯化铵 | C.硝酸钾>氯化铵 | D.无法确定 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】氯化钠和硫酸镁的溶解度曲线与若干温度下的溶解度表如下:

请回答下列问题:
(1)80℃时,硫酸镁的溶解度为__________ ,溶解度曲线甲所代表的物质是__________ 。a点对应的温度t1范围是____________________ 。
(2)t2℃时有含有较多NaCl 的MgSO4溶液,为了得到纯净的MgSO4,可采用的方法__________
(3)40℃时把20g NaCl放入50g水中,形成的溶液中溶质质量分数为__________ (精确到0.1%),要使t3℃饱和的MgSO4溶液中溶质质量分数增大,可采用的措施是__________ 。
| 温度/℃ | 20 | 30 | 40 | 60 | 80 | 90 | 100 | |
| 溶解度 (g/100GH20) | NaCl | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.0 | 39.8 |
| MgSO4 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 | 52.9 | 50.4 | |

请回答下列问题:
(1)80℃时,硫酸镁的溶解度为
(2)t2℃时有含有较多NaCl 的MgSO4溶液,为了得到纯净的MgSO4,可采用的方法
(3)40℃时把20g NaCl放入50g水中,形成的溶液中溶质质量分数为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】甲、乙两种固体物质的溶解度曲线如图1所示(其中一种是KNO3):


(1)t2℃时,溶解度大小关系为:甲_______ 乙(填“>”、“<”或“=”);
(2)图2“操作X”可能是 (填序号,下同);
(3)下列说法正确的是 ;
(4)t2℃时,等质量的甲、乙饱和溶液降温到t1℃,下列说法正确的是 。


(1)t2℃时,溶解度大小关系为:甲
(2)图2“操作X”可能是 (填序号,下同);
| A.加适量硝酸钾 | B.蒸发适量水 |
| C.降低温度 | D.升高温度 |
| A.由图2推测硝酸钾是图1中的甲物质 |
| B.t2℃时,甲的饱和溶液的溶质质量分数为80% |
| C.甲中混有少量乙,可采用降温结晶的方法提纯甲 |
| D.将KNO3溶液经过某种操作后,析出KNO3晶体,过滤后所得溶液溶质的质量分数一定比原溶液小 |
| A.溶液质量:甲<乙 |
| B.溶质质量:甲=乙 |
| C.溶质质量分数:甲=乙 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】如图是硝酸钾和氯化钾的溶解度曲线图,据图回答下列问题:

(1)当温度______ ℃时,硝酸钾的溶解度小于氯化钾的溶解度。
(2)t1℃时,分别将30g硝酸钾和氯化钾加入到100g水中,充分溶解后形成两种溶液。两种溶液的溶质质量分数的大小关系是硝酸钾______ 氯化钾(填“>”、“=”或“<”表示)。
(3)t3℃时,将200g硝酸钾饱和溶液、100g硝酸钾饱和溶液、100g氯化钾饱和溶液分别恒温蒸发10g水,析出晶体(不含结晶水)质量分别为A、B、C,则______ (填A、B、C的大小关系)。
(4)某小组进行如下图实验,X物质是硝酸钾或氯化钾中的一种,下列说法正确的的是______。


(1)当温度
(2)t1℃时,分别将30g硝酸钾和氯化钾加入到100g水中,充分溶解后形成两种溶液。两种溶液的溶质质量分数的大小关系是硝酸钾
(3)t3℃时,将200g硝酸钾饱和溶液、100g硝酸钾饱和溶液、100g氯化钾饱和溶液分别恒温蒸发10g水,析出晶体(不含结晶水)质量分别为A、B、C,则
(4)某小组进行如下图实验,X物质是硝酸钾或氯化钾中的一种,下列说法正确的的是______。

| A.X物质是氯化钾 | B.溶质的质量分数②>③=① |
| C.只有烧杯③中上层清液是饱和溶液 | D.烧杯③中析出固体质量为25g |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图是甲、乙、丙三种固体物质的溶解度曲线,据图回答下列问题。

(1)0℃时,乙物质的溶解度是______ 。
(2)t1℃时,三种物质溶解度由大到小的顺序是______ 。
(3)t3℃时,将40g甲物质加到50g水中,充分搅拌后所得溶液的质量是______ g,其质量分数为______ 。
(4)t3℃时,将甲、丙两物质的饱和溶液同时降温至______ ℃,它们溶质的质量分数相等。
(5)将甲乙丙的饱和溶液从t3℃降温到t2℃,溶质的质量分数由大到小是______ 。

(1)0℃时,乙物质的溶解度是
(2)t1℃时,三种物质溶解度由大到小的顺序是
(3)t3℃时,将40g甲物质加到50g水中,充分搅拌后所得溶液的质量是
(4)t3℃时,将甲、丙两物质的饱和溶液同时降温至
(5)将甲乙丙的饱和溶液从t3℃降温到t2℃,溶质的质量分数由大到小是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】水是生命之源,也是人类最宝贵的资源.用你学过的化学知识回答下列问题:
(1)某同学在完成电解水实验时,发现正极产生了10mL气体,则负极产生的气体体积是_____ .
(2)20℃时,等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙物质的溶解度曲线如图3.

①图3中,表示甲的溶解度曲线是_____ (填“M”或“N”);
②50℃时,20克乙物质中加入50g水后所得溶液的溶质的质量分数是_____ ;(结果保留到0.1%)
③根据图中信息下列说法正确的是_____ .(填字母序号)
A 图2中乙溶液一定不饱和
B 图2中两溶液中溶质质量分数一定相等
C 图2中的甲乙溶液降温至30℃时其溶质质量分数一定相等
D 图2中乙溶液降温至30℃无晶体析出.
(1)某同学在完成电解水实验时,发现正极产生了10mL气体,则负极产生的气体体积是
(2)20℃时,等质量的甲、乙固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙物质的溶解度曲线如图3.

①图3中,表示甲的溶解度曲线是
②50℃时,20克乙物质中加入50g水后所得溶液的溶质的质量分数是
③根据图中信息下列说法正确的是
A 图2中乙溶液一定不饱和
B 图2中两溶液中溶质质量分数一定相等
C 图2中的甲乙溶液降温至30℃时其溶质质量分数一定相等
D 图2中乙溶液降温至30℃无晶体析出.
您最近一年使用:0次
【推荐1】碘酸钾(KIO3)主要用作食盐加碘剂,我省实施的新的碘盐含碘量标准,碘盐中碘含量从每千克35毫克降至25毫克,已知碘酸钾的热稳定性好,氯化钠和碘酸钾的溶解度如下图所示:

(1)50℃时碘酸钾的溶解度为_______ 。
(2)将30℃质量为220.0g的碘酸钾饱和溶液升温到50℃,需加入_______ g碘酸钾才能变成饱和溶液。
(3)若某碘酸钾溶液中含有少量的氯化钠,为了得到比较纯净的碘酸钾,你建议采用的方法为_______ 。(填序号)
A 迅速升温、蒸发结晶、过滤、热水洗涤、干燥
B 蒸发浓缩、降温结晶、过滤、热水洗涤、干燥
C 蒸发浓缩、降温结晶、过滤、冰水洗涤、干燥
(4)t℃时,若要使m克质量分数为15%的碘酸钾溶液变为20%,采用的方法可以是_______ 。(填序号)
A 蒸发掉0.25m克水 B 蒸发掉原溶液中溶剂质量的1/3
C 再加入0.05m克的KIO3粉末 D 加入0.4m克40%的KIO3溶液

(1)50℃时碘酸钾的溶解度为
(2)将30℃质量为220.0g的碘酸钾饱和溶液升温到50℃,需加入
(3)若某碘酸钾溶液中含有少量的氯化钠,为了得到比较纯净的碘酸钾,你建议采用的方法为
A 迅速升温、蒸发结晶、过滤、热水洗涤、干燥
B 蒸发浓缩、降温结晶、过滤、热水洗涤、干燥
C 蒸发浓缩、降温结晶、过滤、冰水洗涤、干燥
(4)t℃时,若要使m克质量分数为15%的碘酸钾溶液变为20%,采用的方法可以是
A 蒸发掉0.25m克水 B 蒸发掉原溶液中溶剂质量的1/3
C 再加入0.05m克的KIO3粉末 D 加入0.4m克40%的KIO3溶液
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】为了探究影响固体溶解性的因素,某同学设计了如下三组实验:
(1)分析上表,第一组实验研究的因素是_______ 。
(2)有上述实验可知,影响固体溶解性的因素是_______ 。(填标号)
①温度 ②加入溶剂种类 ③加入溶剂质量 ④加入固体种类 ⑤加入固体质量
(3)在第二组实验中,该同学按照如下步骤进行实验(假设溶液损失不计,水的密度是1g/mL)
①用电子天平称取10.0g硝酸钾,放入烧杯中;
②量取10.0mL水,倒入上述烧杯中,称量烧杯、硝酸钾和水的总质量为m1g;
③搅拌至硝酸钾不再溶解为止;
④过滤,称量所得硝酸钾溶液和烧杯的总质量为m2g
⑤计算:m1-m2=_______ g(结合第二组实验数据进行分析)。
将溶质改为氯化钠,重复上述步骤进行实验。
由实验可知,20℃时氯化钠的溶解度_______ (填“>”“=”“<”)硝酸钾的溶解度。
(4)根据上述实验,以下推论错误的是(填标号)
| 因素 | 第一组 | 第二组 | 第三组 | ||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80℃ |
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 |
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g |
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 氯化钠 | 硝酸钾 |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | 3.1g | 3.6g | 10g |
(2)有上述实验可知,影响固体溶解性的因素是
①温度 ②加入溶剂种类 ③加入溶剂质量 ④加入固体种类 ⑤加入固体质量
(3)在第二组实验中,该同学按照如下步骤进行实验(假设溶液损失不计,水的密度是1g/mL)
①用电子天平称取10.0g硝酸钾,放入烧杯中;
②量取10.0mL水,倒入上述烧杯中,称量烧杯、硝酸钾和水的总质量为m1g;
③搅拌至硝酸钾不再溶解为止;
④过滤,称量所得硝酸钾溶液和烧杯的总质量为m2g
⑤计算:m1-m2=
将溶质改为氯化钠,重复上述步骤进行实验。
由实验可知,20℃时氯化钠的溶解度
(4)根据上述实验,以下推论错误的是(填标号)
| A.20℃时,氯化钠的溶解度为36 |
| B.20℃时,硝酸钾饱和溶液的溶质质量分数为31% |
| C.第三组实验中得到的硝酸钾溶液肯定是饱和溶液 |
| D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
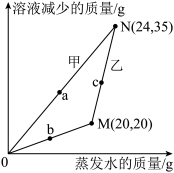
【推荐3】t°C时,将一定质量的甲、乙溶液恒温蒸发,蒸发溶剂的质量与溶液减少的质量之间的关系如图所示(M和N的坐标由图可知)。 _______ 点(填“a”“b”或“c”)
(2)t°C时,_______ (填“甲”或“乙”)的溶解度更大;
(3)乙的饱和溶液溶质质量分数为_______ (保留0.1%)。
(4)下列关于图像的说法正确的有_______ 。
①N点表示t°C时甲和乙的溶解度相等
②甲、乙溶液分别在a和b状态时,溶液中所含溶质的质量可能相等
③甲中含有少量的乙时,一定能用降温结晶的方法提纯甲
④x°C时,质量不相等的甲、乙饱和溶液,蒸发相同质量的溶剂,析出固体质量:甲<乙
(2)t°C时,
(3)乙的饱和溶液溶质质量分数为
(4)下列关于图像的说法正确的有
①N点表示t°C时甲和乙的溶解度相等
②甲、乙溶液分别在a和b状态时,溶液中所含溶质的质量可能相等
③甲中含有少量的乙时,一定能用降温结晶的方法提纯甲
④x°C时,质量不相等的甲、乙饱和溶液,蒸发相同质量的溶剂,析出固体质量:甲<乙
您最近一年使用:0次




