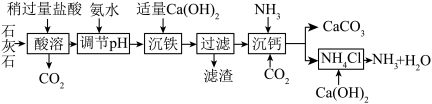
兴趣小组在实验室用某石灰石(含少量Fe2O3)为原料制备高纯CaCO3的流程如图所示,请回答下列问题:______ 。
(2)“沉钙”时发生反应的化学方程式为: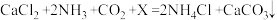 ,X的化学式为
,X的化学式为______ 。
(3)“沉钙”中,其他条件相同,当温度高于35℃时CaCO3产率会明显下降,其主要原因:一是氨水挥发和分解速率加快,二是______ 。
(4)流程中可循环利用的物质有______ (写一种)。
(2)“沉钙”时发生反应的化学方程式为:
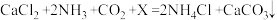 ,X的化学式为
,X的化学式为(3)“沉钙”中,其他条件相同,当温度高于35℃时CaCO3产率会明显下降,其主要原因:一是氨水挥发和分解速率加快,二是
(4)流程中可循环利用的物质有
2023·黑龙江牡丹江·中考真题 查看更多[12]
2023年黑龙江省牡丹江市中考化学真题(已下线)专题20 工艺流程图题(第03期)-学易金卷:2023年中考化学真题分项汇编(全国通用)(已下线)XDRzkgshxzw963山东省淄博市张店区2023-2024学年九年级上学期1月期末化学试题山东省淄博市高新片区2023-2024学年九年级上学期期末化学试题(已下线)2024年中考风向标-全国-流程图(已下线)专题05 工业流程题(题型专练)-备战2024年中考化学一轮复习考点帮(沪教版·全国)(已下线)题型突破06 工艺流程题-备战2024年中考化学复习题型突破学·练·考(全国通用)2024中考一轮复习考点微专题-专题16质量守恒定律、化学方程式-考点2024年湖北省十堰市店子镇初级中学化学中考模拟题5(已下线)专题11??工业流程题-2024年中考化学二轮热点题型归纳与变式演练(全国通用)(已下线)题型三 工艺流程题(讲练)-2024年中考化学二轮复习讲练测(全国通用)
更新时间:2023-07-12 01:21:57
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】空气是一种重要资源:
(一)防治空气污染、改善生态环境已成为全民共识。近年来,一些城市空气中出现可吸入悬浮颗粒物与雾形成“雾霾”天气。粒径不大于 2.5μm 的可吸入悬浮颗粒物(PM2.5) 富含大量有毒、有害物质。
(1)下列行为可能会导致“雾霾”加重的是__________ (填标号)。
a.燃煤脱硫 b.植树造林 c.静电除尘 d.燃放鞭炮
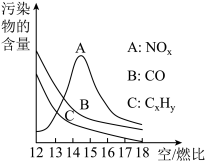
(2)为了减少雾霾、降低大气中有害气体含量, 研究机动车尾气中CO、NOx及 CxHy 的排放意义重大。机动车尾气污染物的含量与“空/燃比”(空气与燃油气的体积比)的变化关系如图所示。
①利用氨气可将汽车尾气中的氮氧化物 (NOx)在一定条件下转化未对空气无污染的物质。请将该反应的化学方程式补充完整:
4xNH3+6NOx (2 x+3)N2+
(2 x+3)N2+ ___ 。
②随着空燃比增大,CO 和 CxHy 的含量减少的原因是__ 。
(3)CH4、乙炔 (C2H2)和丙烷 (C3H8)都能在空气中燃烧,但是仅 C2H2 燃烧时有浓烟,试从物质组成的角度分析其燃烧现象不同的原因是:___ 。写出丙烷在空气中完全燃烧的化学方程式 _____ 。
(二)用如图装置测定空气中氧气的体积分数。

①如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。红磷燃烧的化学方程式为______ 。 由该实验可得出结论为:氧气约占空气总体积的 ______ 。瓶中剩余的气体主要是 ___ 。
②如果测定的结果低于该体积含量,则可能的原因是______ (填序号)。
A.红磷过量
B.装置漏气
C.实验过程中弹簧夹未夹紧,气体沿导管逸出
D.未冷却至室温就打开了弹簧夹
(一)防治空气污染、改善生态环境已成为全民共识。近年来,一些城市空气中出现可吸入悬浮颗粒物与雾形成“雾霾”天气。粒径不大于 2.5μm 的可吸入悬浮颗粒物(PM2.5) 富含大量有毒、有害物质。
(1)下列行为可能会导致“雾霾”加重的是
a.燃煤脱硫 b.植树造林 c.静电除尘 d.燃放鞭炮
(2)为了减少雾霾、降低大气中有害气体含量, 研究机动车尾气中CO、NOx及 CxHy 的排放意义重大。机动车尾气污染物的含量与“空/燃比”(空气与燃油气的体积比)的变化关系如图所示。

①利用氨气可将汽车尾气中的氮氧化物 (NOx)在一定条件下转化未对空气无污染的物质。请将该反应的化学方程式补充完整:
4xNH3+6NOx
 (2 x+3)N2+
(2 x+3)N2+ ②随着空燃比增大,CO 和 CxHy 的含量减少的原因是
(3)CH4、乙炔 (C2H2)和丙烷 (C3H8)都能在空气中燃烧,但是仅 C2H2 燃烧时有浓烟,试从物质组成的角度分析其燃烧现象不同的原因是:
(二)用如图装置测定空气中氧气的体积分数。

①如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。红磷燃烧的化学方程式为
②如果测定的结果低于该体积含量,则可能的原因是
A.红磷过量
B.装置漏气
C.实验过程中弹簧夹未夹紧,气体沿导管逸出
D.未冷却至室温就打开了弹簧夹
您最近一年使用:0次
【推荐2】2017年5月5日,C919大型客机在浦东机场成功起飞。第三代铝锂合金材料在C919机体结构中的用量达到8.8%。
(1)下列客机上使用的物品中,属于合成材料的是______(填序号)。
(2)金属铍(Be)与铝化学性质相似,铍元素的核电荷数为4,相对原子质量为9,易失电子,化合价为+2价。
①铍原子结构示意图为______ (填序号)。

②在空气中,铍的表面易形成一层氧化铍的保护膜,发生反应的化学方程式为:______ 。
(3)目前“哈罗”等品牌的共享单车成为城市新一轮热门话题。如图是一款共享单车示意图:

①请用微粒的基本性质解释给自行车打气,空气能被压入车胎内的原因______ 。
②请说出一种共享单车利用的防锈方法:______ 。
(4)2018年4月2日,天宫一号目标飞行器在圆满完成任务并超期服役多年后再入大气层。天宫一号在太空中工作需要太阳能硅电池板提供动力。工业上制备硅的反应为2C+SiO2 Si+2X,则X的化学式为
Si+2X,则X的化学式为______ ,该反应属于______ (填写基本反应类型)。

(5)化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:
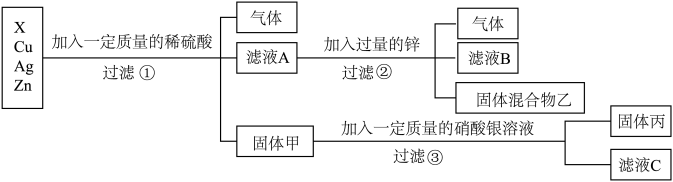
下列说法正确的是______;
(1)下列客机上使用的物品中,属于合成材料的是______(填序号)。
| A.合金门把手 | B.真皮椅套 | C.塑料快餐盒 | D.羊毛毯子 |
(2)金属铍(Be)与铝化学性质相似,铍元素的核电荷数为4,相对原子质量为9,易失电子,化合价为+2价。
①铍原子结构示意图为

②在空气中,铍的表面易形成一层氧化铍的保护膜,发生反应的化学方程式为:
(3)目前“哈罗”等品牌的共享单车成为城市新一轮热门话题。如图是一款共享单车示意图:

①请用微粒的基本性质解释给自行车打气,空气能被压入车胎内的原因
②请说出一种共享单车利用的防锈方法:
(4)2018年4月2日,天宫一号目标飞行器在圆满完成任务并超期服役多年后再入大气层。天宫一号在太空中工作需要太阳能硅电池板提供动力。工业上制备硅的反应为2C+SiO2
 Si+2X,则X的化学式为
Si+2X,则X的化学式为
(5)化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属。流程如下:

下列说法正确的是______;
| A.固体丙中一定只含有银 |
| B.四种金属的活动性顺序由强到弱的是Zn、X、Cu、Ag |
| C.滤液C中一定含有硝酸铜 |
| D.固体甲中一定含有Cu和Ag,可能含有X |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】工业上用闪锌矿(主要成分是锌、铁的化合物)冶炼锌,主要流程如下:

(1)焙烧炉中,通入氧气后灼烧,补全该反应的化学方程式:_______ +3O2 2ZnO+2SO2。
2ZnO+2SO2。
(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液,反应过程中需不断搅拌,其目的是______ ;
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价),底吹炉中,主要发生如下反应:
①3ZnFe2O4+C 2Fe3O4+3ZnO+CO
2Fe3O4+3ZnO+CO
②ZnFe2O4+CO 2FeO+ZnO+CO2
2FeO+ZnO+CO2
③ZnO+CO Zn(蒸汽)+CO2
Zn(蒸汽)+CO2
反应①-③中,化合价发生改变的元素有______ ;
(4)最终可以获得锌的设备有________ ;

(1)焙烧炉中,通入氧气后灼烧,补全该反应的化学方程式:
 2ZnO+2SO2。
2ZnO+2SO2。(2)酸浸槽中,硫酸与锌焙砂反应得到用于电解的酸浸液,反应过程中需不断搅拌,其目的是
(3)酸浸渣的主要成分是铁酸锌(ZnFe2O4,其中Fe为+3价),底吹炉中,主要发生如下反应:
①3ZnFe2O4+C
 2Fe3O4+3ZnO+CO
2Fe3O4+3ZnO+CO②ZnFe2O4+CO
 2FeO+ZnO+CO2
2FeO+ZnO+CO2③ZnO+CO
 Zn(蒸汽)+CO2
Zn(蒸汽)+CO2反应①-③中,化合价发生改变的元素有
(4)最终可以获得锌的设备有
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】CO2对人类生存、生活有着重大影响,某小组同学对 CO2的相关知识作如下探究。
(一)CO2的制取和性质探究:用如图所示装置制取干燥的 CO2,并对 CO2的部分性质进行探究。

查阅资料 :①二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水;
②浓硫酸具有吸水性。
(1)装置 A 中反应的化学符号表达式为______ 。
(2)为获得干燥的 CO2,装置 B 中试剂 X 应该选用______(填字母)。
(3)仪器 a 名称是______ ,装置 A 中固体和液体改变后实验室也能制取氧气,对应的化学符号表达式为______ 。
(4)收集 CO2并验满。将集满 CO2的锥形瓶与盛有足量氢氧化钠(NaOH)溶液的注射器和传感器密封连接,缓慢的将 NaOH 溶液注入到锥形瓶中,采集信息形成图像。见下图。

①检验装置 C 中 CO2已经集满的方法是______ 。
②随着反应的进行,锥形瓶中压强降低的原因是______ 。
③反应结束后锥形瓶中的压强保持在 40kPa,说明______ 。
(二)CO2相关的碳循环
(5)大米、面粉等食物中的淀粉是绿色植物通过______ 作用合成、转化形成的。
(6)2021 年 9 月,中国科学家发表了利用 CO2、H2人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少 CO2排放,缓解______ (填环境问题)等。
(7)如图为人工合成淀粉的关键步骤。
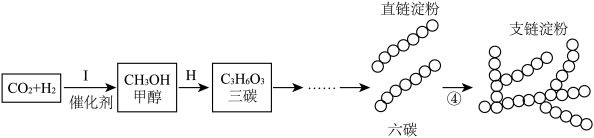
经检测,人工合成的淀粉与天然淀粉在分子组成、结构上一致,实验室可用______(填字母)初步检验出有淀粉生成,会变成蓝色。
(三) CO2的捕集与资源化利用是化学研究的热点。
(8)控制 CO2的排放,加压水洗法可捕集 CO2,是因为压强增大时 CO2在水中的溶解能力______ (填“增大”“不变”或“减小”)。
(9)石灰石循环法可用于捕集烟气中的 CO2,该方法以 CaO 捕集 CO2,将所得产物在高温下煅烧可重新获得 CaO 和 CO2,生成的 CaO 具有疏松多孔的内部结构,其在捕集过程中对CO2具有良好的______ 性。
(10)对 CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是______ (“分子本身”或“分子间的空隙”)。干冰能用于人工降雨,是因为干冰升华______ (填“吸热”或“放热”),使水蒸气凝结成小水滴。
(11)CO2可用于食品保鲜,实验测得,一定条件下,气体中 CO2的体积分数增加,其对应溶液的酸性也随之增加,请回答:
①气体中 CO2体积分数增大时,造成酸性增强的主要原因是 H2CO3浓度增大,请写出生成H2CO3的反应化学符号表达式______ 。
②智能化食品包装通过颜色变化显示包装内 CO2气体含量的变化,举出一种可通过颜色变化用于该智能化包装的物质______ 。
(12)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结果见图-1 和图-2。通过测量其一年内每天空气中 CO2 含量等数据,分析所得碳交换的结果见图-3。碳交换以每月每平方米植物吸收或释放 CO2的质量表示,正值为净吸收 CO2,负值为净释放 CO2。

①由上图可推测,影响公园中植物与大气碳交换的因素有______ 和______ 。
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因素是其一年内每天______ 的变化。
(一)CO2的制取和性质探究:用如图所示装置制取干燥的 CO2,并对 CO2的部分性质进行探究。

查阅资料 :①二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水;
②浓硫酸具有吸水性。
(1)装置 A 中反应的化学符号表达式为
(2)为获得干燥的 CO2,装置 B 中试剂 X 应该选用______(填字母)。
| A.浓 H2SO4 | B.澄清石灰水 | C.氢氧化钠溶液 |
(3)仪器 a 名称是
(4)收集 CO2并验满。将集满 CO2的锥形瓶与盛有足量氢氧化钠(NaOH)溶液的注射器和传感器密封连接,缓慢的将 NaOH 溶液注入到锥形瓶中,采集信息形成图像。见下图。

①检验装置 C 中 CO2已经集满的方法是
②随着反应的进行,锥形瓶中压强降低的原因是
③反应结束后锥形瓶中的压强保持在 40kPa,说明
(二)CO2相关的碳循环
(5)大米、面粉等食物中的淀粉是绿色植物通过
(6)2021 年 9 月,中国科学家发表了利用 CO2、H2人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少 CO2排放,缓解
(7)如图为人工合成淀粉的关键步骤。

经检测,人工合成的淀粉与天然淀粉在分子组成、结构上一致,实验室可用______(填字母)初步检验出有淀粉生成,会变成蓝色。
| A.水 | B.碘酒 | C.生理盐水 |
(三) CO2的捕集与资源化利用是化学研究的热点。
(8)控制 CO2的排放,加压水洗法可捕集 CO2,是因为压强增大时 CO2在水中的溶解能力
(9)石灰石循环法可用于捕集烟气中的 CO2,该方法以 CaO 捕集 CO2,将所得产物在高温下煅烧可重新获得 CaO 和 CO2,生成的 CaO 具有疏松多孔的内部结构,其在捕集过程中对CO2具有良好的
(10)对 CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是
(11)CO2可用于食品保鲜,实验测得,一定条件下,气体中 CO2的体积分数增加,其对应溶液的酸性也随之增加,请回答:
①气体中 CO2体积分数增大时,造成酸性增强的主要原因是 H2CO3浓度增大,请写出生成H2CO3的反应化学符号表达式
②智能化食品包装通过颜色变化显示包装内 CO2气体含量的变化,举出一种可通过颜色变化用于该智能化包装的物质
(12)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结果见图-1 和图-2。通过测量其一年内每天空气中 CO2 含量等数据,分析所得碳交换的结果见图-3。碳交换以每月每平方米植物吸收或释放 CO2的质量表示,正值为净吸收 CO2,负值为净释放 CO2。

①由上图可推测,影响公园中植物与大气碳交换的因素有
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因素是其一年内每天
您最近一年使用:0次
【推荐2】CO2的捕集与资源化利用是化学研究的热点。
(1)控制CO2的排放,是为了减缓_________ 效应,加压水洗法可捕集CO2,是因为压强增大时CO2在水中的溶解度_______ (填“增大”“不变”或“减小”)。
(2)石灰石循环法可用于捕集烟气中的CO2,该方法以CaO捕集CO2,将所得产物在高温下煅烧可重新获得CaO,高温煅烧时反应的化学方程式为_______ ,生成的CaO疏松多孔,结构与活性炭相似,其在捕集过程中对CO2具有良好的_________ 性。
(3)对CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是_______ 。干冰能用于人工降雨,是因为______ 。
(4)CO2可用于食品保鲜,实验测得气体中CO2的体积分数与溶液pH的关系如图-1所示。
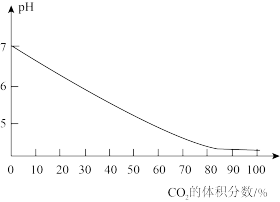
①气体中CO2体积分数增大时,造成图示变化的主要原因是溶液中_______ 浓度增大(填化学式)。
②智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可通过颜色变化用于该智能化包装的物质__________________ 。
(5)已知一定条件下CO2与H2以质量比11:2反应可生成CH4。与该反应类似,不同条件下,CO2与H2反应也能生成甲醇(CH4O)。生成甲醇时参加反应的CO2与H2的质量比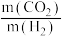 =
=___________ 。
(6)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结果见图-2和图-3。通过测量其一年内每天空气中CO2含量等数据,分析所得碳交换的结果见图-4。碳交换以每月每平方米植物吸收或释放CO2的质量表示,正值为净吸收CO2,负值为净释放CO2。
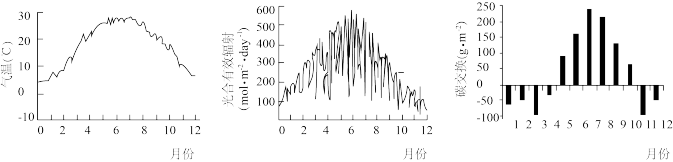
①由上图可推测,影响公园中植物与大气碳交换的因素有_________ 。
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因素是其一年内每天_________ 的变化。
(1)控制CO2的排放,是为了减缓
(2)石灰石循环法可用于捕集烟气中的CO2,该方法以CaO捕集CO2,将所得产物在高温下煅烧可重新获得CaO,高温煅烧时反应的化学方程式为
(3)对CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是
(4)CO2可用于食品保鲜,实验测得气体中CO2的体积分数与溶液pH的关系如图-1所示。

①气体中CO2体积分数增大时,造成图示变化的主要原因是溶液中
②智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可通过颜色变化用于该智能化包装的物质
(5)已知一定条件下CO2与H2以质量比11:2反应可生成CH4。与该反应类似,不同条件下,CO2与H2反应也能生成甲醇(CH4O)。生成甲醇时参加反应的CO2与H2的质量比
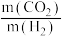 =
=(6)为研究某公园中植物与大气间的碳交换,对该公园一年内每天的气温及光合有效辐射进行测量,结果见图-2和图-3。通过测量其一年内每天空气中CO2含量等数据,分析所得碳交换的结果见图-4。碳交换以每月每平方米植物吸收或释放CO2的质量表示,正值为净吸收CO2,负值为净释放CO2。

①由上图可推测,影响公园中植物与大气碳交换的因素有
②为进一步研究环境因素对公园中植物与大气碳交换的影响,从光合作用的角度出发,还需测量的重要因素是其一年内每天
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】下图为海水吸收CO2并进行碳循环的原理图。

(1)大气中的CO2过多会引发的环境问题是________ 。
(2)“吸收”:吸收大量CO2会导致海水酸化的原因________ (用化学方程式表示)。随着海水温度升高,海水吸收二氧化碳的吸收率在下降,其原因是_________ 。
(3)“钙化”:释放CO2的反应为2NaHCO3 + CaCl2 =CaCO3 + CO2↑ +
+ CO2↑ +_______ + H2O,“吸收”的CO2与“钙化”中释放的CO2的量______ (填“相等”或“不相等”)。
(4)“光合”:绿色植物将二氧化碳转化为有机物,同时伴随的能量转化形式为________ 。

(1)大气中的CO2过多会引发的环境问题是
(2)“吸收”:吸收大量CO2会导致海水酸化的原因
(3)“钙化”:释放CO2的反应为2NaHCO3 + CaCl2 =CaCO3
 + CO2↑ +
+ CO2↑ +(4)“光合”:绿色植物将二氧化碳转化为有机物,同时伴随的能量转化形式为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐1】某白色圆体中可能含有碳酸钠、硝酸钡,氢氧化钠、硫酸铜中的一种或几种,为确定该固体成分固体的成分,现进行以下实验:

(1)白色固体A加入足量水后其中发生的化学方程式是_____ 。
(2)康康为进一步确定固体A中可能存在的物质,对滤液C进行了相关实验,发现固体A中并不含氢氧化钠。请写出康康进行实验的步骤和现象_____ 。
(3)综合以上情况,可知无色滤液C中的溶质是_____ 。

(1)白色固体A加入足量水后其中发生的化学方程式是
(2)康康为进一步确定固体A中可能存在的物质,对滤液C进行了相关实验,发现固体A中并不含氢氧化钠。请写出康康进行实验的步骤和现象
(3)综合以上情况,可知无色滤液C中的溶质是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A~G是初中化学常见的物质,它们之间的转化关系如图所示(部分生成物已略去)。其中A、B、C中均含有同一种元素,D是温室气体,G是重要的调味品。

(1)G的化学式为__________ 。
(2)反应②的化学方程式为____________ 。

(1)G的化学式为
(2)反应②的化学方程式为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展作出了杰出的贡献,他发明的侯氏制碱法大大提高了原料的利用率,其工业流程大致如图:
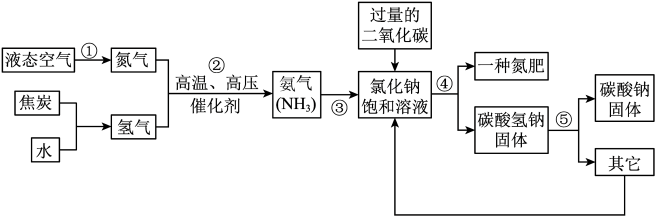
(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、_________ 等.
(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则步骤②、⑤发生反应的化学方程式是:②_________ ,⑤_________ .
(3)上述流程中,可循环利用的物质是_________ .
(4)上述流程中,“一种氮肥”的化学式是_________ .

(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、
(2)上述流程中,已知步骤②发生的是化合反应,步骤⑤发生的是分解反应,则步骤②、⑤发生反应的化学方程式是:②
(3)上述流程中,可循环利用的物质是
(4)上述流程中,“一种氮肥”的化学式是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】比较和分类是学习化学常用的学习方法,请回答问题:
(1)化学反应速率常受到反应温度、反应物接触面积、是否有催化剂等因素的影响,请分析以下四个实验,可以将实验D与实验_____ (填字母)分为一类,分类依据是_____ 。
(2)通过比较可发现:相同的反应物会发生不同的反应。参照示例归纳反应规律。
(1)化学反应速率常受到反应温度、反应物接触面积、是否有催化剂等因素的影响,请分析以下四个实验,可以将实验D与实验
 |  |  |  |
| A | B | C | D |
(2)通过比较可发现:相同的反应物会发生不同的反应。参照示例归纳反应规律。
| 组别 | 化学方程式 | 规律 |
| 示例 | C+O2(充足) CO2 CO22C+O2(不充足)  2CO 2CO | 反应物相同时,反应物的量不同,生成物可能不同。 |
| ① | 4Na+O2═2Na2O 2Na+O2  Na2O2 Na2O2 | 反应物相同时, |
| ② | 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | 反应物相同时, |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】铁红(Fe2O3)是中国传统红色颜料的重要着色剂,以FeSO4为原料制备铁红的一种方法如图1:

(1)“溶解”时能加快溶解的方法有______ (写一种)。
(2)“沉淀”时的主要反应为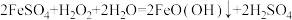 ,则FeO(OH)中铁元素的化合价为
,则FeO(OH)中铁元素的化合价为______ 。
(3)实验室进行过滤操作时需要的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是______ 。
(4)“煅烧” FeO(OH) 时生成两种氧化物,写出“煅烧”时的化学方程式______ 。
(5)如图2为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。
①最适宜的煅烧温度为______ ℃。
②当煅烧温度过高时,产品中Fe2O3质量分数降低,所得产品开始发黑,且铁元素质量分数升高,其可能原因是______ 。

(1)“溶解”时能加快溶解的方法有
(2)“沉淀”时的主要反应为
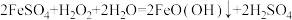 ,则FeO(OH)中铁元素的化合价为
,则FeO(OH)中铁元素的化合价为(3)实验室进行过滤操作时需要的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是
(4)“煅烧” FeO(OH) 时生成两种氧化物,写出“煅烧”时的化学方程式
(5)如图2为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。
①最适宜的煅烧温度为
②当煅烧温度过高时,产品中Fe2O3质量分数降低,所得产品开始发黑,且铁元素质量分数升高,其可能原因是
您最近一年使用:0次




